
01.01.2025
Описание препарата Стрезам® (капсулы, 50 мг) основано на официальной инструкции, утверждено компанией-производителем в 2025 году
Дата согласования: 01.01.2025
Особые отметки:
Содержание
- Действующее вещество
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав
- Описание лекарственной формы
- Фармакологическое действие
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Производитель
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Заказ в аптеках Москвы
Действующее вещество
ATX
Фармакологическая группа
Состав
| Капсулы | 1 капс. |
| действующее вещество: | |
| этифоксина гидрохлорид | 50 мг |
| вспомогательные вещества: лактозы моногидрат; тальк; МКЦ; кремния диоксид коллоидный безводный; магния стеарат | |
| оболочка капсулы: титана диоксид; желатин; индигокармин |
Описание лекарственной формы
Гладкие блестящие желатиновые капсулы №2 с белым корпусом и голубой крышечкой.
Содержимое — порошок белого или белого с легким желтоватым оттенком цвета.
Фармакологическое действие
Фармакодинамика
Этифоксина гидрохлорид принадлежит к производным бензоксазина, обладает анксиолитическим действием, в меньшей степени оказывает седативное действие. Не вызывает привыкания и синдрома отмены. В in vitro и in vivo-исследованиях у крыс и мышей было показано, что анксиолитическая активность этифоксина обусловлена двойным механизмом его действия (прямое и опосредованное) на ГАМК-А-рецепторы, улучшающим ГАМКергическую передачу импульса. При прямом воздействии на ГАМК-А-рецептор путем аллостерической модуляции этифоксин связывается преимущественно с субъединицами β2- или β3-рецептора; исследования показали, что этифоксин связывается с ГАМК-А-рецептором на участках, отличных от мест связывания бензодиазепинов. Непрямое действие обеспечивается посредством увеличения синтеза нейростероидов (с помощью активации митохондриального белка-транслокатора), таких как аллопрегнанолон, также являющегося положительным аллостерическим модулятором ГАМК-А-рецептора.
Фармакокинетика
Быстро всасывается из ЖКТ, быстро метаболизируется в печени до образования нескольких метаболитов. Один из метаболитов (диэтилэтифоксин) является активным, и его T1/2 составляет около 20 часов.
Проникает через плацентарный барьер.
Время достижения Cmax в крови — 2–3 часа, T1/2 — около 6 часов.
Выводится преимущественно с мочой в виде метаболитов, а также в неизмененном виде в небольших количествах. Также выводится с желчью.
Показания
Лечение тревоги и связанных с ней психосоматических расстройств.
Противопоказания
- повышенная чувствительность к действующему веществу или к любому из вспомогательных веществ;
- шоковые состояния (угнетение ЦНС любой этиологии);
- тяжелая печеночная и/или почечная недостаточность;
- миастения;
- пациенты с тяжелыми формами гепатита или цитолизом печени на фоне предшествующего лечения этифоксином;
- пациенты, у которых во время предыдущего лечения этифоксином возникали серьезные кожные реакции, такие как синдром лекарственной гиперчувствительности с эозинофилией и системными симптомами (DRESS-синдром), синдром Стивенса-Джонсона (ССД) или генерализованный эксфолиативный дерматит;
- пациенты с редко встречающейся наследственной непереносимостью галактозы, дефицитом лактазы или глюкозо-галактозной мальабсорбцией;
- детский возраст до 18 лет.
Применение при беременности и кормлении грудью
Не применять препарат в период беременности и грудного вскармливания.
Способ применения и дозы
Внутрь, с небольшим количеством воды.
Доза препарата определяется врачом индивидуально, в зависимости от состояния больного.
Обычно назначается по 1 капс. 3 раза в день или по 2 капс. 2 раза в день (150–200 мг/сут).
В случае пропуска приема препарата не следует удваивать дозу при следующем приеме.
Продолжительность лечения — от нескольких дней до 4–6 нед, в зависимости от состояния больного.
Побочные действия
Реклама: ООО «РЛС-Патент», ИНН 5044031277
Ниже перечислены нежелательные явления (НЯ), отмечавшиеся при приеме данного препарата, согласно классификации по системно-органным классам и частотам возникновения: редко — ≥1/10000 и <1/1000; очень редко — <1/10000; частота не установлена (по имеющимся данным невозможно определить частоту). Внутри каждой группы по частоте проявлений НЯ перечислены в порядке убывания частоты.
Нарушения со стороны нервной системы: редко — незначительная сонливость, появляющаяся в первые дни приема и обычно исчезающая самостоятельно в процессе лечения.
Нарушения со стороны кожи и подкожной клетчатки: редко — кожные реакции (макулопапулезные высыпания, многоформная эритема, зуд, отек лица); очень редко — аллергические реакции (крапивница, отек Квинке), тяжелые кожные реакции: DRESS-синдром, синдром Стивенса-Джонсона, генерализованный эксфолиативный дерматит; частота не установлена — анафилактический шок, лейкоцитокластический васкулит.
Нарушения со стороны печени и желчевыводящих путей: частота не установлена — гепатит, цитолитический гепатит.
Нарушения со стороны половых органов и молочной железы: очень редко — метроррагия у женщин, принимающих оральные контрацептивы.
Нарушения со стороны ЖКТ: очень редко — лимфоцитарный колит.
Взаимодействие
Потенцирует действие препаратов, угнетающих ЦНС, таких как опиоидные анальгетики, барбитураты, снотворные препараты, бензодиазепины, H1-антигистаминные средства, нейролептики, антидепрессанты с седативным эффектом, антигипертензивные средства центрального действия, баклофен, талидомид. Также усиливает воздействие алкоголя.
Передозировка
Симптомы: вялость, чрезмерная сонливость.
Лечение: при необходимости — симптоматическое лечение. Специфический антидот отсутствует.
Особые указания
Тяжелые кожные реакции
Очень редко при применении этифоксина наблюдались тяжелые кожные реакции, включая кожную сыпь в сочетании с эозинофилией и проявлениями DRESS-синдрома, синдром Стивенса-Джонсона и генерализованный эксфолиативный дерматит. Начало реакции со стороны кожи при применении препарата Стрезам® отмечали в период от нескольких дней до 1 мес, в зависимости от проявлений реакции. По данным наблюдений в постмаркетинговый период, после отмены этифоксина исход большинства кожных реакций, как правило, благоприятный. При применении этифоксина не наблюдалось летальных исходов, связанных с кожными реакциями. Пациентов следует информировать о рисках развития реакций со стороны кожи, а также о необходимости тщательного наблюдения за такими проявлениями. При выявлении токсической кожной реакции на этифоксин прием препарата следует прекратить и ни в коем случае не возобновлять.
Тяжелые реакции со стороны печени
В постмаркетинговый период при применении этифоксина очень редко наблюдались случаи цитолитического гепатита. По данным наблюдений в постмаркетинговый период, время возникновения реакций со стороны печени после применения этифоксина составляет от 2 недель до 1 месяца от начала лечения. В связи с риском реакций со стороны печени, требуется осторожность при применении этифоксина у пациентов пожилого возраста, в случае ранее перенесенного вирусного гепатита, а также при наличии других выявленных у пациента особых состояний, по мнению его лечащего врача. Нарушения со стороны печени могут не иметь клинических проявлений и обнаруживаются только при лабораторном исследовании. Пациентам с риском нарушения функции печени необходимо проводить контроль активности печеночных ферментов до начала лечения этифоксином и через месяц после окончания лечения. В случае выявления токсических нарушений функции печени прием препарата следует немедленно прекратить и ни в коем случае не возобновлять.
Лимфоцитарный колит
В постмаркетинговый период применения этифоксина отмечены отдельные случаи лимфоцитарного колита. При возникновении водянистой диареи у пациентов, получающих этифоксин, прием препарата следует немедленно прекратить и ни в коем случае не возобновлять. Обязательно проводят обследование пациента.
Метроррагия
В постмаркетинговый период применения этифоксина имели место случаи метроррагии у женщин, получающих оральные контрацептивы.
Взаимное усиление действия
Следует с особой осторожностью принимать препараты этифоксина гидрохлорида с препаратами, угнетающими ЦНС, из-за риска возможного взаимного усиления действия последних (см. «Взаимодействие»).
Влияние на способность управлять транспортными средствами и работать с механизмами. В связи с риском возникновения сонливости, следует во время лечения избегать управления автотранспортом и деятельности, требующей повышенного внимания, например управления различными механизмами.
Форма выпуска
Капсулы, 50 мг. По 12 капс. в блистере ПВХ/алюминий. По 2 блистера с инструкцией по применению помещают в пачку картонную или по 20 капс. в блистере ПВХ/алюминий, по 3 блистера с инструкцией по применению помещают в пачку картонную.
Возможно наличие контроля первого вскрытия.
Производитель
Biocodex, Франция 1 avenue Blaise Pascale, 60000 Beauvais.
Держатель регистрационного удостоверения. Biocodex, Франция 7, avenue Gallieni, 94250 Gentilly.
Организация, принимающая претензии потребителей: ООО «БИОКОДЕКС», 127051, Москва, б-р Цветной, д. 2.
Тел.: +7 (495) 783-26-80.
e-mail: phv@biocodex-corp.ru
www.biocodex.ru
Условия отпуска из аптек
По рецепту.
Условия хранения
При температуре 15–25 °C.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не применять по истечении срока годности, указанного на упаковке.
Описание проверено
-
Лобанова Елена Георгиевна
(фармаколог, доктор медицинских наук, профессор)
Опыт работы: более 30 лет
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
Стрезам® (Stresam) инструкция по применению
📜 Инструкция по применению Стрезам®
💊 Состав препарата Стрезам®
✅ Применение препарата Стрезам®
📅 Условия хранения Стрезам®
⏳ Срок годности Стрезам®
Препарат отпускается по рецепту
Температура хранения: от 15 до 25 °С

Описание лекарственного препарата
Стрезам®
(Stresam)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для электронного издания справочника Видаль 2025
года, дата обновления: 2024.12.20
Владелец регистрационного удостоверения:
Контакты для обращений:
БИОКОДЕКС ООО
(Россия)
Лекарственная форма
|
Препарат отпускается по рецепту |
Стрезам® |
Капсулы 50 мг: 24 или 60 шт. рег. №: ЛСР-005103/08 |
Форма выпуска, упаковка и состав
препарата Стрезам®
Капсулы желатиновые, размер №2, гладкие, блестящие, с белым корпусом и голубой крышечкой; содержимое капсул — порошок белого или белого с легким желтоватым оттенком цвета.
Вспомогательные вещества: лактозы моногидрат, тальк, целлюлоза микрокристаллическая, кремния диоксид коллоидный безводный, магния стеарат.
Состав оболочки капсулы: титана диоксид, желатин, индигокармин.
12 шт. — блистеры (2) — пачки картонные.
20 шт. — блистеры (3) — пачки картонные.
Возможно наличие контроля первого вскрытия.
Фармакологическое действие
Этифоксина гидрохлорид принадлежит к производным бензоксазина. Обладает анксиолитическим действием, в меньшей степени оказывает седативное действие. Не вызывает привыкания и синдрома отмены.
В исследованиях in vitro и in vivo у крыс и мышей было показано, что анксиолитическая активность этифоксина обусловлена двойным механизмом его действия (прямого и опосредованного) на ГАМК-А рецепторы, улучшающим ГАМК-ергическую передачу импульса.
При прямом воздействии на ГАМК-А-рецептор путем аллостерической модуляции этифоксин связывается преимущественно с субъединицами β2- или β3-рецептора; исследования показали, что этифоксин связывается с ГАМК-А-рецептором на участках, отличных от места связывания бензодиазепинов. Непрямое действие обеспечивается посредством увеличения синтеза нейростероидов (с помощью активации митохондриального белка-транслокатора), таких как аллопрегнанолон, также являющегося положительным аллостерическим модулятором ГАМК-А рецептора.
Фармакокинетика
Всасывание
После приема внутрь препарат быстро всасывается из ЖКТ. Время достижения Cmax в крови составляет 2-3 ч.
Распределение
Проникает через плацентарный барьер.
Метаболизм
Быстро метаболизируется в печени до образования нескольких метаболитов. Один из метаболитов — диэтилэтифоксин — является активным.
Выведение
T1/2 этифоксина составляет около 6 ч, T1/2 активного метаболита — 20 ч. Выводится преимущественно с мочой в виде метаболитов и в небольших количествах в неизмененном виде; также выводится с желчью.
Показания препарата
Стрезам®
- лечение тревоги и связанных с ней психосоматических расстройств.
Режим дозирования
Дозу и продолжительность курса лечения врач определяет индивидуально, в зависимости от состояния пациента.
Препарат назначают внутрь, как правило, по 50 мг (1 капс.) 3 раза/сут или по 100 мг (2 капс.) 2 раза/сут. Курс лечения обычно составляет от нескольких дней до 4-6 недель.
Капсулы запивают небольшим количеством воды.
Побочное действие
Определение частоты нежелательных явлений (НЯ), отмечавшиеся при приеме данного препарата: редко (≥1/10 000 и <1/1000), очень редко (< 1/10 000) в порядке убывания частоты.
Со стороны нервной системы: редко — незначительная сонливость, появляющаяся в первые дни приема и обычно исчезающая самостоятельно в процессе лечения.
Со стороны кожи и подкожной клетчатки: редко — макуло-папулезные высыпания, многоформная эритема, зуд, отек лица, тяжелые кожные реакции — DRESS-синдром, синдром Стивенса-Джонсона, генерализованный эксфолиативный дерматит.
Аллергические реакции: очень редко — крапивница, отек Квинке, частота не установлена — анафилактический шок, лейкоцитокластический васкулит.
Со стороны печени и желчевыводящих путей: очень редко — гепатит, цитолитический гепатит.
Со стороны половых органов и молочной железы: очень редко — метроррагия у женщин, принимающих пероральные контрацептивы.
Со стороны ЖКТ: очень редко — лимфоцитарный колит.
Противопоказания к применению
- повышенная чувствительность к активному веществу или к любому из вспомогательных веществ, входящих в состав препарата;
- шоковые состояния (угнетение ЦНС любой этиологии);
- миастения;
- тяжелая печеночная недостаточность;
- тяжелая почечная недостаточность;
- пациенты с тяжелыми формами гепатита или цитолизом печени на фоне предшествующего лечения этифоксином:
- пациенты, у которых во время предыдущего лечения этифоксином возникали серьезные кожные реакции, такие как синдром лекарственной гиперчувствительности с эозинофилией и системными симптомами (DRESS-синдром), синдром Стивенса-Джонсона (ССД) или генерализованный эксфолиативный дерматит;
- пациенты с редко встречающейся наследственной непереносимостью галактозы, дефицитом лактазы или глюкозо-галактозной мальабсорбцией;
- детский возраст до 18 лет.
Применение при беременности и кормлении грудью
Не применять препарат в период беременности и грудного вскармливания.
Применение при нарушениях функции печени
Применение препарата при тяжелых нарушениях функции печени противопоказано.
Применение при нарушениях функции почек
Применение препарата при тяжелых нарушениях функции почек противопоказано.
Применение у детей
Не рекомендуется использовать препарат у детей и подростков в возрасте до 18 лет.
Особые указания
Тяжелые кожные реакции
Очень редко при применении этифоксина наблюдались тяжелые кожные реакции, включая кожную сыпь в сочетании с эозинофилией и проявлениями DRESS-синдрома, синдром Стивенса-Джонсона и генерализованный эксфолиативный дерматит. Начало реакции со стороны кожи при применении препарата Стрезам® отмечали в период от нескольких дней до 1 месяца, в зависимости от проявлений реакции. По данным наблюдений в постмаркетинговый период, после отмены этифоксина исход большинства кожных реакций, как правило, благоприятный. При применении этифоксина не наблюдалось летальных исходов, связанных с кожными реакциями. Пациентов следует информировать о рисках развития реакций со стороны кожи, а также о необходимости тщательного наблюдения за такими проявлениями. При выявлении токсической кожной реакции на этифоксин. Прием препарата следует прекратить и ни в коем случае не возобновлять.
Тяжелые реакции со стороны печени
В постмаркетинговый период при применении этифоксина очень редко наблюдались случаи цитолитического гепатита. По данным наблюдений в постмаркетинговый период время возникновения реакций со стороны печени после применения этифоксина составляет от 2 недель до 1 месяца от начала лечения. В связи с риском реакций со стороны печени, требуется осторожность при применении этифоксина у пациентов пожилого возраста, в случае ранее перенесенного вирусного гепатита, а также при наличии других выявленных у пациента особых состояний, по мнению его лечащего врача. Нарушения со стороны печени могут не иметь клинических проявлений и обнаруживаются только при лабораторном исследовании. Пациентам с риском нарушения функции печени необходимо проводить контроль активности печеночных ферментов до начала лечения этифоксином и через месяц после окончания лечения. В случае выявления токсических нарушении функции печени прием препарата следует немедленно прекратить и ни в коем случае не возобновлять.
Лимфоцитарный колит
В постмаркетинговый период применения этифоксина отмечены отдельные случаи лимфоцитарного колита. При возникновении водянистой диареи у пациентов, получающих этифоксин, прием препарата следует немедленно прекратить и ни в коем случае не возобновлять. Обязательно проводят обследование пациента.
Метроррагия
В постмаркетинговый период применения этифоксина. Имели место случаи метроррагии у женщин, получающих пероральные контрацептивы.
Взаимное усиление действия
Следует с особой осторожностью принимать препараты этифоксина гидрохлорида с препаратами, угнетающими ЦНС, из-за риска возможного взаимного усиления действия последних (см. раздел «Лекарственное взаимодействие»).
Влияние на способность к управлению транспортными средствами и механизмами
В связи с риском возникновения сонливости, следует во время лечения избегать управления автотранспортом и деятельности, требующей повышенного внимания, например, управления различными механизмами.
Передозировка
Симптомы: вялость, чрезмерная сонливость.
Лечение: при необходимости проводится симптоматическая терапия. Специфический антидот отсутствует.
Лекарственное взаимодействие
Стрезам® потенцирует действие препаратов, угнетающих ЦНС, таких как: опиоидные анальгетики, барбитураты, снотворные препараты, бензодиазепины, блокаторы гистаминовых H1-рецепторов, нейролептики, антидепрессанты с седативным эффектом, антигипертензивные средства центрального действия, баклофен, талидомид.
Стрезам® усиливает воздействие этанола.
Условия хранения препарата Стрезам®
Препарат следует хранить в недоступном для детей месте при температуре от 15° до 25°С.
Срок годности препарата Стрезам®
Срок годности — 3 года.
Условия реализации
Препарат отпускают по рецепту.
БИОКОДЕКС ООО
(Россия)
|
127051 Москва, |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Синонимы, аналоги
Статьи
Пен-иньектор UnoPen GM-B1 представляет собой предварительно заполненную одноразовую шприц-ручку для многократных инъекций (далее «Шприц-ручка»), содержащую гипогликемическое средство, аналог глюкагоноподобного пептида-1 (ГПП-1) – семаглутид.
Семавик® (0,25 мг/доза, 0,5 мг/доза, 1 мг/доза) – раствор для п/к введения в предварительно заполненной шприц-ручке позволяет вводить дозы 0,25 мг, 0,5 мг и 1 мг. Шприц-ручка предназначена для титрации дозы 0,25 мг и поддержания терапевтической дозы 0,5 мг и 1 мг. Одна шприц-ручка содержит 3 мл раствора.
Инструкция по применению препарата Семавик®
Варианты использования шприц-ручки при введении препарата Семавик®:
Вариант 1 – титрация дозы
4 – инъекции по 0,25 мг
4 – инъекции по 0,5 мг
1 – инъекция по 1 мг
Вариант 2 – поддержание терапевтической дозы
4 – инъекции по 1 мг
Шприц-ручка предназначена для использования с одноразовыми инъекционными иглами WellFine, Dexfine и Verifine. В упаковку препарата Семавик® включены иглы WellFine 4 mm 32G (Dexfine 4 mm 32G или Verifine 4 mm 32G) в количестве 4 шт.
Препарат Семавик® можно вводить при помощи игл длиной до 8 мм.
Перед каждой инъекцией необходимо использовать новую иглу. После инъекции хранить и транспортировать шприц-ручку необходимо без иглы! Это предотвращает непроходимость игл, загрязнение, заражение, вытекание раствора и введение некорректной дозы препарата.
Утилизировать иглы необходимо согласно местным требованиям, соблюдая нормы и правила обращения с потенциально инфицированными материалами.
Применение шприц-ручки должно проводиться только одним человеком. Шприц-ручка не должна передаваться третьему лицу.
Если препарат Семавик® в шприц-ручке выглядит иначе, чем бесцветный прозрачный раствор, то его применять нельзя.
Не подвергайте ручки воздействию низких (ниже +2°С) и высоких (выше +30°С) температур. Не помещайте шприц-ручки в морозильную камеру. Шприц-ручки нельзя замораживать!
Использованные шприц-ручки подлежат утилизации и не должны повторно эксплуатироваться (нельзя повторно заполнять шприц-ручку).
Транспортировать шприц-ручки при высоких/низких температурах воздуха лучше в специальном термопенале/сумке (например, оригинальный термопенал ГЕРОФАРМ).
Храните шприц-ручку и иглы в недоступных для всех, и в особенности для детей, местах.
Не пытайтесь самостоятельно ремонтировать шприц-ручку. В случае поломки сообщите в организацию, принимающую претензии потребителей, указанную в инструкции по медицинскому применению препарата. Телефон информационной линии помощи ГЕРОФАРМ: 8 (800) 333-43-76.
Инструкция по применению предварительно заполненной шприц-ручки с препаратом Семавик® 0,25 мг/доза, 0,5 мг/доза, 1 мг/доза раствор для подкожного введения.
Перед первой инъекцией необходимо внимательно прочитать и изучить инструкцию по использованию предварительно заполненных одноразовых шприц-ручек UnoPen GM-B1.
Необходимо проконсультироваться с лечащим врачом (специалистом) по применению шприц-ручки. Попросите продемонстрировать правильное использование шприц-ручки. Первая инъекция препарата должна проводиться под контролем врача или медсестры.
Внимательно прочитайте этикетку на шприц-ручке и убедитесь в том, что Вы используете именно тот лекарственный препарат, который Вам назначил врач, в нужной Вам дозировке, а также проверьте срок годности препарата. Затем посмотрите на представленные ниже иллюстрации, чтобы ознакомиться с характеристиками и составными частями шприц-ручки.
Перед началом использования шприц-ручки необходимо исследовать ее на наличие видимых механических повреждений и подтеков (свидетельствующих о нарушении герметичности картриджа). Если Вы не уверены, что шприц-ручка исправна, и у нее отсутствуют повреждения, никогда не пользуйтесь шприц-ручкой. Всегда проверяйте шприц-ручку перед каждой инъекцией.
Тщательно следуйте инструкции по использованию шприц-ручки: предотвращайте падение ручки и влияние прочих внешних факторов (термальное воздействие, прямые солнечные лучи, механическое повреждение и пр.). Если произошло повреждение, необходимо начать использовать новую шприц-ручку.
Слабовидящий пациент или пациент, у которого имеются серьезные проблемы со зрением, и он не может различить цифры на счетчике дозы, должен использовать шприц-ручку под контролем медицинского персонала, родственников или человека с хорошим зрением, прошедших обучение по введению препарата предварительно заполненной шприц-ручкой.
Лица, осуществляющие уход за больным, должны обращаться с использованными иглами с особой осторожностью, чтобы предотвратить уколы иглой и перекрестное инфицирование.
Предварительно заполненная шприц-ручка UnoPen GM-B1 с препаратом Семавик®
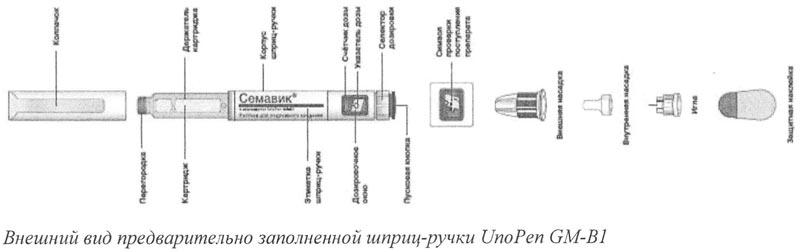
I. Подготовка шприц-ручки с новой иглой к использованию
1. Проверьте название на этикетке шприц-ручки. Необходимо убедиться, что в ручке содержится препарат Семавик® 0,25 мг/доза, 0,5 мг/доза, 1 мг/доза. Это особенно важно, если Вы применяете более одного инъекционного препарата.

2. Удерживайте шприц-ручку одной рукой и снимите колпачок со шприц-ручки, потянув за него другой рукой.
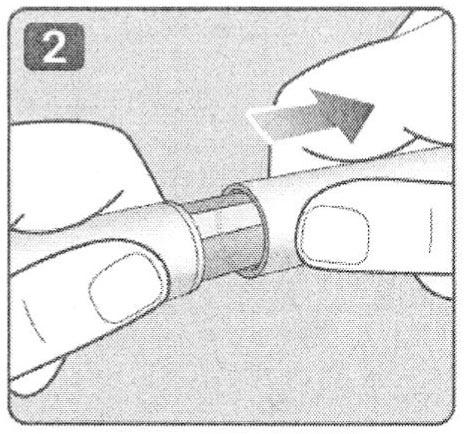
3. Убедитесь, что раствор в шприц-ручке бесцветный или почти бесцветный и прозрачный. Посмотрите в окошко держателя картриджа шприц-ручки.
Примечание: Если раствор мутный, не бесцветный или есть посторонние примеси, такую шприц-ручку использовать нельзя!
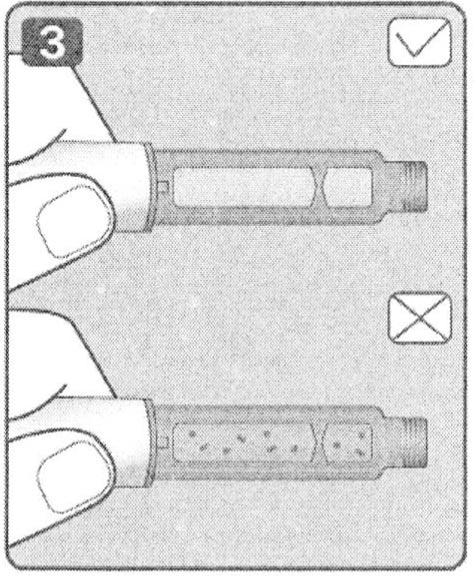
4. Возьмите новую иглу и удалите защитную наклейку с внешней насадки иглы.
Примечание: Используйте иглы строго в соответствии с рекомендациями врача. При каждой инъекции используйте новую иглу, чтобы свести к минимуму риск введения неправильной дозы препарата, инфицирования и травматизации тканей.
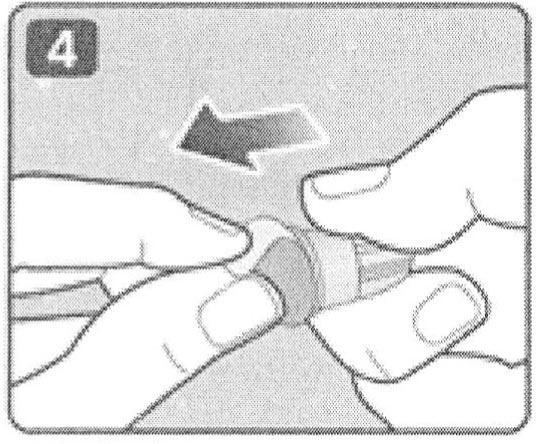
5. При помощи внешней насадки иглы установите ее точно на держатель картриджа. Надежно закрутите ее, чтобы игла плотно держалась на шприц-ручке.
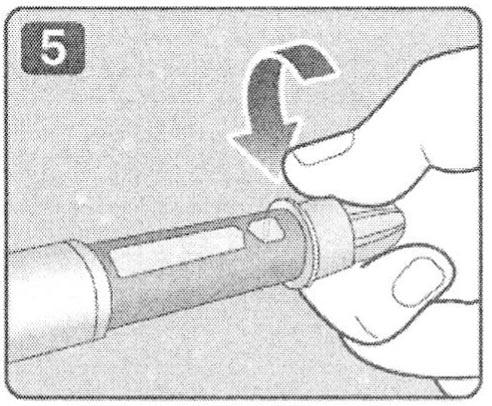
6. Снимите наружный колпачок иглы, но не выбрасывайте его. Он понадобится после завершения инъекции, чтобы безопасно снять иглу со шприц-ручки.
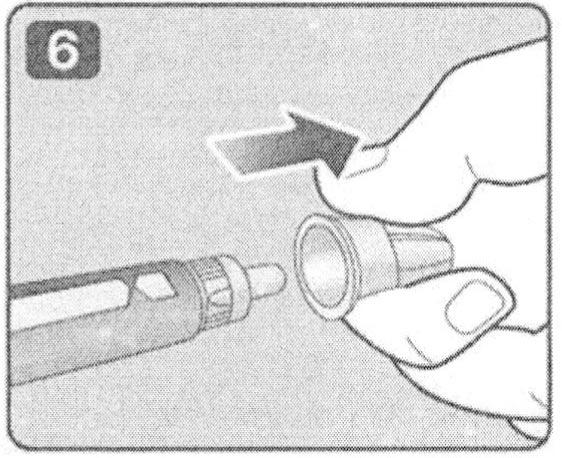
7. Снимите Внутреннюю насадку и выбросите. Удерживайте шприц-ручку иглой вверх. Слегка постучите пальцем по держателю картриджа, чтобы пузырьки воздуха поднялись вверх. Наличие мелкодисперсных пузырьков допустимо.
Примечание: Игла становится видимой (обнажается) по мере удаления внутренней насадки.
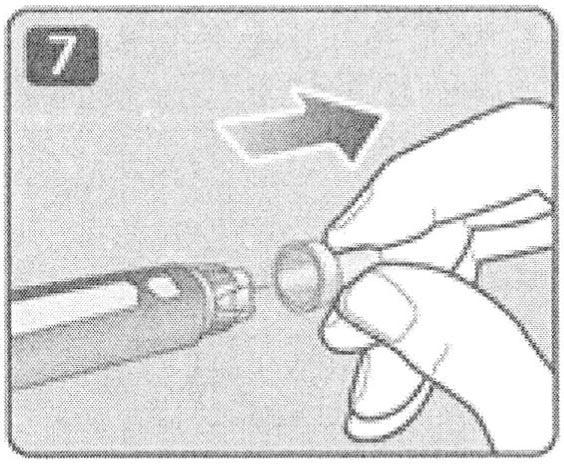
При установке иглы на держатель картриджа может появиться капля препарата, это нормальное явление, однако все равно необходимо проверить прохождение (поступление) препарата через иглу, если шприц-ручка используется в первый раз. Присоединяйте новую иглу к шприц-ручке непосредственно перед инъекцией, когда пациент будет готов к введению препарата.
II. Проверка прохождения (поступления) препарата через иглу
8. Перед первым применением шприц-ручки необходимо проверить прохождение (поступление) препарата через иглу.
Прокрутите селектор дозировки до символа проверки прохождения (поступления) препарата таким образом, чтобы символ совпадал с указателем дозы. При наборе символа проверки вы должны услышать 2 (два) щелчка.
Примечание: Если селектор дозировки проскочил необходимый символ, прокрутите его в противоположном направлении для того, чтобы скорректировать положение символа проверки. Если шприц-ручка уже находится в использовании, то начинайте использование с пункта «Установка дозы».
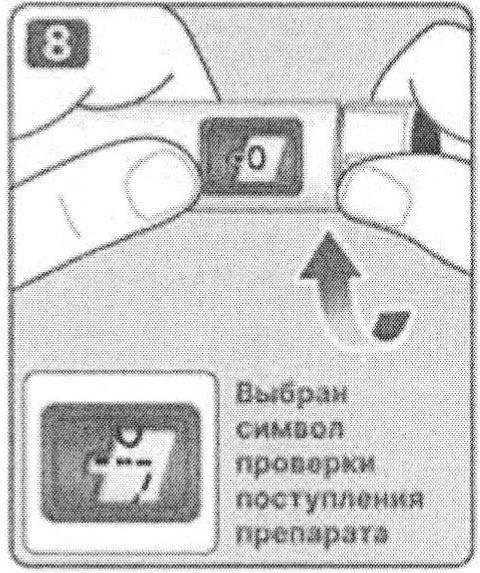
9. Удерживая шприц-ручку иглой вверх, нажимайте на пусковую кнопку и удерживайте ее в этом положении, селектор дозировки издаст щелчок, в дозировочном окне появится значение ноль «0». На конце иглы должна появиться 1 (2) капля препарата.
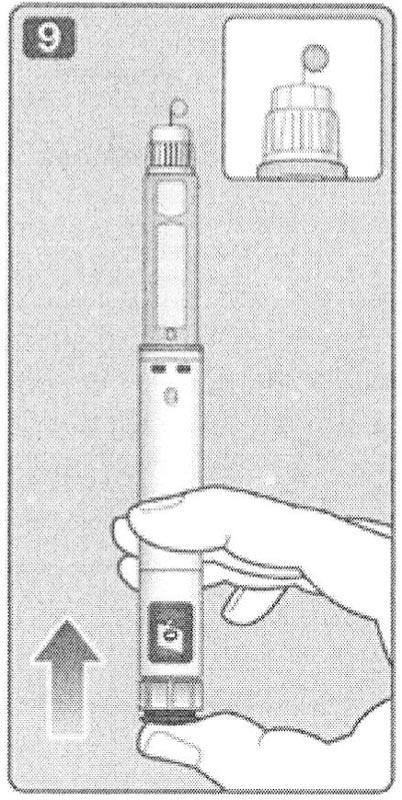
Если после проверки прохождения (поступления) препарата капля не появилась на конце иглы, необходимо повторить действия пункта «II», но не более 6 раз. Если капля препарата так и не появилась, необходимо заменить иглу и повторить действия пункта «II» Проверка прохождения (поступления) препарата через иглу» еще раз. Если капля раствора так и не появилась, необходимо утилизировать шприц-ручку и использовать новую.
Перед использованием шприц-ручки в первый раз следует быть уверенным в том, что игла хорошо пропускает препарат, а на конце иглы появилась капля раствора. Это гарантирует введение препарата. Если игла повреждена или закупорена, капля раствора не появится, препарат не будет введен, даже если селектор дозировки и счетчик дозы будут двигаться. Пациент может не ввести необходимую дозу, и эффект препарата Семавик® не будет достигнут. Необходимо обязательно проверять прохождение препарата через иглу перед первой инъекцией.
III. Установка дозы
Перед каждой инъекцией необходимо проверять какую дозу препарата (мг) пациент набрал по счетчику дозы и указателю дозы. Не ориентируйтесь на щелчки шприц-ручки, не следует их считать.
На шприц-ручке можно выбирать дозы 0,25 мг, 0,5 мг или 1 мг. Выбор осуществляется селектором дозы. При правильном наборе дозы счетчик дозы и указатель дозы покажут количество мг препарата в выбранной пациентом дозе.
Пациент может выбрать до 1 мг препарата на дозу. Если в шприц-ручке содержится менее 1 мг, счетчик дозы остановится прежде, чем появится «1».
10. Поворачивайте селектор дозы до тех пор, пока он не покажет необходимую дозу 0,25 мг, 0,5 мг или 1 мг. Выбранная доза должна находиться точно напротив указателя дозы.
Примечание: Если доза была выбрана неправильно, поворотным движением селектора дозы вперед или назад, установите правильную дозу.
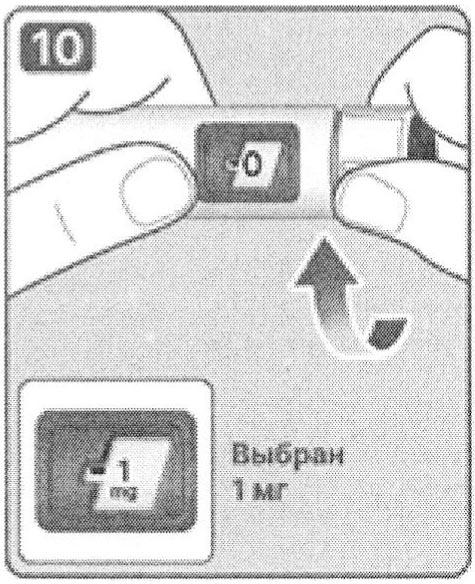
11. Для определения остаточного количества препарата, необходимо использовать счетчик дозы: поворачивая селектор дозы до остановки счетчика дозы. Если в дозировочном окне он показывает «1», в шприц-ручке осталось не менее 1 мг препарата. Если счетчик дозы остановился до того, как появилось «1», то это означает, что в шприц-ручке осталось недостаточное количество препарата, чтобы ввести полную дозу 1 мг.

Важно! Не используйте шприц-ручку, если осталось недостаточное количество препарата для введения полной дозы. Используйте новую шприц-ручку.
IV. Введение препарата
12. Одним непрерывным движением руки введите иглу под кожу.
Примечание: Используйте техники инъекций, рекомендованные врачом или средним медицинским персоналом.
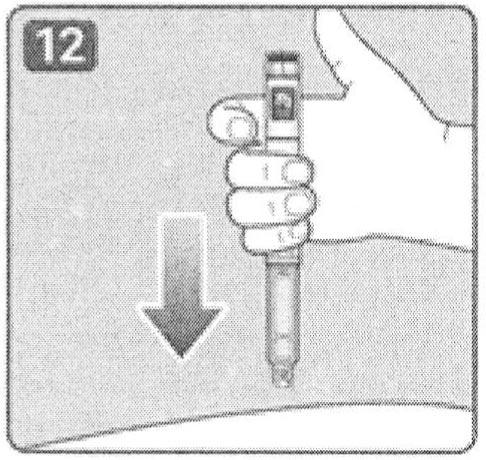
13. Убедитесь, что дозировочное окно находится в поле зрения человека, проводящего инъекцию.
Нажмите на пусковую кнопку и удерживайте ее, пока значение «0» не совпадет с указателем дозы. При нажатии на кнопку пациент может услышать или ощутить щелчок.
Нельзя дотрагиваться пальцами до счетчика дозы в дозировочном окне – это может прервать инъекцию.
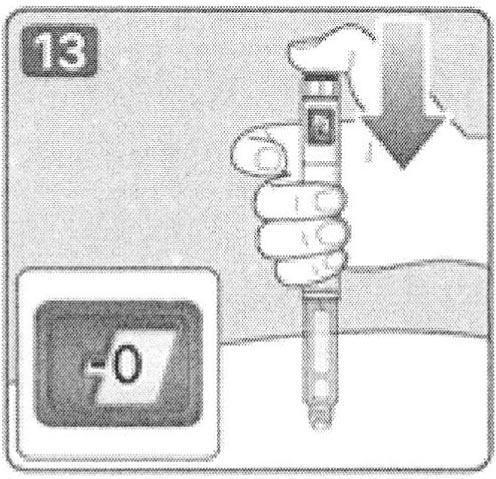
14. Удерживайте иглу под кожей, после того, как счетчик дозы вернулся к «0» и медленно считайте до 6.
Примечание: Если извлечь иглу из-под кожи раньше, пациент может увидеть, как препарат вытекает из иглы. В этом случае будет введена неполная доза препарата.
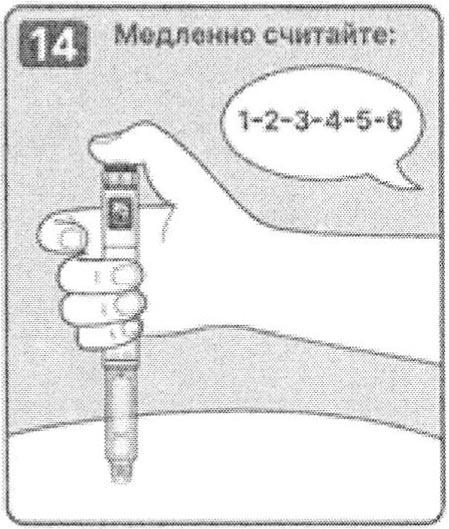
15. Осторожно извлеките иглу из-под кожи.
Примечание: Если в месте инъекции появилась кровь, необходимо слегка прижать к месту укола ватный тампон.
Не следует массировать место укола.
После завершения инъекции пациент может увидеть каплю раствора на конце иглы. Это нормально и не влияет на дозу препарата, которая введена.
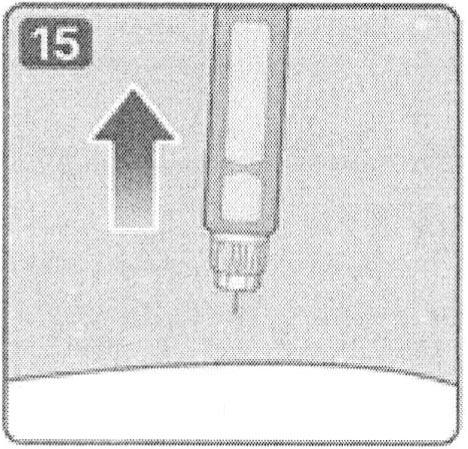
V. Утилизация иглы
Важно! После каждой инъекции препарата всегда удаляйте иглу со шприц-ручки. Это может предотвратить закупорку игл, загрязнение, инфицирование, вытекание раствора и введение неправильной дозы препарата.
Хранить и транспортировать шприц-ручку необходимо без иглы!
16. После завершения инъекции осторожно наденьте внешнюю насадку на иглу до упора.
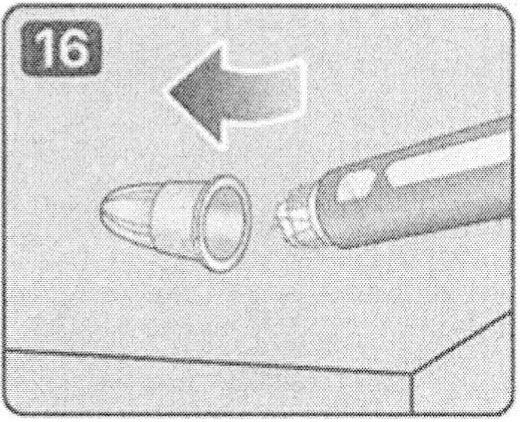
17. Открутите иглу и выбросите ее вместе с внешней насадкой, соблюдая меры предосторожности.
Примечание: При утилизации использованных игл соблюдайте местные требования, нормы и правила обращения с потенциально инфицированными материалами.

18. Наденьте колпачок шприц-ручки и храните шприц-ручку до следующего использования согласно условиям хранения, указанным в инструкции по применению препарата.
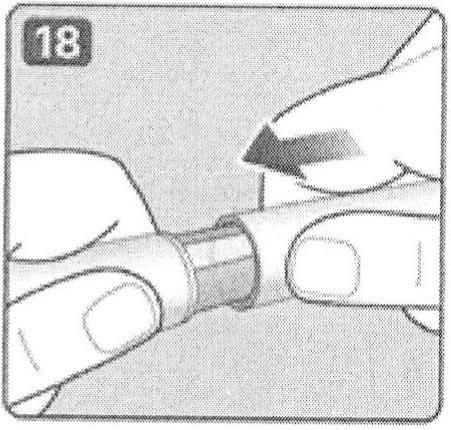
VI. Уход за шприц-ручкой
Со шприц-ручкой следует обращаться аккуратно. Небрежное или неправильное обращение может стать причиной неправильной дозировки препарат Семавик®, что может привести к слишком высокой или слишком низкой концентрации глюкозы крови или вызвать дискомфорт в области живота (тошнота или рвота).
Необходимо предохранять шприц-ручку от попадания пыли, загрязнений и жидкости. Запрещается мыть шприц-ручку, погружать ее в жидкости. По мере загрязнения шприц-ручку можно протирать влажной тканью, смоченной мягким моющим средством.
Если шприц-ручка подверглась физическому воздействию (удар, механическая вибрация, термические явления и пр.) или пациент сомневается в ее исправности, необходимо присоединить новую иглу и проверить прохождение (поступление) препарата перед тем, как сделать инъекцию.
Запрещается оставлять шприц-ручку в местах, где она может подвергаться воздействию слишком высоких или слишком низких температур (в автомобиле, на подоконнике и пр.). Запрещается проводить инъекцию препарат Семавик®, если он был заморожен.
Использованную (пустую) шприц-ручку необходимо выбросить. Выбрасывать пустую шприц-ручку с отсоединенной иглой необходимо в соответствии с рекомендациями, данными врачом, медсестрой, фармацевтом или местными требованиями.
Купить Предварительно заполненная шприц-ручка UnoPen GM-B1 для введения препарата Семавик в apteka.ru
Купить Предварительно заполненная шприц-ручка UnoPen GM-B1 для введения препарата Семавик в ГорЗдрав
Купить Предварительно заполненная шприц-ручка UnoPen GM-B1 для введения препарата Семавик в megapteka.ru
Купить Предварительно заполненная шприц-ручка UnoPen GM-B1 для введения препарата Семавик в Планета Здоровья
*Цены в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Показания
Лечение тревоги и связанных с ней психосоматических расстройств.
Противопоказания
Повышенная чувствительность к действующему веществу или к любому из вспомогательных веществ; шоковые состояния (угнетение центральной нервной системы (ЦПС) любой этиологии); тяжелая печеночная и/или почечная недостаточность; миастения; пациенты с тяжелыми формами гепатита или цитолизом печени на фоне предшествующего лечения этифоксином; пациенты, у которых во время предыдущего лечения этифоксином возникали серьезные кожные реакции, такие как синдром лекарственной гиперчувствительности с эозинофилией и системными симптомами (DRESS синдром), синдром Стивенса-Джонсона (ССД) или генерализованный эксфолиативный дерматит; пациенты с редко встречающейся наследственной непереносимостью галактозы, дефицитом лактазы или глюкозо-галактозной мальабсорбцией; детский возраст до 18 лет.
Беременность и лактация
Не применять препарат в период беременности и грудного вскармливания.
Рекомендации по применению
Внутрь, с небольшим количеством воды.
Доза препарата определяется врачом, индивидуально, в зависимости от состояния больного.
Обычно назначается по 1 капсуле 3 раза в день, или по 2 капсулы 2 раза в день (150 — 200 мг/сут).
В случае пропуска приёма препарата не следует удваивать дозу при следующем приеме. Продолжительность лечения — от нескольких дней до 4-6 недель, в зависимости от состояния больного.
Инструкция по использованию
—
Побочные эффекты
Ниже перечислены нежелательные явления (НЯ), отмечавшиеся при приеме данного препарата, согласно классификации по системно-органным классам и частоте возникновения («редко»: ≥1/10 000 и <1/1000, «очень редко»: <1/10 000) внутри каждой группы по частоте проявлений НЯ перечислены в порядке убывания частоты.
Нарушения со стороны нервной системы
Редко: незначительная сонливость, появляющаяся в первые дни приема и обычно исчезающая самостоятельно в процессе лечения.
Нарушения со стороны кожи и подкожной клетчатки
Редко: кожные реакции: макулопапулезные высыпания, многоформная эритема, зуд, отёк лица.
Очень редко: аллергические реакции: крапивница, отек Квинке; тяжелые кожные реакции: DRESS-синдром, синдром Стивенса-Джонсона, генерализованный эксфолиативный дерматит.
Частота не установлена: анафилактический шок, лейкоцитокластический васкулит.
Нарушения со стороны печени и желчевыводящих путей
Очень редко: гепатит, цитолитический гепатит.
Нарушения со стороны половых органов и молочной железы
Очень редко: метроррагия у женщин, принимающих оральные контрацептивы.
Нарушения со стороны желудочно-кишечного тракта
Очень редко: лимфоцитарный колит.
Передозировка
Симптомы: вялость, чрезмерная сонливость.
Лечение: при необходимости оказывают симптоматическое лечение. Специфический антидот отсутствует.
Взаимодействия
Потенцирует действие препаратов, угнетающих ЦНС, таких как: опиоидные анальгетики, барбитураты, снотворные препараты, бензодиазепины, Н1-антигистаминные средства, нейролептики, антидепрессанты с седативным эффектом, антигипертензивные средства центрального действия, баклофен, талидомид. Также усиливает воздействие алкоголя.
Особые указания
Тяжелые кожные реакции
Очень редко при применении этифоксина наблюдались тяжелые кожные реакции, включая кожную сыпь в сочетании с эозинофилией и проявлениями DRESS-синдрома, синдром Стивенса-Джонсона и генерализованный эксфолиативный дерматит. Начало реакции со стороны кожи при применении препарата Стрезам отмечали в период от нескольких дней до 1 месяца, в зависимости от проявлений реакции. По данным наблюдений в постмаркетинговый период, после отмены этифоксина исход большинства кожных реакций, как правило, благоприятный. При применении этифоксина не наблюдалось летальных исходов, связанных с кожными реакциями. Пациентов следует информировать о рисках развития реакций со стороны кожи, а также о необходимости тщательного наблюдения за такими проявлениями. При выявлении токсической кожной реакции на этифоксин Приём препарата следует прекратить и ни в коем случае не возобновлять.
Тяжелые реакции со стороны печени
В постмаркетинговый период при применении этифоксина очень редко наблюдались случаи цитолитического гепатита. По данным наблюдений в постмаркетинговый период время возникновения реакций со стороны печени после применения этифоксина составляет от 2 недель до 1 месяца от начала лечения. В связи с риском реакций со стороны печени, требуется осторожность при применении этифоксина у пациентов пожилого возраста, в случае ранее перенесенного вирусного гепатита, а также при наличии других выявленных у пациента особых состояний, по мнению его лечащего врача. Нарушения со стороны печени могут не иметь клинических проявлений и обнаруживаются только при лабораторном исследовании. Пациентам с риском нарушения функции печени необходимо проводить контроль активности печеночных ферментов до начала лечения этифоксином и через месяц после окончания лечения. В случае выявления токсических нарушений функций печени прием препарата следует немедленно прекратить и ни в коем случае не возобновлять.
Лимфоцитарный колит
В постмаркетинговый период применения этифоксина отмечены отдельные случаи лимфоцитарного колита. При возникновении водянистой диареи у пациентов, получающих этифоксин, приём препарата следует немедленно прекратить и ни в коем случае не возобновлять. Обязательно проводят обследование пациента.
Метроррагия
В постмаркетинговый период применения этифоксина имели место случаи метроррагии у женщин, получающих оральные контрацептивы.
Взаимное усиление действия
Следует с особой осторожностью принимать препараты этифоксина гидрохлорида с препаратами, угнетающими ЦНС, из-за риска возможного взаимного усиления действия последних (см. раздел «Взаимодействие с другими лекарственными средствами»).
Влияние на способность управлять трансп. ср. и мех.
В связи с риском возникновения сонливости, следует во время лечения избегать управления автотранспортом и деятельности, требующей повышенного внимания, например, управления различными механизмами.
Упаковка
По 12 капсул в блистеры ПВХ/алюминий, по 2 блистера с инструкцией по применению в пачки картонные; или по 20 капсул в блистеры ПВХ/алюминий, по 3 блистера с инструкцией по применению в пачки картонные.
Возможно наличие контроля первого вскрытия.
Условия хранения
Хранить при температуре от 15 °С до 25 °С.
Хранить в недоступном для детей месте!
Условия транспортирования
—
Срок годности
3 года.
Не использовать после истечения срока годности.
Условия отпуска
По рецепту
Стрезам®
МНН: Этифоксин
Производитель: Биокодекс
Анатомо-терапевтическо-химическая классификация: Etifoxine
Номер регистрации в РК:
№ РК-ЛС-5№009901
Информация о регистрации в РК:
26.09.2017 — 26.09.2022
Номер регистрации в РБ:
8949/09/14/18/19
Информация о регистрации в РБ:
11.10.2019 — бессрочно
- русский
- қазақша
- Скачать инструкцию медикамента
Торговое название
Стрезам®
Международное непатентованное название
Этифоксин
Лекарственная форма
Капсулы 50 мг
Состав
Одна капсула содержит
активное вещество
– этифоксина гидрохлорид 50 мг,
вспомогательные вещества:
лактозы моногидрат, тальк очищенный, целлюлоза микрокристаллическая,
кремния диоксид коллоидный, магния стеарат,
cостав
капсулы — индигокармин
(Е132), титана диоксид (Е171), желатин, вода очищенная,
крышечка- титана диоксид (Е
171), вода очищенная, желатин.
Описание
Твердая
желатиновая капсула размера «2» с корпусом белого цвета и
крышечкой голубого цвета. Содержимое капсулы порошок белого цвета.
Фармакотерапевтическая группа
Препараты для лечения
заболеваний нервной системы.
Анксиолитики другие
Код АТС N05ВХ03
Фармакологические свойства
Фармакокинетика
Этифоксина гидрохлорид хорошо
всасывается в желудочно-кишечном тракте. Быстро метаболизируется в
печени. Средняя максимальная концентрация этифоксина гидрохлорида и
его активного метаболита диэтилэтифоксина в крови достигается через
1-2 часа, проникает через плацентарный барьер. Начальные уровни
этифоксина гидрохлорида и активного метаболита в крови постепенно
уменьшаются на протяжении первых 2-х часов и 20 часов соответственно.
Период полувыведения этифоксина – 6 ч. Период полувыведения
диэтилэтифоксина 20 часов. Препарат и его основной метаболит
выводятся почками и кишечником.
Фармакодинамика
В терапевтических дозах
этифоксина гидрохлорид обладает анксиолитическим действием.
Производное бензоксазина, обладает анксиолитической активностью в
меньшей степени оказывает седативное действие. Избирательно действует
на хлорные каналы супрамолекулярного ГАМК-бензодиазепинхлорионофор
рецепторного комплекса, ингибируя ГАМК-ергическую передачу
Показания к применению
— неврастенические состояния,
связанные со стрессовыми расстройствами, которые сопровождаются
тревогой, страхом и беспокойством
— тревожно —
фобические расстройства
— вегетативные расстройства с
умеренно выраженным страхом, апатией, пониженной активностью.
Способ применения и дозы
Дозу и длительность курса
лечения врач определяет индивидуально, в зависимости от тяжести
заболевания. Взрослым назначают по 1 капсуле до еды по 2 – 3
раза в сутки. Максимальный курс лечения составляет 6 недель.
Побочные действия
иногда
— легкая сонливость
редко
— кожная сыпь, отек Квинке
очень редко
крапивница, ангиодерматит
Противопоказания
— повышенная чувствительность
к компонентам препарата
— шоковое состояние
— миастения
— тяжелые нарушения функции
печени, почек
— период беременности и
лактации
— десткий возрат до 18 лет
— одновременный прием этанола
Лекарственные взаимодействия
При одновременном применении
Стрезама®
с лекарственными средствами, которые угнетают действие центральной
нервной системы (нейролептики, транквилизаторы, антидепрессанты,
антигистаминные, барбитураты, анальгетики, седативные), усиливает их
действия. Усиливает действия этанола.
Особые указания
В состав препарата входит
лактоза, поэтому не рекомендуется назначать больным с врожденной
галактоземией, с синдромом мальабсорбции глюкозы и галактозы или с
дефицитом лактозы.
Не рекомендуется употребление
алкоголя и применения других веществ центрального действия (
галоперидол, диазепам, имипрамин и т.д. ) во время лечения
Стрезамом®.
В случае прекращения лечения
Стрезамом®,
у пациентов не возникает синдрома отмены.
Особенности влияния
лекарственного средства на способность управлять транспортным
средством или потенциально опасными механизмами:
В период лечения необходимо
воздержаться от управления автотранспортом и потенциально опасными
механизмами.
Передозировка
Симптомы:
вялость, чрезмерная
сонливость.
Лечение:
промывание желудка, в случае необходимости – симптоматическое
лечение. Специфического антидота не существует.
Форма выпуска и упаковка
По
20 капсул в контурной ячейковой упаковке из ПВХ и алюминиевой фольги.
По 3 контурной ячейковой
упаковке вместе с инструкцией по медицинскому применению на
государственном и русском языках помещают в картонную пачку
Условия хранения
Хранить в защищенном от света
месте, при температуре не выше 25 оС.
Хранить в недоступном для
детей месте!
Срок хранения
3 года
Не применять препарат после
истечения срока годности, указанного на упаковке.
Условия отпуска из аптек
По рецепту
Производитель
Биокодекс,
7
Авеню Гальени, 94250 Жантилли- Франция
FRA
250
Владелец регистрационного удостоверения
«Брюфармэкспорт
с.п.р.л.», Бельгия
Адрес организации,
принимающей на территории Республики Казахстан претензии от
потребителей по качеству продукции (товара)
РК, г. Алматы, ул. Богенбай
Батыра, 142 офис 724
Номер телефона 8 (727) 250 72
70
Номер факса 8 (727) 250 72 70
Адрес
электронной почты alma02@mail.ru,
bruphbe@brupharm.skynet.be
| Стрезам.doc | 0.04 кб |
| стрезам_капс_каз.doc | 0.05 кб |
Отправить прикрепленные файлы на почту
Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники «Центр экспертиз и испытаний в здравоохранении» МЗ РБ
