Описание препарата Церезим® (лиофилизат для приготовления раствора для инфузий, 200 ЕД) основано на официальной инструкции, утверждено компанией-производителем в 2012 году
Дата согласования: 31.08.2012
Содержание
- Действующее вещество
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав
- Описание лекарственной формы
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Производитель
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Аналоги (синонимы) препарата Церезим®
Действующее вещество
ATX
Фармакологическая группа
Состав
| Лиофилизат для приготовления раствора для инфузий | 1 фл. |
| активное вещество: | |
| имиглюцераза* | 200 ЕД** |
| 400 ЕД** | |
| * модифицированная форма глюкоцереброзидазы, продуцируемая клетками яичников китайских хомячков с помощью рекомбинантной ДНК-технологии | |
| ** ЕД обозначает количество фермента, которое катализирует гидролиз 1 мкмоля синтетического субстрата п-нитрофенил-?-D-глюкопиранозида (pNP-Glc) за 1 мин при температуре 37 °C | |
| вспомогательные вещества: маннитол; натрия цитрата дигидрат; лимонной кислоты моногидрат; полисорбат 80 |
Описание лекарственной формы
Лиофилизированный порошок или лиофилизат белого или почти белого цвета.
Восстановленный раствор: прозрачная бесцветная жидкость без посторонних включений.
Фармакодинамика
Имиглюцераза (рекомбинантная макрофаг-нацеленная β-глюкоцереброзидаза) катализирует гидролиз глюколипида глюкоцереброзида до глюкозы и церамида путем нормальной деградации мембранных липидов.
В основном, глюкоцереброзид образуется в результате гематопоэтического обмена клеток. Болезнь Гоше характеризуется функциональной недостаточностью ферментной активности β-глюкоцереброзидазы, что приводит к накоплению липида глюкоцереброзида в тканевых макрофагах, которые переполняются этим липидом и носят название «клетки Гоше». Клетки Гоше обычно обнаруживаются в печени, селезенке и костном мозге и иногда также в легких, почках и кишечнике. Ко вторичным гематологическим проявлениям заболевания относятся тяжелая анемия и тромбоцитопения в сочетании с характерной для болезни Гоше прогрессирующей гепатоспленомегалией. Наиболее распространенными и, зачастую, наиболее истощающими и инвалидизирующими последствиями болезни Гоше являются скелетные осложнения. К возможным скелетным осложнениям относятся остеонекроз, остеопения с вторичными патологическими переломами, недостаточность ремоделирования, остеосклероз и костные кризы.
Контролируемых клинических исследований эффективности препарата в отношении неврологических проявлений заболевания не проводилось. Поэтому заключений об эффектах ферментозаместительной терапии в отношении неврологических проявлений заболевания не имеется.
Фармакокинетика
В результате в/в инфузий 4 доз имиглюцеразы (7,5; 15, 30, 60 ЕД/кг) в течение 1 ч устойчивая ферментная активность достигалась к 30-й мин. После инфузии ферментная активность в плазме быстро снижалась с T1/2 от 3,6 до 10,4 мин. Плазменный Cl варьировал от 9,8 до 20,3 мл/мин/кг (среднее значение ± стандартное отклонение — 14,5±4,0 мл/мин/кг). Vss в пересчете на вес пациента, колебался от 0,09 до 0,15 л/кг (среднее значение ± стандартное отклонение — 0,12±0,02 л/кг). Вероятно, эти показатели не зависят от дозы или продолжительности инфузии, однако каждую дозу и скорость инфузии изучали только у 1 или 2 пациентов.
Показания
Длительная ферментозаместительная терапия у пациентов с подтвержденным диагнозом болезни Гоше первого типа (без нейронопатических проявлений) или третьего типа (с хроническими нейронопатическими проявлениями), у которых имеются клинически значимые не неврологические проявления данного заболевания. К не неврологическим проявлениям болезни Гоше относятся один или более из следующих симптомов:
— анемия (после исключения других причин, таких как дефицит железа);
— тромбоцитопения;
— костные заболевания (после исключения других причин, таких как дефицит витамина D);
— гепатомегалия или спленомегалия.
Противопоказания
Повышенная чувствительность к активному ингредиенту или другим компонентам препарата.
С осторожностью: при введении препарата пациентам, у которых наблюдается образование антител или развитие симптомов повышенной чувствительности к Цередазе (альглюцеразе).
Применение при беременности и кормлении грудью
Достаточных данных о применении имиглюцеразы у беременных женщин нет. Церезим® не должен применяться у беременных женщин, кроме случаев явной необходимости (при четких показаниях и анализе соотношения польза/риск для матери и плода).
Неизвестно, выделяется ли имиглюцераза с молоком, поэтому при применении препарата у кормящих матерей следует соблюдать осторожность.
Способ применения и дозы
В/в, в виде инфузии.
Каждый флакон препарата предназначен только для однократного применения.
После восстановления и разведения (см. «Инструкцию по восстановлению и разведению препарата») препарат вводят путем в/в инфузий в течение 1–2 ч. Альтернативно можно вводить подходящую дозу со скоростью, не превышающей 1 ЕД/кг/мин.
Вследствие гетерогенности и мультисистемной природы болезни Гоше режим дозирования должен быть индивидуальным для каждого пациента и основываться на всесторонней оценке клинических проявлений заболевания.
Различные режимы дозирования продемонстрировали эффективность в отношении некоторых или всех неневрологических проявлений заболевания. Применение начальных доз 60 ЕД/кг однократно каждые 2 нед продемонстрировало улучшение гематологических и висцеральных параметров в течение 6 мес терапии, а продолжение лечения приводило к приостановлению прогрессирования или уменьшало выраженность костных поражений.
Применение доз ниже 2,5 ЕД/кг 3 раза в неделю или однократное введение 15 ЕД/кг каждые 2 нед продемонстрировало улучшение гематологических показателей и органомегалии, но не влияло на параметры костной системы.
Обычно используемая и наиболее удобная для пациента частота проведения инфузий составляет 1 раз в 2 нед; большинство данных представлено именно в отношении этой частоты проведения инфузий.
Необходимо регулярно оценивать реакцию пациента на лечение и корректировать применяемые дозы (увеличивать или снижать) на основании всесторонней оценки реакции пациента в отношении всех клинических проявлений заболевания. Только после четкого определения и стабилизации индивидуальной реакции пациента на лечение (в отношении всех соответствующих клинических проявлений заболевания) может быть проведена коррекция дозы для продолжения эффективного лечения, при условии продолжения тщательного наблюдения за реакцией пациента на лечение и общим состоянием его здоровья. Обычно интервалы между контрольными обследованиями пациента составляют от 6 до 12 мес.
Исследований эффективности препарата в отношении неврологических симптомов у пациентов с хроническими нейронопатическими проявлениями болезни Гоше не проводилось, поэтому специальный режим дозирования для лечения этих проявлений не установлен.
Инструкция по восстановлению и разведению препарата
Лиофилизат восстанавливают водой для инъекций с последующим разведением с помощью 0,9 % раствора натрия хлорида для в/в инъекций и затем вводят путем в/в инфузии. На основании индивидуального для больного режима дозирования необходимо определить число флаконов, содержимое которых должно быть восстановлено, и достать их из холодильника. В некоторых случаях допускается небольшое изменение дозы во избежание неполного использования содержимого флаконов. Дозы могут округляться до наиболее близкой величины, соответствующей числу полных флаконов, но так, чтобы ежемесячно вводимая доза существенно не изменялась.
Восстановление и разведение препарата должны проводиться в асептических условиях.
Восстановление
Содержимое каждого флакона восстанавливают добавлением 5,1 мл (для дозировки 200 ЕД) или 10,2 мл (для дозировки 400 ЕД) воды для инъекций, избегая введения воды для инъекций сильной струей, после чего осторожно перемешивают раствор, не допуская образования пены. Объем восстановленного раствора составляет 5,3 мл (для дозировки 200 ЕД) или 10,6 мл (для дозировки 400 ЕД), а рН восстановленного раствора — приблизительно 6,1. Восстановленный раствор должен быть прозрачным, бесцветным и не должен содержать посторонних частиц. После восстановления необходимо сразу же развести содержимое флаконов. Перед разведением необходимо провести визуальный осмотр восстановленного раствора на наличие посторонних частиц и изменение цвета. Не использовать флаконы при наличии в полученном растворе посторонних частиц или при изменении цвета раствора!
Разведение
Восстановленный раствор содержит 40 ЕД имиглюцеразы в 1 мл (200 ЕД/5 мл или 400 ЕД/10 мл). Извлекаемый объем восстановленного раствора из каждого флакона составляет 5,0 мл (для дозировки 200 ЕД) или 10,0 мл (для дозировки 400 ЕД). В зависимости от предписанной дозы, извлеченные объемы восстановленного раствора из нескольких флаконов соответствующей дозировки объединяют и разводят 0,9% раствором хлорида натрия для в/в инъекций до общего объема 100–200 мл. Полученный раствор осторожно перемешивают.
Побочные действия
Реклама: ООО «РЛС-Патент», ИНН 5044031277
Ниже представлены нежелательные реакции, классифицированные по системам органов и частоте возникновения (часто — от ?1/100 до <1/10 и редко — от ?1/1000 до <1/100). В каждой группе нежелательные реакции перечислены в порядке уменьшения степени их выраженности.
| Со стороны ЦНС и периферической нервной системы | Редко — головокружение, головная боль, парестезия |
| Со стороны сердца | Редко — тахикардия, цианоз |
| Со стороны сосудистой системы | Редко — приливы, гипотензия |
| Со стороны дыхательной системы | Часто — респираторные симптомы |
| Со стороны ЖКТ | Редко — рвота, тошнота, спастические боли в животе, диарея |
| Со стороны кожи и подкожной клетчатки | Часто — крапивница/ангионевротический отек, зуд, сыпь |
| Со стороны скелетно-мышечной системы и соединительной ткани | Редко — артралгия |
| Общие расстройства и нежелательные реакции в месте введения препарата | Редко — чувство дискомфорта, жжение и отек в месте инъекции, стерильный абсцесс в месте инъекции, дискомфорт в области грудной клетки, лихорадка, озноб, чувство усталости |
У небольшого числа пациентов сообщалось о возникновении нежелательных эффектов, связанных со способом введения препарата: дискомфорт, зуд, жжение, отек или стерильный абсцесс в месте венопункции.
Приблизительно у 3% пациентов сообщалось о предположительных реакциях повышенной чувствительности. Подобные симптомы появлялись во время проведения инфузии или же вскоре после ее окончания; они включали в себя зуд, приливы, крапивницу/ангионевротический отек, дискомфорт в области грудной клетки, тахикардию, цианоз, респираторные симптомы и парестезию. Редко сообщалось о развитии гипотензии, ассоциируемой с повышенной чувствительностью. При возникновении подобных симптомов пациентам следует прекратить инфузию препарата и обратиться к лечащему врачу. Обычно при возникновении подобных симптомов назначают антигистаминные и/или кортикостероидные препараты.
Взаимодействие
Исследований взаимодействия препарата не проводилось. Поэтому препарат не следует смешивать с другими ЛС.
Передозировка
Не сообщалось о случаях передозировки препарата.
Особые указания
Лечение должно проводиться под наблюдением врача, имеющего опыт лечения болезни Гоше.
Желательно, чтобы врач или медицинские работники регистрировали пациентов с болезнью Гоше, включая пациентов с хроническими нейронопатическими проявлениями заболевания, в специальном регистре.
Препарат содержит натрий и вводится после разведения 0,9% раствором натрия хлорида. После восстановления раствор содержит 0,62 ммоль натрия (200 ЕД/5 мл) или 1,24 ммоль натрия (400 ЕД/10 мл), Эту информацию необходимо учитывать при назначении препарата пациентам, находящимся на диете с контролируемым потреблением натрия.
Разведенный раствор рекомендуется вводить больному сразу или не позднее 3 ч после его приготовления. Разведенный 0,9% раствором натрия хлорида раствор препарата сохраняет свою химическую стабильность в течение 24 ч при хранении при температуре 2–8 °C в защищенном от света месте, однако микробиологическая безопасность зависит от соблюдения асептических условий при восстановлении и разведении препарата. Препарат не содержит консервантов.
Весь неиспользованный препарат и остаточные материалы должны быть уничтожены в соответствии с установленными требованиями.
Гиперчувствительность
Полученные на настоящий момент данные свидетельствуют о том, что в течение первого года терапии IgG-антитела к имиглюцеразе образуются приблизительно у 15% пациентов, получающих терапию. Предполагают, что формирование IgG-антител у таких пациентов вероятнее всего происходит в течение первых 6 мес терапии, и что после 12 мес терапии антитела к Церезиму образуются редко. В связи с этим рекомендуется проводить периодический мониторинг формирования IgG-антител к имиглюцеразе у пациентов с подозреваемым снижением реакции на лечение.
У пациентов, имеющих антитела к Церезиму (имиглюцераза) существует более высокий риск развития реакций повышенной чувствительности (см. раздел «Побочные действия»). Если у пациента развиваются предполагаемые реакции повышенной чувствительности, рекомендуется провести исследование на наличие антител к имиглюцеразе. Как и при применении других протеинсодержащих препаратов, возможно развитие тяжелых реакций повышенной чувствительности аллергического типа. При возникновении таких реакций следует немедленно прекратить инфузию препарата и предпринять соответствующие меры.
Легочная гипертензия
Легочная гипертензия является известным осложнением болезни Гоше. Легочная гипертензия наблюдается у пациентов, как получающих, так и не получающих ферментозаместительную терапию. Какой-либо взаимосвязи развития легочной гипертензии с ферментозаместительной терапией не установлено. Пациентов с респираторными симптомами необходимо обследовать на наличие легочной гипертензии.
Терапевтическую эффективность следует оценивать индивидуально для каждого пациента. Стандартно рекомендуемый мониторинг улучшения состояния при проведении терапии с применением имиглюцеразы включает в себя измерение уровня гемоглобина и тромбоцитов каждые 3 мес, оценку размера селезенки и печени (КТ или МРТ) каждые 12 мес, МРТ всей бедренной кости, рентген бедренной кости и позвоночника, проведение денситометрии каждые 12 мес, а также определение метаболических биомаркеров, таких как хитотриозидаза, каждые 3 мес.
Принимая во внимание степень выраженности болезни Гоше до начала лечения, симптоматику и возраст пациента, по усмотрению лечащего врача может потребоваться дополнительный мониторинг.
При достижении терапевтических целей и после тщательной оценки со стороны лечащего врача, частота мониторинга может быть уменьшена.
Влияние на способность управлять автомобилем или выполнять работы, требующие повышенной скорости физических и психических реакций. Церезим® не влияет или несущественно влияет на способность управлять автомобилем и пользоваться механизмами.
Форма выпуска
Лиофилизат для приготовления раствора для инфузий, 200 ЕД или 400 ЕД. Во флаконах из стекла типа 1 емкостью 20 мл, закрывающихся пробкой из силиконизированного бутила и алюминиевой крышкой, на которую надет пластиковый колпачок марки «Flip off»; в картонной пачке 1 флакон.
Производитель
Фирма-производитель (выпускающий контроль качества): Джензайм Лтд., Великобритания.
Распространение по России — ЗАО «Авентис Фарма».
Условия отпуска из аптек
По рецепту.
Условия хранения
При температуре 2–8 °C (в холодильнике).
Хранить в недоступном для детей месте.
Срок годности
2 года.
Не применять по истечении срока годности, указанного на упаковке.
Описание проверено
-
Крылов Юрий Федорович
(фармаколог, доктор медицинских наук, профессор, академик Международной академии информатизации)
Опыт работы: более 34 лет
Церезим® (Cerezyme®)
💊 Состав препарата Церезим®
✅ Применение препарата Церезим®
Препарат отпускается по рецепту
Входит в список «Жизненно необходимых и важнейших лекарственных
препаратов»
Температура хранения: от 2 до 8 °С
⚠️ Государственная регистрация данного препарата отменена
Описание активных компонентов препарата
Церезим®
(Cerezyme®)
Приведенная научная информация является обобщающей и не может быть использована для принятия
решения о возможности применения конкретного лекарственного препарата.
Дата обновления: 2021.08.30
Владелец регистрационного удостоверения:
Код ATX:
A16AB02
(Имиглюцераза)
Лекарственная форма
|
Препарат отпускается по рецепту |
Церезим® |
Лиофилизат для приготовления раствора для инфузий 400 ЕД: фл. 1 шт. рег. №: П N013386/01 |
Форма выпуска, упаковка и состав
препарата Церезим®
Лиофилизат для приготовления раствора для инфузий в виде порошка белого или почти белого цвета.
* имиглюцераза — это модифицированная форма кислой β-глюкозидазы человека, продуцируемая клетками яичников китайских хомячков с помощью рекомбинантной ДНК-технологии, с маннозной модификацией для направленного взаимодействия с макрофагами.
** ЕД обозначает количество фермента, которое катализирует гидролиз 1 микромоля синтетического субстрата пара-нитрофенил β-D-глюкопиранозида (pNP-Glc) за 1 минуту при температуре 37°С.
Вспомогательные вещества: маннитол, натрия цитрата дигидрат, лимонной кислоты моногидрат, полисорбат 80.
Флаконы стеклянные емкостью 20 мл (1) — пачки картонные.
Фармакологическое действие
Рекомбинантная макрофаг-нацеленная бета-глюкоцереброзидаза — аналог лизосомальной бета-глюкоцереброзидазы человека. Очищенная имиглюцераза — мономерный гликопротеин, в состав которого входят 497 аминокислотных остатков и олигосахаридный компонент. Болезнь Гоше характеризуется функциональной недостаточностью ферментативной активности бета-глюкоцереброзидазы и приводящей к накоплению липида глюкоцереброзида в макрофагах, которые становятся переполненными и носят название «клетки Гоше». Клетки Гоше обычно обнаруживаются в печени, селезенке, костном мозге, иногда — в легких, почках и кишечнике. Вторичные гематологические проявления включают тяжелую анемию и тромбоцитопению, которые сочетаются с характерной прогрессирующей гепатоспленомегалией. Изменения костей являются общими и часто наиболее ослабляющими и инвалидизирующими последствиями болезни Гоше. К ним относятся: остеонекроз, остеопения с вторичными патологическими переломами, недостаточное ремоделирование, остеосклероз. Имиглюцераза компенсирует функциональную недостаточность ферментативной активности бета-глюкоцереброзидазы: катализирует гидролиз липида — глюкоцереброзида, в результате чего образуются глюкоза и церамид (в соответствии с нормальным путем деградации жиров).
После в/в введения в течение 1 ч 4 доз (7.5, 15, 30, 60 ЕД/кг) имиглюцеразы устойчивое повышение ферментативной активности достигается к 30 мин. После завершения инфузии ферментативная активность плазмы быстро снижается.
Фармакокинетика
Vd — 0.09-0.15 л/кг. T1/2 — от 3.6 до 10.4 мин. Клиренс варьирует от 9.8 до 20.3 мл/мин/кг.
Показания активных веществ препарата
Церезим®
Болезнь Гоше I типа (для длительной ферментозаместительной терапии у больных с подтвержденным диагнозом, имеющим клинически значимые проявления данного заболевания: анемия (после исключения других ее причин), тромбоцитопения; патологические изменения костей (после исключения других причин, таких как дефицит витамина D; гепато- или спленомегалия).
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Учитывая гетерогенность и мультисистемную природу болезни Гоше, дозу устанавливают индивидуально после клинической оценки всех проявлений заболевания.
Вводят в/в капельно.
Начальная доза — 60 ЕД/кг 1 раз в 2 нед. (в среднем через 6 мес отмечается улучшение гематологических показателей и симптомов со стороны внутренних органов). Продолжение лечения способствует приостановлению прогрессирования болезни и уменьшению выраженности симптоматики со стороны костной системы. Применение в дозе 2.5 ЕД/кг 3 раза в нед. или 15 ЕД/кг 1 раз в 2 нед. способствует улучшению гематологических параметров, уменьшению размеров печени и селезенки, но не влияет на симптомы со стороны костной системы.
Контрольное обследование пациентов рекомендуется проводить 1 раз в 6-12 мес.
Дозу рекомендуется корректировать (повышать или снижать) в зависимости от выраженности симптомов.
Побочное действие
Со стороны пищеварительной системы: 10-16% — тошнота, диарея, рвота.
Со стороны ЦНС: 10-16% — головная боль, головокружение.
Дерматологические реакции: 10-16% — кожные высыпания.
Аллергические реакции: 3% — генерализованный зуд, ангионевротический отек, одышка, бронхоспазм.
Местные реакции: дискомфорт, зуд и жжение кожи, отек в месте венепункции.
Прочие: 10-16% — повышение температуры тела, «приливы» крови к лицу.
Противопоказания к применению
Повышенная чувствительность к активному веществу.
Применение при беременности и кормлении грудью
C осторожностью применять при беременности и в период лактации.
Применение у детей
С осторожностью применять у детей.
Особые указания
Необходим периодический контроль за образованием IgG антител к имиглюцеразе. В первый год терапии IgG антитела к имиглюцеразе образуются примерно у 15% больных. Появление IgG антител чаще всего происходит в первые 6 мес лечения и редко — после 12 мес терапии.
Во время лечения каждые 2-3 мес следует контролировать активность кислой фосфатазы и АПФ (по мере продолжительности лечения их активность должна снижаться). Эффективность терапии можно контролировать также по уровню активности АЛТ, АСТ каждые 6-12 мес (снижение их активности также указывает на положительный клинический эффект). Каждые 6-12 мес необходим контроль концентрации билирубина, Ca2+, креатинина, электролитов и фосфора.
Для оценки эффективности терапии ежемесячно следует контролировать содержание Hb и тромбоцитов (увеличение их количества свидетельствует об эффективности терапии). Каждые 6 мес следует контролировать размеры печени и селезенки (должны уменьшаться).
Каждые 1-2 года больным показана МРТ длинных костей (при положительном клиническом эффекте их характеристики должны улучшаться). У больных, имеющих антитела к имиглюцеразе, чаще возникают реакции повышенной чувствительности. В подобных случаях рекомендуется премедикация антигистаминными препаратами и/или ГКС, а также снижение частоты инфузий.
С осторожностью применять у детей.
Лекарственное взаимодействие
Фармацевтически несовместим с другими лекарственными средствами.
Адрес производителя
| GENZYME IRELAND Limited |
Ирландия |
IDA Industrial Park, Old Kilmeaden Road, Waterford, Ireland |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Церезим — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
П N013386/01
Торговое наименование:
Церезим®
Международное непатентованное название:
имиглюцераза
Лекарственная форма
Лиофилизат для приготовления раствора для инфузий
Состав
Каждый флакон содержит:
Активный ингредиент: имиглюцераза** 400 ЕД*.
Вспомогательные вещества: маннитол, натрия цитрата дигидрат, лимонной кислоты моногидрат, полисорбат 80.
* ЕД обозначает количество фермента, которое катализирует гидролиз 1 микромоля синтетического субстрата пара-нитрофенил P-D-глюкопиранозида (pNP-Glc) за 1 минуту при температуре 37°С.
** Имиглюцераза — это модифицированная форма кислой β-глюкозидазы человека, продуцируемая клетками яичников китайских хомячков с помощью рекомбинантной ДНК-технологии, с маннозной модификацией для направленного взаимодействия с макрофагами.
Описание:
Лиофилизированный порошок или лиофилизат белого или почти белого цвета.
Описание восстановленного раствора:
Прозрачная бесцветная жидкость без посторонних включений.
Фармакотерапевтическая группа:
фермент-имиглюцераза
АТХ код:
А16АВ02
Фармакологические свойства
Фармакодинамика
Болезнь Гоше — редкое аутосомно-рецессивное метаболическое заболевание, вызванное недостаточностью лизосомального фермента — кислой β-глюкозидазы. Этот фермент катализирует реакцию гидролиза глюкозилцерамида, ключевого компонента липидной структуры клеточных мембран, до глюкозы и церамида. У пациентов с болезнью Гоше происходит недостаточный распад глюкозилцерамида, что приводит к накоплению большого количества данного субстрата в лизосомах макрофагов (они называются «клетками Гоше»), вследствие чего возникают распространенные вторичные патологические изменения.
Клетки Гоше обычно обнаруживаются в печени, селезенке и костном мозге, иногда — в легких, почках и кишечнике. С клинической точки зрения, болезнь Гоше характеризуется гетерогенным фенотипическим спектром. Наиболее частыми проявлениями заболевания являются гепатоспленомегалия, тромбоцитопения, анемия и патологические изменения костной ткани. Эти изменения часто являются наиболее инвалидизирующими проявлениями болезни Гоше. Они включают: инфильтрацию костного мозга, остеонекроз, боль в костях и костные кризы, остеопению и остеопороз, патологические переломы и нарушение роста костей. Болезнь Гоше связана с повышенной продукцией глюкозы и повышенной степенью энергетических затрат в покое, что может вносить вклад в появление повышенной утомляемости и развитие кахексии. У пациентов с болезнью Гоше также могут быть слабо выраженные воспалительные изменения. Кроме того, болезнь Гоше связана с повышенным риском развития диспротеинемии в форме гипергаммаглобулинемии, поликлональной гаммапатии, моноклональной гаммапатии неустановленной этиологии и миеломной болезни. Как правило, течение болезни Гоше характеризуется прогрессированием с риском развития необратимых осложнений, с течением времени появляющихся со стороны различных органов. Клинические проявления болезни Гоше могут неблагоприятно сказываться на качестве жизни. Болезнь Гоше характеризуется проблемой повышенной заболеваемости и ранней смертности. При появлении признаков и симптомов в детском возрасте, как правило, заболевание протекает тяжелее. У детей болезнь Гоше может привести к задержке роста и полового развития.
Имиглюцераза (рекомбинантная макрофаг-таргетированная Р-глюкозидаза) замещает недостаток фермента, гидролизуя глюкозилцерамид, таким образом купируя начальные патофизиологические изменения и предотвращая развитие вторичных патологических проявлений заболевания. Церезим приводит к уменьшению размеров селезенки и печени, улучшает или нормализует уровень тромбоцитов и эритроцитов в крови, улучшает или нормализует минеральную плотность костей и снижает инфильтрацию костного мозга, а также ослабляет или купирует боль в костях и костные кризы. Церезим снижает степень энергетических затрат в покое. Было показано, что он улучшает как ментальные, так и физические характеристики качества жизни пациентов с болезнью Гоше. Церезим снижает уровень хитотриозидазы — биомаркера накопления глюкозилцерамида в макрофагах и ответа на проводимую терапию. При применении у детей Церезим приводит к нормальному половому развитию и наверстыванию роста, что во взрослом возрасте проявляется нормальным ростом и нормальной минеральной плотностью костной ткани.
Скорость и степень выраженности реакции на лечение Церезимом зависит от дозы. Как правило, улучшения со стороны систем органов быстрее появляются в системах с более высокой скоростью метаболизма, например, — со стороны системы крови, по сравнению с теми, где этот процесс происходит медленнее, — как, например, костная ткань.
В регистре пациентов с болезнью Гоше Объединенной международной группы по изучению болезни Гоше (ICGG) анализ большой группы пациентов (n=528) с болезнью Гоше 1 типа показал эффект Церезима, зависимый от времени и дозы, в отношении гематологических и висцеральных проявлений (число тромбоцитов, концентрация гемоглобина, размер печени и селезенки) в дозах, составлявших 15, 30 и 60 ЕД/кг однократно раз в 2 недели. Пациенты, получавшие 60 ЕД/кг раз в 2 недели продемонстрировали более быстрое улучшение и наибольший максимальный эффект лечения по сравнению с пациентами, получавшими более низкие дозы.
Сходным образом, в регистре пациентов с болезнью Гоше (ICGG) анализ минеральной плотности костной ткани с помощью двухэнергетической рентгеновской абсорбциометрии (ДЭРА) показал, что у 342 пациентов после 8 лет терапии был достигнут нормальный уровень минеральной плотности костной ткани при применении дозы Церезима, равной 60 ЕД/кг однократно раз в 2 недели, но этого не было отмечено при более низких дозах — 15 и 30 ЕД/кг однократно раз в 2 недели (Wenstrup и др., 2007).
В исследовании по оценке 2 групп пациентов, получавших средние дозы в 80 ЕД/кг и 30 ЕД/кг раз в 4 недели, среди пациентов, степень инфильтрации костного мозга ≥ 6, у большего числа в группе с более высокой дозой (33%; n=22) было достигнуто снижение инфильтрации на 2 балла после 24 месяцев терапии Церезимом по сравнению с группой, получавшей более низкую дозу (10%; n=13) (de Fost и др., 2006).
Терапия Церезимом в дозе 60 ЕД/кг однократно раз в 2 недели привела к снижению выраженности болей в спине по прошествии 3 месяцев, в течение 12 месяцев уменьшилась выраженность костных кризов, а минеральная плотность костной ткани улучшилась в течение 24 месяцев терапии (Sims и др., 2008).
Врачам и медицинским работникам рекомендуется регистрировать пациентов с болезнью Гоше, включая тех, у которых были отмечены хронические нейропатические проявления данного заболевания, в регистре пациентов с болезнью Гоше Объединенной международной группы по изучению болезни Гоше (ICGG). В данном регистре собраны анонимные данные по пациентам. Целью создания регистра пациентов с болезнью Гоше (ICGG) было улучшение понимания болезни Гоше и оценка эффективности ферментозаместительной терапии, в конечном итоге являясь предпосылкой повышения безопасности и эффективности применения Церезима.
Фармакокинетика
В результате внутривенных инфузий 4 доз имиглюцеразы (7.5, 15, 30, 60 ЕД/кг массы тела) в течение 1 часа, устойчивая ферментная активность достигалась к 30 минуте. После инфузии ферментная активность в плазме быстро снижалась с периодом полувыведения от 3,6 до 10,4 минут. Плазменный клиренс варьировал от 9,8 до 20,3 мл/мин/кг (среднее значение ± стандартное отклонение, 14,5 ± 4,0 мл/мин/кг). Объем распределения в пересчете на вес пациента, колебался от 0,09 до 0,15 л/кг (среднее значение ± стандартное отклонение, 0,12 ± 0,02 л/кг). Вероятно, эти показатели не зависят от дозы или продолжительности инфузии, однако, каждую дозу и скорость инфузии изучали только у 1 или 2 пациентов.
Показания к применению
Для длительной ферменто-заместительной терапии у пациентов с подтвержденным диагнозом болезни Гоше первого типа (без нейронопатических проявлений) или третьего типа (с хроническими нейронопатическими проявлениями), у которых имеются клинически значимые не неврологические проявления данного заболевания.
К не неврологическим проявлениям болезни Гоше относятся один или более из следующих симптомов:
- анемия (после исключения других причин, таких, как дефицит железа)
- тромбоцитопения
- костные заболевания (после исключения других причин, таких как дефицит витамина D)
- гепатомегалия или спленомегалия
Противопоказания
Повышенная чувствительность к активному ингредиенту или другим компонентам препарата.
С осторожностью
Следует соблюдать осторожность при введении препарата пациентам, у которых наблюдается образование антител или симптомов повышенной чувствительности к Цередазе (альглюцеразе).
Влияние на фертильность, применение при беременности и в период грудного вскармливания
Ограниченное количество имеющихся данных об исходах 150 беременностей (главным образом основанных на спонтанных сообщениях и литературных данных) свидетельствует о том, что применение Церезима помогает контролировать болезнь Гоше во время беременности. Кроме того, эти данные не подтвердили наличия токсического действия Церезима на плод, вызывающего мальформации, хотя статистических данных было мало. Сообщения о гибели плода поступали редко и точно неизвестно, были ли эти случаи связаны с применением Церезима, или обусловлены наличием болезни Гоше.
Доклинических исследований на животных в отношении оценки влияния Церезима на беременность, развитие эмбриона/плода, роды и постнатальное развитие не проводилось. Нет сведений о том, проникает ли Церезим через плаценту к развивающемуся плоду.
В каждом случае у беременных пациенток с болезнью Гоше и у тех, кто планирует беременность, необходима оценка соотношения риск-ожидаемая польза лечения. У забеременевших пациенток с болезнью Гоше может возникнуть период повышения активности заболевания во время беременности и в послеродовой период, что проявляется повышенным риском развития изменений со стороны костей, обострением цитопении, кровотечениями и повышением необходимости в гемотрансфузии. Как известно, беременность и грудное вскармливание оказывают стрессовое влияние на обмен кальция у матери и ускоряют процесс ремоделирования костной ткани. Это может вносить вклад в степень выраженности костных изменений при болезни Гоше.
Женщинам, не получавшим лечения, необходимо порекомендовать рассмотреть вопрос о начале терапии до зачатия с целью достижения оптимального уровня общего состояния. У женщин, получающих Церезим, должен быть рассмотрен вопрос о продолжении терапии на протяжении всей беременности. Для индивидуального подбора дозы в соответствии с потребностями пациентки и ее реакцией на лечение необходим тщательный контроль течения беременности и клинических проявлений болезни Гоше.
Нет данных о том, проникает ли действующее вещество препарата в грудное молоко или нет, однако, вероятнее всего данный фермент все-таки поступает в желудочно-кишечный тракт ребенка.
Способ применения и дозы
Для внутривенной инфузии.
Каждый флакон Церезима предназначен только для однократного применения.
После восстановления и разведения препарат вводят путем в/в инфузий. При первых инфузиях Церезим необходимо вводить со скоростью, не превышающей 0,5 ЕД/кг/мин. Впоследствии скорость инфузии можно увеличить, но не более чем до 1 ЕД/кг/мин. Увеличение скорости инфузии должно проводиться под наблюдением медицинского работника.
Инфузию Церезима можно проводить в домашних условиях у пациентов, у которых отмечалась хорошая реакция на введение препарата в течение нескольких месяцев. Решение о возможности введения препарата дома принимается после получения соответствующей оценки и рекомендаций лечащего врача. Инфузия Церезима самим пациентом или лицом, осуществляющим уход, требует подготовки, проводимой медицинским работником в условиях клиники. Пациенту или лицу, осуществляющему за ним уход, объясняется техника проведения инфузии и необходимость ведения дневника. Пациентам, у которых появились нежелательные явления в ходе инфузии, необходимо немедленно прекратить инфузию и обратиться за медицинской помощью. Для последующих инфузий могут потребоваться условия клиники. Доза и частота инфузий не должны изменяться при проведении их дома, а также не должны изменяться без наблюдения медицинского работника.
Вследствие гетерогенности и мультисистемной природы болезни Гоше режим дозирования должен быть индивидуальным для каждого пациента и основываться на всесторонней оценке клинических проявлений заболевания. Только после четкого определения индивидуальной реакции пациента на лечение (в отношении всех соответствующих клинических проявлений заболевания) может быть проведена коррекция дозы и частоты введения препарата либо для поддержания уже достигнутых оптимальных показателей клинического состояния, либо для последующего улучшения тех клинических показателей, которые еще не были нормализованы.
Различные режимы дозирования продемонстрировали эффективность в отношении некоторых или всех не неврологических проявлений заболевания. Применение начальных доз 60 ЕД/кг однократно каждые 2 недели продемонстрировало улучшение гематологических и висцеральных параметров в течение 6 месяцев терапии, а продолжение лечения приводило к приостановлению прогрессирования или уменьшало выраженность костных поражений. Применение доз по 15 ЕД/кг однократно каждые 2 недели продемонстрировало улучшение гематологических показателей и сокращение органомегалии, но не влияло на параметры костной системы. Обычная частота инфузий составляет один раз в 2 недели; это та частота, в отношении которой приведено большинство данных.
Обычно частота инфузий составляет один раз в 2 недели. Исследование поддерживающей терапии раз в 4 недели (Q4) в той же суммарной дозе, что и при терапии раз в 2 недели (Q2), было проведено у взрослых пациентов с устойчивыми остаточными проявлениями болезни Гоше 1 типа. Изменения в уровне гемоглобина, числе тромбоцитов, размере селезенки и печени, показателе костных кризов и изменений со стороны костной ткани по сравнению с исходными значениями составляли предварительно определенную комбинированную конечную точку исследования; достижение и поддержание установленного положительного терапевтического эффекта по гематологическим и висцеральным проявлениям болезни Гоше составляли дополнительную конечную точку. 63% пациентов, получавших режим Q4, и 81%, получавших Q2, соответствовали комбинированной конечной точке при оценке через 24 месяца; различия не были статистически достоверны при доверительном интервале 95% (-0,357; 0,058). 89% пациентов, получавших терапию в режиме Q4, и 100%, получавших в режиме Q2, соответствовали конечной точке, основанной на положительном терапевтическом эффекте; различия не были статистически достоверны при доверительном интервале 95% (-0,231; 0,060). Режим Q4 может быть терапевтически обоснован для некоторых взрослых пациентов с устойчивыми остаточными проявлениями болезни Гоше 1 типа, но в данный момент имеется мало клинических данных.
Применение у детей
Нет необходимости в специальном подборе дозы для детей.
Исследований эффективности препарата в отношении неврологических симптомов у пациентов с хроническими нейронопатическими проявлениями болезни Гоше не проводилось, поэтому специальный режим дозирования для лечения этих проявлений не установлен.
Необходимо регулярно оценивать реакцию пациентов на лечение и корректировать применяемые дозы (увеличивать или снижать) на основании всесторонней оценки реакции пациента в отношении всех клинических проявлений заболевания. Только после четкого определения и стабилизации индивидуальной реакции пациента на лечение (в отношении всех соответствующих клинических проявлений заболевания), может быть проведена коррекция дозы для продолжения эффективного лечения, при условии продолжения тщательного наблюдения за реакцией пациента на лечение и общим состоянием его здоровья. Обычно интервалы между контрольными обследованиями пациента составляют от 6 до 12 месяцев.
Инструкция по восстановлению и разведению препарата
Лиофилизат для приготовления раствора для инфузий восстанавливают водой для инъекций с последующим разведением с помощью 0,9 % раствора натрия хлорида для в/в инъекций и затем вводят путем в/в инфузии.
На основании индивидуального для пациента режима дозирования необходимо определить число флаконов, содержимое которых должно быть восстановлено, и достать их из холодильника.
В некоторых случаях допускается небольшое изменение дозы во избежание неполного использования содержимого флаконов. Дозы могут округляться до наиболее близкой величины, соответствующей числу полных флаконов, но так, чтобы ежемесячно вводимая доза существенно не изменялась.
Восстановление и разведение препарата должны проводиться в асептических условиях. Восстановление
Содержимое каждого флакона восстанавливают добавлением 10,2 мл воды для инъекций, избегая введения воды для инъекций сильной струей, после чего осторожно перемешивают раствор, не допуская образования пены. Объем восстановленного раствора составляет 10,6 мл, а рН восстановленного раствора — приблизительно 6,1. Восстановленный раствор должен быть прозрачным, бесцветным и не должен содержать посторонних частиц. После восстановления необходимо сразу же развести содержимое флаконов. Перед разведением необходимо провести визуальный осмотр восстановленного раствора на наличие посторонних частиц и изменение цвета. Нельзя использовать флаконы при наличии в полученном растворе посторонних частиц или при изменении цвета раствора. После восстановления содержимое флаконов сразу разводится, препарат не хранится для последующего применения.
Разведение
Восстановленный раствор содержит 40 ЕД имиглюцеразы в 1 мл. Извлекается 10,0 мл восстановленного раствора из каждого флакона, полученный объем объединяется, затем его разводят 0,9% раствором хлорида натрия для в/в инъекций до общего объема 100-200 мл. Полученный раствор осторожно перемешивают.
Побочное действие
Ниже представлены нежелательные реакции, классифицированные по системам органов и частоте возникновения (часто — от ≥1/100 до <1/10, нечасто (от ≥1/1000 до <1/100) и редко (от ≥1/10000 до <1/1000)). В каждой группе нежелательные реакции перечислены в порядке уменьшения степени их тяжести.
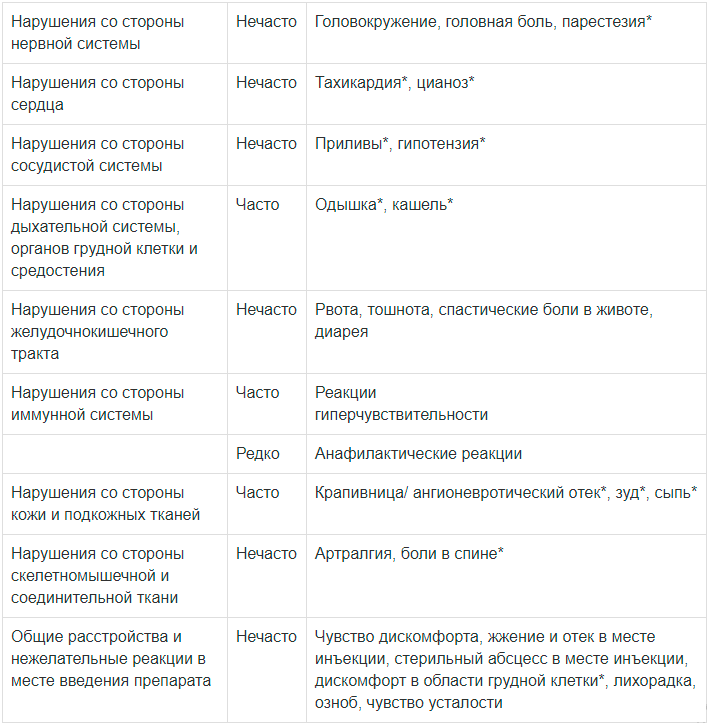
Всего приблизительно у 3% пациентов были выявлены симптомы, свидетельствующие о гиперчувствительности (обозначенные * в таблице выше). Они были зарегистрированы в ходе инфузий или сразу после них. Как правило, такие симптомы купируются применением антигистаминных препаратов и/или глюкокортикоидов. Пациентам следует порекомендовать прекратить инфузию препарата и связаться с лечащим врачом при появлении таких симптомов.
Передозировка
О случаях передозировки препарата не сообщалось. У пациентов использовались дозировки до 240 ЕД/кг однократно раз в две недели.
Взаимодействие с другими лекарственными препаратами и другие формы взаимодействий
Исследований взаимодействия препарата не проводилось. Поэтому препарат не следует смешивать с другими лекарственными средствами.
Особые указания
При ведении пациентов с болезнью Гоше лечащим врачам необходимо консультироваться с врачами, имеющими опыт терапии данной патологии.
Врачам и медицинским работникам рекомендуется регистрировать пациентов с болезнью Гоше, включая тех, у которых были отмечены нейропатические проявления данного заболевания, в регистре пациентов с болезнью Гоше Объединенной международной группы по изучению болезни Гоше (ICGG). Данный лекарственный препарат содержит натрий и вводится внутривенно после разведения в 0,9% растворе хлорида натрия. После разведения раствор содержит 1,24 ммоль натрия (400 ЕД/10 мл).
Это необходимо принимать во внимание пациентам, находящимся на диете с ограничением соли.
Разведенный раствор рекомендуется вводить через проходной фильтр, обладающий низкой белковосвязывающей активностью, с диаметром пор 0,2 мкм для удаления частиц белка, что не приведет к снижению активности имиглюцеразы.
Разведенный раствор рекомендуется вводить пациенту сразу или не позднее 3 ч после его приготовления. Разведенный 0,9% раствором натрия хлорида раствор препарата сохраняет свою химическую стабильность в течение 24 ч при хранении при температуре 2-8 °C в защищенном от света месте, однако, микробиологическая безопасность зависит от соблюдения асептических условий при восстановлении и разведении препарата.
Гиперчувствительность
Данные, полученные с использованием скринингового иммуносорбентного ферментного анализа (ELISA) и подтвержденные в ходе радиоиммунопреципитационного анализа, свидетельствуют о том, что в течение первого года терапии IgG-антитела к имиглюцеразе образуются приблизительно у 15% пациентов, получающих терапию. Предполагают, что формирование IgG-антител у таких пациентов вероятнее всего происходит в течение первых 6 месяцев терапии, и что после 12 месяцев терапии антитела к Церезиму образуются редко. В связи с этим при подозрении на снижение ответа на терапию рекомендуется проводить периодический мониторинг уровня IgG-антител к имиглюцеразе. У пациентов, имеющих антитела к имиглюцеразе, существует более высокий риск развития реакций повышенной чувствительности. Если у пациента развиваются предполагаемые реакции повышенной чувствительности, рекомендуется провести исследование на наличие антител к имиглюцеразе. Как и при применении других внутривенных протеинсодержащих препаратов, возможно развитие тяжелых реакций повышенной чувствительности аллергического типа, но они возникают редко. При возникновении таких реакций следует немедленно прекратить инфузию Церезима и предпринять соответствующие меры. Необходимо соблюдать действующие медицинские стандарты неотложной терапии.
Если у пациентов было зарегистрировано образование антител к Цередазе (альглюцеразе) или появление симптомов гиперчувствительности, лечение Церезимом (имиглюцеразой) должно проводиться с осторожностью.
Легочная гипертензия.
Легочная гипертензия является известным осложнением болезни Гоше. Пациенты со спленэктомией в анамнезе имеют повышенный риск развития легочной гипертензии. Лечение Церезимом в большинстве случаев снижает потребность в проведении спленэктомии, а раннее начало терапии Церезимом снижало риск развития легочной гипертензии. Рекомендовано регулярное обследование на предмет выявления симптомов легочной гипертензии после постановки диагноза болезнь Гоше и в дальнейшем. Пациенты, которым поставлен диагноз легочная гипертензия, в частности, должны получать адекватные дозы Церезима для контроля болезни Гоше, а также у них должна проводиться оценка на предмет необходимости применения специальной терапии для лечения легочной гипертензии.
Влияние на способность управлять автомобилем и пользоваться механизмами
Церезим® не влияет или несущественно влияет на способность управлять автомобилем и пользоваться механизмами.
Форма выпуска
Лиофилизат для приготовления раствора для инфузий, 400 ЕД во флаконах из стекла типа I, емкостью 20 мл, закрывающихся пробкой из силиконизированного бутила и алюминиевой крышкой, на которую надет пластиковый колпачок. Каждый флакон с инструкцией по применению помещают в картонную пачку.
Условия хранения
Хранить при температуре 2°С — 8°С (в холодильнике).
Хранить в недоступном для детей месте.
Срок годности
2 года.
Не использовать по истечении срока годности.
Условия отпуска из аптек
По рецепту.
Наименование производителя и адрес места производства:
Производство, первичная упаковка:
Джензайм Ирландия Лимитед
ИДА Индастриал Парк, Олд Килмиден Роуд, Уотефорд, Ирландия
Вторичная (потребительская) упаковка и выпускающий контроль качества:
Джензайм Лтд.
Холлэндс Роуд 37, Хаверхилл
Суффолк СВ9 8PU, Великобритания
Джензайм Ирландия Лимитед
ИДА Индастриал Парк, Олд Килмиден Роуд, Уотефорд, Ирландия
Претензии потребителей направлять по адресу:
Представительство АО «Санофи-авентис груп»
125009, г. Москва, ул. Тверская, д. 22.
В случае упаковки препарата Церезим®, лиофилизат для приготовления раствора для инфузий 400 ЕД на ОАО «Фармстандарт-УфаВИТА»:
Наименование и адрес места производства:
Производство, первичная упаковка:
Джензайм Ирландия Лимитед
ИДА Индастриал Парк, Олд Килмиден Роуд, Уотефорд, Ирландия
Вторичная (потребительская) упаковка и выпускающий контроль качества:
ОАО «Фармстандарт-УфаВИТА»
450077, Россия, г. Уфа, ул. Худайбердина, д. 28.
Претензии потребителей направлять по адресу:
ОАО «Фармстандарт-УфаВИТА»
450077, Россия, Республика Башкортостан, г. Уфа, ул. Худайбердина, д. 28.
*Цены в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Фармакодинамика
Болезнь Гоше является редкой рецессивно-наследуемой метаболической патологией, вызываемой недостаточностью лизосомального фермента кислой β-глюкозидазы. Фермент участвует в расщеплении глюкозилцерамида, который является ключевым компонентом липидных структур клеточных мембран, до глюкозы и церамида. У пациентов с болезнью Гоше расщепление глюкозилцерамида нарушено, что приводит к накоплению большого количества этого субстрата в лизосомах макрофагов (так называемых «клетках Гоше») и ведет к развитию вторичной патологии.
Клетки Гоше обычно находят в печени, селезенке и костном мозге, иногда — в легких, почках и кишечнике. С клинической точки зрения болезнь Гоше характеризуется гетерогенным и фенотипическим спектром. Наиболее частыми проявлениями болезни являются гепатоспленомегалия, тромбоцитопения, анемия и патологические изменения костной ткани. Патологические изменения костной ткани часто являются наиболее инвалидизирующими проявлениями болезни Гоше. Они включают инфильтрацию костного мозга, остеонекроз, боль в костях и костные кризы, остеопению и остеопороз, патологические переломы, нарушение роста.
Болезнь Гоше связана с повышенной продукцией глюкозы и повышенной степенью энергетических затрат в покое, что может вносить вклад в появление повышенной утомляемости и развитие кахексии. У пациентов с болезнью Гоше также могут быть слабо выраженные воспалительные изменения. Кроме того, болезнь Гоше связана с повышенным риском развития диспротеинемии в форме гипергаммаглобулинемии, поликлональной гаммапатии, моноклональной гаммапатии неустановленной этиологии и миеломной болезни.
Как правило, течение болезни Гоше характеризуется прогрессированием с риском развития необратимых осложнений, с течением времени появляющихся со стороны различных органов. Клинические проявления болезни Гоше могут неблагоприятно сказываться на качестве жизни. Болезнь Гоше характеризуется проблемой повышенной заболеваемости и ранней смертности. При появлении признаков и симптомов в детском возрасте, как правило, заболевание протекает тяжелее. У детей болезнь Гоше может привести к задержке роста и полового развития.
Легочная гипертензия является известным осложнением болезни Гоше. У пациентов после спленэктомии риск легочной гипертензии повышен. Терапия Церезимом снижает потребность в спленэктомии в большинстве случаев, а раннее начало лечения Церезимом ассоциировано со сниженным риском развития легочной гипертензии. Необходимо периодически тестировать пациента с болезнью Гоше на наличие легочной гипертензии и проводить сравнительную оценку в динамике.
Пациенты с установленным диагнозом легочной гипертензии должны получать, в частности, адекватные дозы Церезима для того, чтобы контролировать течение имеющейся фоновой болезни Гоше, а также следует провести оценку на необходимость назначения дополнительной специфической терапии легочной гипертензии.
Фармакодинамические свойства
Имиглюцераза (рекомбинантная макрофаг-таргетированная кислая β-глюкозидаза) замещает недостаток фермента, гидролизуя глюкозилцерамид, таким образом корректируя начальные патофизиологические изменения и предотвращая развитие вторичных патологических проявлений заболевания.
Церезим приводит к уменьшению размеров селезенки и печени, уменьшает или устраняет анемию и тромбоцитопению, улучшает минеральную плотность костей, уменьшает поражение костного мозга, ослабляет или устраняет боль в костях и костные кризы. Церезим снижает степень энергетических затрат в покое.
Было показано, что он улучшает как ментальные, так и физические характеристики качества жизни пациентов с болезнью Гоше. Церезим снижает уровень хитотриозидазы биомаркера накопления глюкозилцерамида в макрофагах и ответа на проводимую терапию. Было показано, что при применении у детей Церезим способствует нормальному половому развитию и наверстыванию роста, что во взрослом возрасте проявляется нормальным ростом и нормальной минеральной плотностью костной ткани.
Данные о клинической эффективности и безопасности
Скорость и степень выраженности ответа на назначение Церезима зависят от дозы. Как правило, улучшения со стороны систем органов быстрее появляются в системах с более высокой скоростью метаболизма, например, — со стороны системы крови, по сравнению с теми, где этот процесс происходит медленнее, — как, например, костная ткань.
В регистре пациентов с болезнью Гоше Объединенной международной группы по изучению болезни Гоше (ICGG) анализ большой группы пациентов (n=528) с болезнью Гоше 1 типа показал эффект Церезима, зависимый от времени и дозы, в отношении гематологических и висцеральных проявлений (число тромбоцитов, концентрация гемоглобина, размеры печени и селезенки) в дозах, составлявших 15, 30 и 60 ЕД/кг массы тела один раз в 2 недели. Пациенты, получавшие 60 ЕД/кг массы тела один раз в 2 недели продемонстрировали более быстрое улучшение и наибольший максимальный эффект лечения по сравнению с пациентами, получавшими более низкие дозы.
Сходным образом, в регистре пациентов с болезнью Гоше (ICGG) анализ минеральной плотности костной ткани с помощью двухэнергетической рентгеновской абсорбциометрии (ДЭРА) показал, что у 342 пациентов после 8 лет терапии был достигнут нормальный уровень минеральной плотности костной ткани при применении дозы Церезима, равной 60 ЕД/кг массы тела один раз в 2 недели, но этого не было отмечено при более низких дозах 15 и 30 ЕД/кг массы тела один раз в 2 недели (Wenstrup и др., 2007).
В исследовании по оценке 2 групп пациентов, получавших средние дозы в 80 ЕД/кг массы тела и 30 ЕД/кг массы тела один раз в 4 недели, среди пациентов, степень инфильтрации костного мозга >6, у большего числа в группе с более высокой дозой (33%; п=22) было достигнуто снижение инфильтрации на 2 балла после 24 месяцев терапии Церезимом по сравнению с группой, получавшей более низкую дозу (10%; п=13) (de Fost и др., 2006).
Терапия Церезимом в дозе 60 ЕД/кг массы тела один раз в 2 недели привела к снижению выраженности болей в спине по прошествии 3 месяцев, в течение 12 месяцев уменьшилась выраженность костных кризов, а минеральная плотность костной ткани улучшилась в течение 24 месяцев терапии (Sims и др., 2008).
Обычно частота инфузий составляет один раз в 2 недели (см. раздел «Способ применения и дозы»). У взрослых пациентов со стабильными остаточными проявлениями болезни Гоше 1 типа исследовалась поддерживающая терапия при введении один раз в 4 недели (Q4) в той же суммарной дозе, как и при введении один раз в 2 недели (Q2). Предварительно определенная комбинированная конечная точка исследования включала изменение уровня гемоглобина, числа тромбоцитов, размеров печени и селезенки, показателя костных кризов и изменений со стороны костной ткани; дополнительной конечной точкой являлось достижение или поддержание определенных терапевтических эффектов при болезни Гоше по гематологическим и висцеральным показателям. Комбинированной конечной точки достигли к 24 месяцам терапии 63% пациентов из Q4- и 81% пациентов из Q2-группы лечения, различия не были статистически достоверны при доверительном интервале 95% (- 0,357; 0,058). 89% пациентов из группы Q4 и 100% пациентов из группы Q2 соответствовали конечной точке, основанной на положительном терапевтическом эффекте, различия не были статистически достоверны при доверительном интервале 95% (-0,231; 0,060). Режим введения Q4 может представлять собой вариант терапии для некоторых взрослых пациентов со стабильными остаточными проявлениями болезни Гоше 1 типа, но клинические данные ограничены.
Не проводилось контролируемых клинических исследований в отношении эффективности Церезима при неврологических проявлениях заболевания. Таким образом, отсутствуют выводы об эффекте ферментозаместительной терапии на неврологические проявления болезни Гоше.
Врачам и медицинским работникам рекомендуется регистрировать пациентов с болезнью Гоше, включая тех, у которых были отмечены хронические нейропатические проявления данного заболевания, в регистре пациентов с болезнью Гоше Объединенной международной группы по изучению болезни Гоше (ICGG). В данном регистре собраны анонимные данные по пациентам. Целью создания регистра пациентов с болезнью Гоше (ICGG) является изучение болезни Гоше, и оценка эффективности ферментозаместительной терапии, что в конечном итоге является предпосылкой повышения безопасности и эффективности применения Церезима.
Фармакокинетика
В результате внутривенных инфузий 4 доз имиглюцеразы (7,5, 15, 30, 60 ЕД/кг массы тела) в течение одного часа, устойчивая ферментная активность достигалась к 30 минуте. После инфузии ферментная активность в плазме быстро снижалась с периодом полувыведения от 3,6 до 10,4 минут. Плазменный клиренс варьировал от 9,8 до 20,3 мл/мин/кг (среднее ± SD, 14,5 ± 4,0 мл/мин/кг). Объем распределения в пересчете на вес пациента колебался от 0,09 до 0,15 л/кг (среднее ± SD, 0,12 ± 0,02 л/кг). Вероятно, данные показатели не зависят от дозы или продолжительности инфузии, однако, каждую дозу и скорость инфузии изучали только у одного или двух пациентов.
Данные доклинических исследований безопасности
Доклинические данные не выявили опасности применения у людей, основываясь на исследованиях фармакологической безопасности, токсичности однократной и повторной доз, а также генотоксичности.
Общая информация
Устаревшее наименование
—
Владелец
Номер регистрационного удостоверения РФ
П N013386/01
Действующее вещество (МНН)
Форма выпуска / дозировка
Лиофилизат для приготовления раствора для инфузий
Лекарственная форма ГРЛС
Лиофилизат д/инфузий
Состав
Каждый флакон содержит:
Активный ингредиент: имиглюцераза** 400 ЕД*.
Вспомогательные вещества: маннитол, натрия цитрата дигидрат, лимонной кислоты моногидрат, полисорбат 80.
* ЕД обозначает количество фермента, которое катализирует гидролиз 1 микромоля синтетического субстрата пара-нитрофенил β-D-ппокопиранозида (pNP-Glc) за 1 минуту при температуре 37°С.
** Имиглюцераза — это модифицированная форма кислой бета-глюкозидазы человека, продуцируемая клетками яичников китайских хомячков с помощью рекомбинантной ДНК-технологии, с маннозной модификацией для направленного взаимодействия с макрофагами.
Описание препарата
Лиофилизированный порошок или лиофилизат белого или почти белого цвета.
Фармако-терапевтическая группа
Ферментное средство
