Описание препарата ИЛСИРА® (раствор для подкожного введения, 180 мг/мл) основано на официальной инструкции, утверждено компанией-производителем в 2022 году
Дата согласования: 20.06.2022
Особые отметки:
Содержание
- Фотографии упаковок
- Действующее вещество
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав
- Описание лекарственной формы
- Фармакологическое действие
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Производитель
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Аналоги (синонимы) препарата ИЛСИРА®
Фотографии упаковок
20.06.2022
Действующее вещество
ATX
Фармакологическая группа
Состав
| Раствор для п/к введения | 1 мл/0,9 мл* |
| действующее вещество: | |
| левилимаб | 180,0/162,0 мг |
| вспомогательные вещества: натрия ацетата тригидрат — 0,436/0,392 мг; глицин — 7,5/6,8 мг; маннитол — 23,0/20,7 мг; кислота уксусная ледяная — до рН 5,0/5,0; вода для инъекций — до 1,0/0,9 мл | |
| * В предварительно наполненном шприце |
Описание лекарственной формы
Раствор для п/к введения: прозрачный, желто-коричневого цвета. Возможно наличие легкой опалесценции.
Фармакологическое действие
Фармакодинамика
Левилимаб — рекомбинантное моноклональное антитело к рецептору ИЛ-6 подкласса IgG1. Левилимаб связывается и блокирует как растворимые (рИЛ6Р), так и мембранные рецепторы ИЛ-6 (мИЛ6Р). Блокада обеих форм рецептора позволяет предотвратить реализацию ИЛ-6-ассоциированного провоспалительного каскада, препятствует активации антигенпрезентирующих клеток, В- и Т-лимфоцитов, моноцитов и макрофагов, эндотелиальных клеток и фибробластов, и избыточной продукции других провоспалительных цитокинов. ИЛ-6 является ключевым элементом синдрома массивного высвобождения цитокинов (синдром цитокинового шторма, гемофагоцитарный лимфогистиоцитоз или синдром активации макрофагов), который может привести к острому респираторному дистресс-синдрому, полиорганной недостаточности и являться причиной летального исхода. Массивное высвобождение цитокинов (цитокиновый шторм) наблюдается у пациентов, получающих иммуносупрессивную терапию, включая деплецирующие агенты (в частности моноклональные антитела к рецепторам Т- и В-лимфоцитов), а также при тяжелых инфекционных заболеваниях, в т.ч. у пациентов с COVID-19. Высокий уровень ИЛ-6 в крови ассоциирован с более тяжелым течением новой коронавирусной инфекции и выраженными изменениями легких, что обусловливает потребность в интенсивной терапии и увеличивает риск летального исхода при COVID-19. ИЛ-6 — единственный цитокин, непосредственно индуцирующий синтез острофазовых белков в гепатоцитах: С-реактивного белка (СРБ), фибриногена, сывороточного амилоидного белка А, гипсидина, лептина. Кроме того, ИЛ-6 участвует в активации и поддержании местных воспалительных реакций (образование паннуса в синовии, стимуляция остеокластогенеза — эрозия хрящевой ткани, остеопороз), что наблюдается в патогенезе ревматоидного артрита.
Специфическая противовоспалительная активность левилимаба продемонстрирована в тестах in vitro и in vivo. Левилимаб оказывает антипролиферативное действие на культуру клеток DS-1, вызывая дозозависимое ингибирование роста клеток. На модели коллагениндуцированного артрита у яванских макак (Macaca fascicularis) многократное (1 раз в нед в течение 7 нед) п/к введение левилимаба сопровождается снижением выраженности воспалительной реакции в суставах, что подтверждено при гистологическом исследовании (значимое снижение выраженности воспалительных и дегенеративных изменений хрящевой ткани).
Изменение параметров фармакодинамических маркеров (нарастание концентрации рИЛ6Р, насыщение мИЛ6Р, нарастание концентрации ИЛ-6) свидетельствует о высокоэффективной дозозависимой нейтрализации препаратом левилимаб обеих форм рецептора ИЛ-6, что, в свою очередь, сопровождается быстрым и выраженным снижением сывороточной концентрации СРБ, отражающим эффективное подавление воспалительного процесса. В клинических исследованиях левилимаба продемонстрировано блокирование до 90% мембранных рецепторов к ИЛ-6 в течение первых 2 ч от момента однократного п/к введения препарата в дозе 1,6 мг/кг и более.
Фармакокинетика
Всасывание/распределение. При однократном п/к введении левилимаба наблюдается дозозависимый рост его концентрации в сыворотке крови. После введения препарат начинает обнаруживаться в сыворотке крови пациентов через 2–12 ч, и его концентрация нарастает, достигая максимальных значений через 96 (72–168) ч. Дозы препарата, превышающие 2,0 мг/кг, продемонстрировали двухфазный характер увеличения концентрации: первый пик наблюдался в период 48–72 ч, второй — к 168 ч с последующим снижением до неопределяемых значений к 70-му дню.
После однократного п/к введения препарата в дозе 162 мг Cmax левилимаба в сыворотке крови составляла 17543 (10975; 28323) нг/мл, а значения показателя AUC, рассчитанной в период 0–168 ч (AUC0–168) — 1866231 (1297632; 3719014) нг·ч/мл.
При многократном введении левилимаба пациентам с ревматоидным артритом значения суммарной AUC, рассчитанной в период 0-2016 ч после введения (AUC0–2016), составили 189580779 (134794695; 230680771) нг·ч/мл при введении 1 раз в нед и 50763951 (34465213,5; 65810194,5) нг·ч/мл при введении 1 раз в 2 нед. Показатель Сmax-mult при повторных введениях нарастал и достигал значений 201024 (151563; 246408) нг/мл при еженедельном введении препарата и 51570 (37201; 71740) нг/мл при введении 1 раз в 2 нед. При этом Tmax составляло 1848 (1512; 2016) ч при еженедельном введении препарата и 1848 (1512; 1848) ч при введении 1 раз в 2 нед соответственно. Стационарный Vd составил 7871,029 (4226,795; 13363,547) мл при введении препарата 1 раз в нед и 7130,453 (5532,978; 11387,959) мл при введении 1 раз в 2 нед.
При повторных введениях отмечается накопление препарата, с ростом Cmax в 6,5–14,2 раза при еженедельном введении и в 1,9–4,2 раза при введении препарата 1 раз в 2 нед. Коэффициент кумуляции составил 10,932 (6,446; 14,178) для еженедельного введения препарата и 2,593 (1,902; 4,164) для введения 1 раз в 2 нед.
Таким образом у пациентов с ревматоидным артритом многократное п/к введение левилимаба 1 раз в нед обеспечивает более высокую сывороточную концентрацию и экспозицию по сравнению с введением 1 раз в 2 нед.
Выведение. Общий клиренс (Cl) левилимаба после однократного введения в дозе 2,2 мг/кг составил (35,288±11,7) мл/ч, а в дозе 2,9 мг/кг показатель Cl — (25,974±1,1) мл/ч. T1/2 однократной п/к дозы 2,9 мг/кг составил 133,683 (92,754; 197,197) ч. Значения показателей, характеризующих период элиминации, обладают дозозависимостью (показатели среднего времени пребывания препарата в организме и T1/2 нарастают с увеличением введенной дозы, а Cl — снижается), что говорит о нелинейной фармакокинетике препарата, обусловленной мишень-опосредованными распределением и элиминацией.
Особые группы пациентов
Почечная и печеночная недостаточность. Специальных исследований у данной категории пациентов не проводилось; фармакокинетические данные у больных с почечной и печеночной недостаточностью отсутствуют.
Возраст старше 65 лет. Фармакокинетические данные у лиц старше 65 лет отсутствуют.
Показания
- патогенетическая терапия синдрома высвобождения цитокинов при тяжелом течении новой коронавирусной инфекции (CОVID-19);
- ревматоидный артрит умеренной или высокой степени активности у взрослых с отсутствием адекватного ответа на терапию одним или несколькими болезньмодифицирующими противоревматическими препаратами, в т.ч. для торможения рентгенологической прогрессии (левилимаб применяется в комбинированной терапии с метотрексатом и/или другими синтетическими базисными противовоспалительными препаратами).
Противопоказания
- гиперчувствительность к левилимабу, а также к любому из вспомогательных веществ препарата;
- клинически значимые активные инфекции, включая туберкулез;
- сепсис, обусловленный патогенами, отличными от COVID-19;
- вирусный гепатит В;
- нейтропения менее 0,5·109/л;
- тромбоцитопения менее 50·109/л;
- повышение активности АСТ или АЛТ более чем в 5 раз;
- печеночная недостаточность тяжелой степени (класс С по классификации Чайлд-Пью);
- почечная недостаточность тяжелой и терминальной степени тяжести (СКФ <30 мл/мин);
- комбинированное применение с ингибиторами ФНО-α или применение в течение 1 мес после терапии моноклональными антителами к ФНО-α;
- беременность, грудное вскармливание;
- возраст до 18 лет.
С осторожностью: хронические и рецидивирующие инфекции или анамнестические указания на них; сопутствующие заболевания, предрасполагающие к развитию инфекций; период ранней реконвалесценции после тяжелых и среднетяжелых инфекционных заболеваний; недавно проведенная вакцинация живыми аттенуированными вакцинами; печеночная недостаточность легкой и средней степени тяжести (класс А и В по классификации Чайлд-Пью); почечная недостаточность средней степени тяжести (СКФ <60 и ≥30 мл/мин); дивертикулит, дивертикулез и язвенное поражение органов ЖКТ, в т.ч. в анамнезе (в связи с риском перфорации ЖКТ); демиелинизирующие заболевания; иммуносупрессивная терапия после трансплантации органов; раннее выявление инфекционных заболеваний на фоне терапии (в связи со способностью левилимаба подавлять реакции острой фазы воспаления); пожилой возраст (в связи с ограниченными данными клинических исследований).
Применение при беременности и кормлении грудью
Беременность. Исследований влияния на плод у беременных женщин не проводилось. Известно, что моноклональные антитела могут проникать через плацентарный барьер. Препарат ИЛСИРА® противопоказан к применению во время беременности. Женщины детородного возраста и их половые партнеры должны использовать эффективные средства контрацепции в период проведения терапии левилимабом.
Грудное вскармливание. Неизвестно, проникает ли левилимаб в грудное молоко. Учитывая, что IgG, к которым относится левилимаб, могут выделяться с грудным молоком, препарат ИЛСИРА® противопоказан к применению в период грудного вскармливания.
Фертильность. Данные о влиянии препарата на фертильность у людей отсутствуют.
Способ применения и дозы
П/к.
Препарат ИЛСИРА® предназначен для введения как в амбулаторно-поликлинических, так и в стационарных условиях.
Применение левилимаба должно осуществляться под контролем врача. В случае длительного применения препарата, в частности для терапии ревматоидного артрита, если врач считает это возможным, после соответствующего обучения технике п/к инъекций пациенты могут самостоятельно вводить себе препарат.
Препарат ИЛСИРА® вводится с помощью преднаполненного шприца в область передней брюшной стенки (отступая не менее 5 см от пупка), передней и боковой поверхности бедра или средней трети наружной поверхности плеча.
Не следует вводить препарат в места с поврежденной или измененной кожей (наличие уплотнений, покраснений, новообразований, гиперпигментаций или повышенной чувствительности).
Патогенетическая терапия синдрома высвобождения цитокинов при тяжелом течении новой коронавирусной инфекции (CОVID-19)
Рекомендуемая доза препарата ИЛСИРА® составляет 324 мг однократно в виде двух п/к инъекций по 162 мг каждая. В случае недостаточного эффекта первой дозы левилимаба возможно повторное введение препарата через 48–96 ч в дозе 324 мг в виде двух п/к инъекций по 162 мг каждая. Решение о необходимости повторного введения принимается исключительно врачом.
Ревматоидный артрит
Рекомендуемая доза препарата ИЛСИРА® составляет 162 мг/нед.
При развитии нежелательных явлений в ходе терапии ревматоидного артрита, связанных с изменением лабораторных показателей, следует провести коррекцию дозы и режима введения в соответствии с рекомендациями в таблицах 1, 2 и 3.
Таблица 1
Рекомендации по коррекции дозы при повышении активности печеночных ферментов АЛТ или АСТ
| Значение показателя АЛТ или АСТ | Рекомендации |
| Превышение ВГН в 1–3 раза | При необходимости провести коррекцию дозы одновременно принимаемых препаратов, обладающих гепатотоксическим эффектом (базисных противовоспалительных препаратов, антибактериальных средств, иммуномодулирующих препаратов). При устойчивом повышении активности трансаминаз в данном диапазоне снизить частоту инъекций препарата ИЛСИРА® до 1 раза в 2 нед или прервать терапию препаратом ИЛСИРА® до нормализации показателей АЛТ и АСТ. Возобновить терапию препаратом в дозе 162 мг с частотой введения 1 раз в 2 нед или 1 раз в нед в соответствии с клинической необходимостью |
| Превышение ВГН в 3–5 раз | Следует отменить лечение препаратом ИЛСИРА® до снижения уровня показателя, менее чем в 3 раза превышающего ВГН. Далее следовать вышеуказанным рекомендациям для превышения ВГН в 1–3 раза. При сохранении уровня показателя, более чем в 3 раза превышающего ВГН, отменить терапию препаратом ИЛСИРА® |
| Превышение ВГН более чем в 5 раз | Следует прекратить лечение препаратом ИЛСИРА® |
Таблица 2
Рекомендации по коррекции дозы при снижении абсолютного числа нейтрофилов (АЧН)
| Значение показателя (число клеток·109/л) | Рекомендации |
| АЧН >1 | Дозу препарата ИЛСИРА® оставить без изменений |
| АЧН 0,5–1 | Следует прервать лечение препаратом ИЛСИРА®. При повышении АЧН до 1·109/л и выше рассмотреть возобновление терапии препаратом в рекомендуемой дозе в соответствии с клинической необходимостью |
| АЧН <0,5 | Следует прекратить лечение препаратом ИЛСИРА® |
Таблица 3
Рекомендации по коррекции дозы при снижении количества тромбоцитов
| Значение показателя (число клеток·109/л) | Рекомендации |
| 50–100 | Следует прервать лечение препаратом ИЛСИРА®. При увеличении количества тромбоцитов до 100·109/л и выше рассмотреть возобновление терапии препаратом ИЛСИРА® в дозе 162 мг с частотой введения 1 раз в 2 нед и увеличить частоту введений до 1 раза в нед в соответствии с клинической необходимостью |
| <50 | Следует прекратить лечение препаратом ИЛСИРА® |
Пропуск дозы. При пропуске очередного введения по любой причине инъекция препарата ИЛСИРА® должна быть произведена как можно быстрее. Новый отсчет для даты следующего введения начинают с момента фактически проведенной инъекции препарата ИЛСИРА®.
Подготовка к проведению п/к инъекции (на данном этапе не следует снимать колпачок шприца)
1. Тщательно вымыть руки.
2. Извлечь упаковку со шприцем из холодильника. Затем извлечь шприц с лекарственным препаратом из картонной пачки. Осмотреть шприц, а также лекарственный препарат, находящийся в нем. Нельзя использовать шприц в случае: помутнения раствора, наличия в препарате посторонних видимых частиц; изменения цвета; повреждения любых частей шприца; истечения срока годности («годен до…»), указанного на картонной пачке, а также на этикетке шприца.
3.Оставить шприц при комнатной температуре приблизительно на 25–30 мин. Не следует согревать шприц с препаратом каким-либо другим способом.
4. Подготовить спиртовую салфетку/ватный тампон.
Техника выполнения п/к инъекции препарата ИЛСИРА® в преднаполненном шприце
1. Выбрать место инъекции (передняя брюшная стенка (отступая не менее 5 см от пупка), передняя и боковая поверхность бедра или средняя треть наружной части плеча (возможные места для инъекций закрашены на рисунке ниже).
2. Нельзя вводить препарат в место на коже, где имеется болезненность, покраснение, уплотнение или кровоподтек. Эти признаки могут указывать на наличие инфекции. Также не следует вводить препарат в места родинок, гиперпигментаций и шрамов.
3. Место укола необходимо обработать спиртовой салфеткой круговыми движениями.
4. Шприц не встряхивать.
5. Снять колпачок с иглы, не дотрагиваясь до иглы и избегая прикосновения к другим поверхностям.
6. Одной рукой взять в складку обработанную кожу.
7. В другую руку взять шприц, держа его градуированной поверхностью вверх. Введение препарата необходимо осуществлять под углом 45 или 90° к поверхности кожи в зависимости от толщины кожи и выраженности подкожно-жирового слоя (у худощавых пациентов введение препарата осуществляется под углом 45°, у пациентов с толщиной кожной складки более 1,5 см допустимо введение под углом 90°).
8. Одним быстрым движением полностью ввести иглу в кожную складку.
9. После введения иглы отпустить складку кожи.
10. Ввести весь раствор медленным постоянным надавливанием на поршень шприца в течение 2–5 с.
11. Когда шприц будет пустым, вынуть иглу из кожи под тем же углом.
12. Кусочком марли слегка прижать область инъекции в течение 10 с, но ни в коем случае не тереть поверхность. Из места инъекции может выделиться небольшое количество крови. При желании можно воспользоваться пластырем.
13. После инъекции шприц повторно не использовать.
14. Вторую инъекцию препарата ИЛСИРА® для достижения общей дозы 324 мг выполнить аналогичным образом.
15. При последующих инъекциях следует менять место введения.
Утилизация расходного материала
Неиспользованный раствор препарата, использованные шприцы, салфетки/ватные тампоны и другие расходные материалы подлежат утилизации с применением закрывающегося контейнера, устойчивого к проколам для острых предметов из пластика или стекла. Не допускайть хранения использованных шприцев в местах, доступных для детей.
Побочные действия
Реклама: ООО «РЛС-Патент», ИНН 5044031277
В рамках проведенных клинических исследований у здоровых добровольцев, пациентов с ревматоидным артритом и тяжелым течением новой коронавирусной инфекции (COVID-19) препарат ИЛСИРА® показал благоприятный профиль безопасности. Наиболее частыми нежелательными реакциями в проведенных клинических исследованиях были повышение активности АЛТ и АСТ, нейтропения и повышение уровня липидов в крови. Спектр зарегистрированных нежелательных явлений, связанных с применением препарата ИЛСИРА®, был ожидаемым для класса ингибиторов рецепторов ИЛ-6. Летальных исходов, связанных с терапией препаратом ИЛСИРА®, в ходе клинических исследований не было.
В данной инструкции нежелательные реакции представлены в соответствии с международным словарем нежелательных реакций MedDRA. Ниже приведен перечень нежелательных реакций, зарегистрированных у пациентов, получавших левилимаб в рамках клинических исследований, и имеющих определенную, вероятную или возможную степень связи с приемом препарата. Частота указана с учетом следующих критериев: очень часто (≥1/10); часто (от ≥1/100 до <1/10); нечасто (от ≥1/1000 до <1/100); редко (от ≥1/10000 до <1/1000); очень редко (≤10000).
Таблица 4
| Системно-органный класс | Частота | Наименование реакции |
| Инфекции и инвазии | Нечасто | Вирусные инфекции дыхательных путей, пневмония, обострение хронического тонзиллита, латентный туберкулез, туберкулез легких |
| Со стороны крови и лимфатической системы | Часто | Нейтропения, лейкопения, лимфопения |
| Нечасто | Тромбоцитопения | |
| Общие нарушения и реакции в месте введения | Часто | Реакции в месте введения* |
| Нечасто | Гиперчувствительность в месте инъекции | |
| Со стороны печени и желчевыводящих путей | Нечасто | Токсический гепатит** |
| Со стороны сосудов | Нечасто | Повышение АД, в т.ч. изолированное повышение АД |
| Лабораторные и инструментальные данные | Очень часто | Повышение уровня АЛТ, АСТ |
| Часто | Повышение уровня Хс и триглицеридов в крови, билирубина, положительный результат анализа высвобождения γ-интерферона | |
| Нечасто | Положительный результат внутрикожного диагностического теста на туберкулез, увеличение веса |
* В клинических исследованиях регистрировались местные реакции в виде эритемы и кожного зуда.
** Данная нежелательная реакция проявлялась повышением АСТ и АЛТ и не сопровождалось другими симптомами токсического гепатита на фоне множественной лекарственной терапии.
Также в ходе клинических испытаний регистрировались единичные нежелательные явления, для которых в настоящее время связь с применением левилимаба не установлена достоверно: воспаление очага кожного поражения, анемия, лимфаденит, лимфоцитоз, повышение уровня глюкозы в крови, отклонение от нормы при процедуре визуализации легких, снижение уровня АСТ.
С учетом известного профиля безопасности препаратов класса ингибиторов рецепторов ИЛ-6, в качестве нарушений со стороны иммунной системы возможны реакции гиперчувствительности, несмотря на то что во время клинических исследований препарата левилимаб реакции гиперчувствительности зарегистрированы не были.
Взаимодействие
Сведений о наличии неблагоприятных лекарственных взаимодействий левилимаба с другими лекарственными препаратами до настоящего времени не получено.
Смешивание препарата с другими ЛС строго запрещено.
Передозировка
Симптомы: клинические данные о передозировке препарата ИЛСИРА® отсутствуют. Максимальная переносимая доза левилимаба для человека не установлена. В клинических исследованиях при п/к введении левилимаба в максимальной суточной дозе 324 мг двухкратно с интервалом 48–96 ч новых нежелательных реакций, изменяющих представление о профиле безопасности препарата, не зарегистрировано.
Лечение: симптоматическое. Специфический антидот отсутствует.
Особые указания
Серьезные инфекции
Наличие таких потенциально тяжелых инфекций, как ВИЧ, активный гепатит В, сифилис, туберкулез, относится к противопоказаниям для назначения левилимаба. Левилимаб не следует применять у пациентов с активным течением инфекционных заболеваний, включая локализованные инфекции. Учитывая иммуносупрессивное действие левилимаба, терапия этим препаратом потенциально может приводить к обострению хронических инфекций и повышению риска первичного инфицирования.
При реактивации гепатита В или развитии серьезных инфекций терапия левилимабом должна быть прекращена и назначена соответствующая этиотропная терапия.
Соблюдение осторожности требуется в отношении пациентов с рецидивирующими инфекционными заболеваниями в анамнезе, а также лиц, имеющих факторы риска развития инфекций в виде сопутствующих заболеваний или сопутствующей терапии.
С учетом подавления левилимабом реакций острой фазы воспаления, симптомы инфекционного заболевания могут быть стерты, что следует учитывать при раннем выявлении серьезных инфекций у пациентов, получающих препарат ИЛСИРА®. При появлении любых симптомов, свидетельствующих о развитии инфекционного заболевания на фоне применения левилимаба, пациенту следует немедленно обратиться к врачу для своевременной диагностики и назначения терапии.
Туберкулез
Пациентам с активным туберкулезом терапия препаратом ИЛСИРА® противопоказана. Перед назначением препарата ИЛСИРА® и в ходе терапии необходимо проводить стандартный скрининг на туберкулез. Пациентам с латентным туберкулезом рекомендуется пройти стандартный курс противотуберкулезной терапии перед началом терапии препаратом ИЛСИРА®.
Лабораторные показатели
Нейтропения. В клинических исследованиях препарата ИЛСИРА® отмечалось снижение числа нейтрофилов. При длительной терапии пациентов с ревматоидным артритом снижение АЧН не сопровождалось более высокой частотой развития инфекций, в т.ч. серьезных. Следует соблюдать осторожность при лечении препаратом ИЛСИРА® пациентов с АЧН <2·109/л. При снижении АЧН <0,5·109/л терапию препаратом ИЛСИРА® следует отменить. Следует оценивать число нейтрофилов через 4–8 нед после начала терапии, а в дальнейшем в соответствии с клинической практикой.
Тромбоцитопения. В клинических исследованиях препарата ИЛСИРА® отмечалось снижение числа тромбоцитов. При длительной терапии пациентов с ревматоидным артритом снижение числа тромбоцитов не сопровождалось развитием кровотечений. Следует соблюдать осторожность при назначении терапии препаратом ИЛСИРА® при числе тромбоцитов ниже 100·103/мкл. Лечение не рекомендуется при числе тромбоцитов <50·103/мкл. Следует оценивать число тромбоцитов через 4–8 нед после начала терапии, а в дальнейшем в соответствии с клинической практикой.
Ферменты печени. В клинических исследованиях препарата ИЛСИРА® отмечалось повышение активности печеночных трансаминаз без признаков печеночной недостаточности. Частота возникновения подобных изменений может возрастать при совместном использовании с препаратами, обладающими потенциальным гепатотоксическим действием (в т.ч. метотрексат, антибактериальные препараты). Следует соблюдать осторожность при назначении терапии препаратом ИЛСИРА® у пациентов с показателями АЛТ или АСТ, превышающими ВГН более чем в 1,5 раза. Следует оценивать показатели активности печеночных трансаминаз (АЛТ и АСТ) через 4–8 нед после начала терапии, а в дальнейшем в соответствии с клинической практикой.
Изменение показателей липидного обмена. В клинических исследованиях препарата ИЛСИРА® отмечалось повышение концентрации липидов (Хс общий и/или триглицериды). Следует оценивать показатели липидного обмена через 4–8 нед после начала терапии левилимабом, а в дальнейшем в соответствии с клинической практикой. При ведении пациентов с гиперлипидемией следует учитывать национальные рекомендации.
Реакции гиперчувствительности
При использовании левилимаба потенциально возможно развитие реакции гиперчувствительности. В рамках проведенных клинических исследований препарата ИЛСИРА® анафилактических реакций и реакций гиперчувствительности не зарегистрировано. Однако при использовании других ингибиторов рецепторов ИЛ-6 регистрировались крапивница и другие реакции гиперчувствительности, в т.ч. анафилаксия. При возникновении анафилактических или других серьезных аллергических реакций применение препарата ИЛСИРА® следует немедленно прекратить и начать соответствующую симптоматическую терапию.
Наличие алкогольной или наркотической зависимости
Наличие алкогольной или наркотической зависимости, а также психических расстройств может стать причиной несоблюдения пациентом графика лечения левилимабом, что, в свою очередь, может привести к снижению эффективности терапии. Необходимо более тщательное наблюдение за пациентами с указанными состояниями в связи с отсутствием результатов клинических исследований у данной категории пациентов и возможностью повышенного риска развития гепатотоксичности и других неблагоприятных последствий.
Иммуногенность
В ходе клинических исследований препарата ИЛСИРА®, в т.ч. при долгосрочном (в течение года) лечении ревматоидного артрита, выработки связывающих антител к левилимабу выявлено не было.
Особые группы пациентов
Возраст старше 65 лет. Данные об эффективности и безопасности препарата у пациентов старше 65 лет ограничены. Не предполагается наличия существенных возрастных различий в распределении и выведении препарата.
Нарушения функций почек и печени. Эффективность и безопасность препарата у данной категории пациентов не изучались.
Дети. Исследование эффективности и безопасности препарата у детей и лиц моложе 18 лет не проводилось.
Вакцинация
Не следует проводить иммунизацию живыми аттенуированными вакцинами в ходе лечения препаратом ИЛСИРА®, т.к. клиническая оценка безопасности данного взаимодействия в рамках клинических исследований не проводилась. Вакцинация живыми аттенуированными вакцинами до начала терапии препаратом ИЛСИРА®, а также интервал между вакцинацией и началом терапии должны соответствовать действующим клиническим рекомендациям.
Демиелинизирующие заболевания
С учетом данных по профилю безопасности препаратов класса ингибиторов рецепторов ИЛ-6 следует соблюдать осторожность при применении левилимаба у пациентов с демиелинизирующими заболеваниями. Необходимо тщательно контролировать появление симптомов, указывающих на развитие демиелинизирующего заболевания ЦНС, несмотря на то, что способность левилимаба вызывать демиелинизирующие заболевания ЦНС в настоящее время не установлена.
Влияние на способность управлять транспортными средствами и механизмами. Отсутствуют данные о влиянии препарата ИЛСИРА® на способность управлять транспортными средствами и работать с машинами и/или механизмами. Учитывая то, что при терапии другими ингибиторами рецептора ИЛ-6 отмечались эпизоды головокружения, пациентам, испытывающим головокружение при применении препарата ИЛСИРА®, не рекомендуется управлять транспортными средствами и механизмами до тех пор, пока головокружение не прекратится.
Форма выпуска
Раствор для п/к введения, 180 мг/мл. По 0,9 мл в трехкомпонентных стерильных шприцах из бесцветного нейтрального стекла I гидролитического класса. Шприц с одной стороны имеет впаянную иглу для инъекций из нержавеющей стали, которая защищена пластмассовым колпачком с бутилкаучуковым уплотнителем. Шприц укупорен эластичным уплотнителем на поршень и поршнем. На каждый шприц наклеивают самоклеящуюся этикетку. По 1 шприцу в контурной ячейковой упаковке из пленки ПВХ. По 2 и 4 контурных ячейковых упаковки вместе с инструкцией по применению помещают в пачку из картона.
Пачку дополнительно комплектуют спиртовыми салфетками в количестве 2 или 4 шт.
Производитель
АО «БИОКАД», Россия. 198515, Санкт-Петербург, п. Стрельна, ул. Связи, 34, лит. А.
Владелец регистрационного удостоверения. АО «БИОКАД», Россия. 198515, Санкт-Петербург, п. Стрельна, ул. Связи, 38, стр. 1.
Организация, принимающая претензии потребителей. АО «БИОКАД», Россия. 198515, Санкт-Петербург, п. Стрельна, ул. Связи, 34, лит. А.
Тел.: (812) 380-49-33; факс: (812) 380-49-34.
e-mail: biocad@biocad.ru
Информацию о развитии нежелательных реакций направлять по адресу: safety@biocad.ru
Условия отпуска из аптек
По рецепту.
Условия хранения
В защищенном от света месте, при температуре 2–8 °C (не замораживать).
Хранить в недоступном для детей месте.
Срок годности
2 года.
Не применять по истечении срока годности, указанного на упаковке.
Описание проверено
-
Крылов Юрий Федорович
(фармаколог, доктор медицинских наук, профессор, академик Международной академии информатизации)
Опыт работы: более 34 лет
Аналоги по действующему веществу не найдены.
Инспра — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛСР-004052/10
Торговое наименование препарата:
Инспра®
Международное непатентованное наименование:
эплеренон
Лекарственная форма:
таблетки, покрытые пленочной оболочкой
Состав:
1 таблетка содержит:
активное вещество: эплеренон 25 мг или 50 мг;
вспомогательные вещества: лактозы моногидрат 35,700/ 71,400 мг, целлюлоза микрокристаллическая 15,375/ 30,750 мг, кроскармеллоза натрия 4,250/ 8,500 мг, гипромеллоза 2,550/ 5,100 мг, натрия лаурилсульфат 0,850/ 1,700 мг, тальк 0.850/ 1,700 мг, магния стеарат 0,425/ 0.850 мг;
пленочная оболочка: Опадрай желтый YS-1-12524-А 3,825/ 5,10 мг [гипромеллоза, титана диоксид, макрогол, полисорбат-80, краситель железа оксид желтый, краситель железа оксид красный].
Описание:
таблетки 25 мг: таблетки ромбовидной формы, покрытые пленочной оболочкой, от светло-желтого до желтого цвета, с надписью «NSR» над цифрой «25» на одной стороне и «Pfizer» на другой стороне;
таблетки 50 мг: таблетки ромбовидной формы, покрытые пленочной оболочкой, от светло-желтого до желтого цвета, с надписью «NSR» над цифрой «50» на одной стороне и «Pfizer» на другой стороне.
Фармакотерапевтическая группа:
диуретическое калийсберегающее средство.
Код АТХ:
C03DA04
Фармакологические свойства
Фармакодинамика
Эплеренон обладает высокой селективностью в отношении минералокортикоидных рецепторов у человека в отличие от глюкокортикоидных, прогестероновых и андрогенных рецепторов и препятствует связыванию минералокортикоидных с альдостероном -ключевым гормоном ренин-ангиотензин-альдостероновой системы (РААС), который участвует в регуляции артериального давления (АД) и патогенезе сердечно-сосудистых заболеваний.
Эплеренон вызывает стойкое увеличение активности ренина в плазме крови и альдостерона в сыворотке крови. Впоследствии, секреция ренина подавляется альдостероном по механизму обратной связи. При этом повышение активности ренина или концентрации циркулирующего альдостерона не влияет на эффекты эплеренона.
Эффективность эплеренона изучали в двойном слепом плацебоконтролируемом исследовании EPHESUS (Eplerenone Postacute myocardial infarction Heart failure Efficacy and Survival Study) у 6632 больных с острым инфарктом миокарда (ИМ), дисфункцией левого желудочка (ЛЖ) (фракция выброса (ФВ)<40%) и с клиническими признаками сердечной недостаточности. В течение 3-14 дней (в среднем 7 дней) после острого инфаркта миокарда больным назначали эплеренон или плацебо в дополнение к стандартной терапии. Лечение начинали с дозы 25 мг один раз в сутки и к концу 4 недели увеличивали до 50 мг один раз в сутки, если содержание калия в сыворотке крови оставалось менее 5,0 ммоль/л. Во время исследования пациенты получали стандартную терапию с применением ацетилсалициловой кислоты (92%), ингибиторов ангиогензин-превращающего фермента (АИФ) (90%), бета-адреноблокаторов (83%), нитратов (72%), «петлевых» диуретиков (66%) или ингибиторов 3-гидрокси-3-метилглутарилкоэнзим А редуктазы (ГМГ КоА-редуктазы) (60%).
Первичной конечной точкой в исследовании была общая смертность, а комбинированной конечной точкой — смертность или госпитализации по поводу сердечно-сосудистых заболеваний. В результате терапии эплереноном риск общей смертности был снижен на 15% (относительный риск 0,85; 95% доверительный интервал (ДИ), 0,75-0,96; р=0,008) по сравнению с плацебо, главным образом за счет снижения смертности в результате сердечно-сосудистых заболеваний. Риск летального исхода или госпитализации по поводу сердечно-сосудистых заболеваний при применении эплеренона был снижен на 13% (относительный риск 0.87; 95% ДИ, 0,79-0,95; р=0,002). Снижение абсолютного риска для двух конечных точек — общей смертности и смертности/госпитализации по поводу сердечно-сосудистых заболеваний — составило 2,3 и 3,3% соответственно.
В клиническое исследование EMPHASIS-HF (Eplerenone in Mild Patients Hospitalization And Survival Study in Heart Failure) были включены 2 737 пациентов с хронической сердечной недостаточностью (ХСН) II функционального класса (ФК) по классификации NYHA (New York Heart Association) и выраженной систолической дисфункцией (среднее значение ФВ ЛЖ в исследовании составило 26,1%). Средний период наблюдения — 21 месяц. В группе активного лечения эплереноном перед включением пациенты принимали ингибиторы АПФ или блокаторы рецепторов к ангиотензину II (94%), бета-адреноблокаторы (86,6%). Первичная конечная точка: смерть от сердечно-сосудистых причин или госпитализация по поводу сердечной недостаточности (СП). Клиническое исследование EMPHASIS-HF продемонстрировало, что применение эплеренона в средней дозе 39,1±13,8 мг/сут (25-50 мг) у пациентов с ХСН II ФК по классификации NYIIA снижает смертность, связанную с сердечно-сосудистыми заболеваниями на 37% (р<0,001). Клиническая эффективность была продемонстрирована, главным образом, при применении эплеренона у пациентов в возрасте до 75 лет.
Эффективность терапии у пациентов в возрасте старше 75 лет не изучалась.
Электрокардиография
В исследованиях по изучению динамики электрокардиограммы (ЭКГ) у здоровых добровольцев существенного влияния эплеренона на частоту сердечных сокращений (ЧСС), длительность интервалов QRS, PR или QT не выявлено.
Фармакокинетика
Всасывание и распределение
Абсолютная биодоступность эплеренона составляет 69% после приема 100 мг эплеренона внутрь в виде таблеток. Максимальная концентрация в плазме крови (Сmах) достигается примерно через 1,5-2 часа. Сmах и площадь под кривой «концентрация-время» (AUC) линейно зависят от дозы в диапазоне от 10 до 100 мг и нелинейно — в дозе более 100 мг.
Равновесное состояние достигается в течение 2 дней. Прием пищи не влияет на абсорбцию.
Эплеренон примерно на 50 % связывается с белками плазмы крови, преимущественно с альфа1-кислотной группой гликопротеинов. Расчетный объем распределения в равновесном состоянии составляет 42-90 л. Эплеренон не связывается с эритроцитами.
Метаболизм и выведение
Метаболизм эплеренона осуществляется, в основном, под действием изофермента CYP3A4. Активные метаболиты эплеренона в плазме крови не идентифицированы.
В неизмененном виде через почки и кишечник выводится менее 5% дозы эплеренона.
После однократного приема внутрь меченного эплеренона, около 32% дозы выводилось через кишечник и около 67% — через почки. Период полувыведения эплеренона составляет около 3-6 часов, клиренс из плазмы крови — примерно 10 л/ч.
Особые группы
Возраст, пол и раса: фармакокинетика эплеренона в дозе 100 мг один раз в сутки изучалась у пожилых пациентов (старше 65 лет), мужчин и женщин. Фармакокинетика эплеренона существенно не отличалась у мужчин и женщин. В равновесном состоянии у пожилых пациентов Сmах и AUC были соответственно на 22% и 45% выше, чем у молодых пациентов (18-45 лет).
Почечная недостаточность
Фармакокинетику эплеренона изучали у больных с почечной недостаточностью различной степени тяжести и у пациентов, находящихся на гемодиализе. По сравнению с пациентами контрольной группы у больных с тяжелой почечной недостаточностью выявили увеличение равновесных AUC и Сmах на 38% и 24% соответственно, а у больных, находящихся на гемодиализе — их снижение на 26% и 3%. Корреляции между клиренсом эплеренона из плазмы крови и клиренсом креатинина не обнаружено. Эплеренон не удаляется при гемодиализе.
Печеночная недостаточность
Фармакокинетику эплеренона в дозе 400 мг сравнивали у больных с умеренным нарушением функции печени (7-9 баллов по классификации Чайлд-Пью) и здоровых добровольцев. Равновесные Сmах и AUC эплеренона были увеличены на 3,6% и 42% соответственно. У больных с тяжелой печеночной недостаточностью эплеренон не изучался, поэтому его применение в этой группе больных не показано.
Сердечная недостаточность
Фармакокинетику эплеренона в дозе 50 мг изучали у больных с сердечной недостаточностью (II-IV ФК). Равновесные AUC и Сmах у больных с сердечной недостаточностью были соответственно на 38 и 30% выше, чем у здоровых добровольцев, подобранных по возрасту, массе тела и иолу. Клиренс эплеренона у больных с сердечной недостаточностью сходен с таковым у здоровых пожилых людей.
Показания к применению
- Инфаркт миокарда: в дополнение к стандартной терапии, с целью снижения риска сердечно-сосудистой смертности и заболеваемости у пациентов со стабильной дисфункцией левого желудочка (фракция выброса <40 %) и клиническими признаками сердечной недостаточности после перенесенного инфаркта миокарда.
- Хроническая сердечная недостаточность: в дополнение к стандартной терапии, с целью снижения риска сердечно-сосудистой смертности и заболеваемости у пациентов с хронической сердечной недостаточностью II функционального класса по классификации NYHA, при дисфункции левого желудочка (фракция выброса<35%).
Противопоказания
- повышенная чувствительность к эплеренону или другим компонентам препарата;
- клинически значимая гиперкалиемия;
- содержание калия в сыворотке крови в начале лечения >5,0 ммоль/л;
- тяжелая почечная недостаточность (клиренс креатинина (КК)< 30 мл/мин);
- тяжелая печеночная недостаточность (более 9 баллов по классификации Чайлд-Пью);
- одновременный прием калийсберегающих диуретиков или мощных ингибиторов изофермента CYP3A4. например, итраконазола, кетоконазола, ритонавира, нелфинавира, кларитромицина, телитромицина и нефазодона (см. раздел «Взаимодействие с другими лекарственными средствами»);
- редкие наследственные заболевания, такие как непереносимость лактозы, дефицит лактазы и синдром мальабсорбции глюкозы-галактозы (см. раздел «Особые указания»);
- опыта применения препарата у детей в возрасте до 18 лет нет, поэтому его назначение пациентам этой возрастной группы не рекомендуется.
С осторожностью
- сахарный диабет 2 типа и микроальбуминурия (см. раздел «Особые указания»);
- пожилой возраст;
- нарушения функции почек (КК<50 мл/мин);
- одновременное применение эплеренона и
- ингибиторов АПФ или антагонистов рецепторов ангиотензина II;
- сильных индукторов изофермента CYP3A4;
- препаратов, содержащих литий;
- циклоспорина или гакролимуса;
- дигоксина и варфарина в дозах, близких к максимальным терапевтическим
(см. разделы «Особые указания» и «Взаимодействие с другими лекарственными средствами»).
Не следует применять тройную комбинацию ингибитора АПФ и антагонистов рецепторов ангиотензина II с эплереноном.
Применение при беременности и в период грудного вскармливания
Сведений о применении препарата у беременных нет. Препарат следует применять с осторожностью и только в тех случаях, когда ожидаемая польза для матери значительно превышает возможный риск для плода/ребенка.
Сведений о выведении эплеренона после приема внутрь с грудным молоком нет. Возможные нежелательные эффекты эплеренона на новорожденных, находящихся на грудном вскармливании, неизвестны, поэтому целесообразно или прекратить кормление грудью, или отменить препарат, в зависимости от его важности для матери.
Способ применения и дозы
Внутрь.
Прием пищи не влияет на всасывание препарата Инспра® Для индивидуального подбора дозы можно применять дозировки 25 и 50 мг.
Инфаркт миокарда
Лечение следует начинать с дозы 25 мг один раз в сутки и увеличивать ее до 50 мг один раз в сутки через 4 недели с учетом содержания калия в сыворотке крови (см. табл. 1). Рекомендуемая поддерживающая доза препарата составляет 50 мг один раз в сутки.
Хроническая сердечная недостаточность II функционального класса по классификации NYHA
Лечение также следует начинать с дозы 25 мг один раз в сутки и увеличивать ее до 50 мг один раз в сутки через 4 недели с учетом содержания калия в сыворотке крови (см. табл. 1).
Максимальная суточная доза составляет 50 мг. После временного прекращения приема препарата в связи с повышением содержания калия в сыворотке крови до или более 6,0 ммоль/л, терапию препаратом можно возобновить в дозе 25 мг через день, когда содержание калия в сыворотке крови составит <5,0 ммоль/л.
Общие рекомендации
Содержание калия в сыворотке крови следует определять до назначения препарата Инспра® в течение первой недели и через 1 месяц после начала терапии или при изменении дозы препарата. В дальнейшем также необходимо периодически контролировать содержание калия в сыворотке крови.
Пожилые пациенты
Коррекции начальной дозы у пожилых пациентов не требуется. В связи с возрастным снижением функции почек у пожилых пациентов повышается риск развития гиперкалиемии, особенно при наличии сопутствующих заболеваний, способствующих увеличению концентраций эплеренона в сыворотке крови, в частности при нарушении функции печени от легкой до умеренной степени тяжести. Рекомендуется периодически определять содержание калия в сыворотке крови (см. табл. №1, а также разделы «Особые указания», «С осторожностью»).
Нарушение функции почек
Коррекции начальной дозы у больных с легкими нарушениями функции почек не требуется. Степень гиперкалиемии увеличивается при ухудшении функции почек.
Рекомендуется периодически определять содержание калия в сыворотке крови (см. табл. №1, а также раздел «Особые указания»). Препарат Инспра® не удаляется при гемодиализе. У пациентов с ХСН II ФК по классификации NYHA и нарушениями функции почек средней степени тяжести (КК 30-60 мл/мин) следует начинать терапию с дозы 25 мг через день с последующей коррекцией дозы в зависимости от содержания калия в сыворотке крови (см. табл. №1).
У пациентов с тяжелой недостаточностью функции почек (КК<30 мл/мин) применение препарата противопоказано (см. раздел «Противопоказания»).
Опыта применения препарата Инспра® у пациентов с сердечной недостаточностью после перенесенного инфаркта миокарда и КК<50 мл/мин нет. Следует с осторожностью применять препарат Инспра® у таких пациентов (см. раздел «С осторожностью»).
У пациентов с КК<50 мл/мин применение препарата Инспра® в дозе выше 25 мг один раз в сутки не исследовалось (также см. раздели «Особые указания»).
Нарушение функции печени
Коррекции начальной дозы у больных с нарушениями функции печени от легкой до умеренной степени тяжести не требуется. Учитывая увеличение концентрации эплеренона у таких больных, рекомендуется регулярно контролировать содержание калия в сыворотке крови, особенно у пожилых пациентов (см. раздел «Особые указания»). Применение препарата Инспра® у пациентов с тяжелыми нарушениями функции печени противопоказано (см. раздел «Противопоказания»).
Сопутствующая терапия
При одновременном применении препаратов, оказывающих слабое или умеренно выраженное ингибирующее действие на изофермент CYP3A4, например, эритромицина, саквинавира, амиодарона, дилтиазема, верапамила и флуконазола, лечение препаратом Инспра® следует проводить в дозе 25 мг один раз в сутки(см. раздел «Взаимодействие с другими лекарственными средствами»).
Таблица 1. Подбор дозы после начала лечения
| Содержание калия в сыворотке крови (ммоль/л) |
Действие | Изменение дозы |
| <5,0 | Увеличение дозы | с 25 мг через день до 25 мг один раз в сутки с 25 мг один раз в сутки до 50 мг один раз в сутки |
| 5,0-5,4 | Поддерживающая доза | доза остается прежней |
| 5,5-5,9 | Снижение дозы | с 50 мг один раз в сутки до 25 мг один раз в сутки с 25 мг один раз в сутки до 25 мг через день с 25 мг через день — временная отмена препарата |
| >6,0 | Отмена препарата | Не применимо |
Побочное действие
Ниже перечислены нежелательные явления, которые могли быть связаны с лечением, а также серьезные нежелательные явления, частота которых сопоставима с частотой нежелательных и серьезных нежелательных явлений в группе плацебо. Нежелательные явления распределены по системам организма и частоте: часто >1/100, < 1/10; нечасто >1/1000, <1/100; частота неизвестна (не может быть подсчитана по имеющимся данным).
Со стороны системы кроветворения и лимфатической системы
Нечасто: эозинофилия.
Нарушения метаболизма и питания
Часто: гиперкалиемия, гипертриглицеридемия, дегидратация, гиперхолестеринемия.
Нечасто: гипонатриемия, гипотиреоз.
Психические расстройства
Нечасто: бессонница.
Неврологические нарушения
Часто: обморок, головокружение.
Нечасто: головная боль, гипестезия.
Со стороны сердца
Часто: инфаркт миокарда.
Нечасто: левожелудочковая недостаточность, фибрилляция предсердий, тахикардия.
Сосудистые нарушения
Часто: выраженное снижение АД.
Нечасто: ортостатическая гипотензия, тромбоз артерий нижних конечностей.
Со стороны системы дыхания, грудной клетки и средостения
Часто: кашель.
Нечасто: фарингит.
Со стороны желудочно-кишечного тракта
Часто: диарея, тошнота, запор.
Нечасто: метеоризм, рвота.
Со стороны печени и желчевыводящих путей
Нечасто: холецистит.
Со стороны кожных покровов и подкожно-жировой клетчатки
Часто: кожный зуд.
Нечасто: повышенное потоотделение, сыпь.
Частота неизвестна: ангионевротический отек.
Со стороны опорно-двигательного аппарата и соединительной ткани
Часто: судороги в икроножных мышцах ног, мышечно-скелетные боли.
Нечасто: боль в спине.
Со стороны почек и мочевыводящих путей
Часто: нарушение функции почек.
Общие и местные
Нечасто: астения, недомогание.
Лабораторные показатели
Нечасто: повышение концентрации остаточного азота мочевины, креатинина, снижение экспрессии рецептора эпидермального фактора роста, повышение концентрации глюкозы в сыворотке крови.
Инфекции
Нечасто: пиелонефрит, гинекомастия.
Передозировка
Случаев передозировки эплеренона у человека не описано.
Симптомы: наиболее вероятными проявлениями передозировки могут быть выраженное снижение АД и гиперкалиемия.
Лечение: при развитии выраженного снижения АД необходимо назначить поддерживающее лечение. В случае развития гиперкалиемии показана стандартная терапия. Эплеренон не удаляется при гемодиализе. Установлено, что эплеренон активно связывается с активированным углем.
Взаимодействие с другими лекарственными средствами
Фармакодинамические взаимодействия
Калийсберегающие диуретики и препараты калия:
учитывая повышенный риск развития гиперкалиемии, эплеренон не следует назначать больным, получающим калийсберегающие диуретики и препараты калия (см. раздел «Противопоказания»). Калийсберегающие диуретики могут усилить эффекты гипотензивных средств и других диуретиков.
Препараты, содержащие литий: взаимодействие эплеренона с препаратами лития не изучалось. Однако, у больных, получавших препараты лития в сочетании с диуретиками и ингибиторами АПФ, описаны случаи повышения концентрации и интоксикации литием.
Если подобная комбинация необходима, целесообразно контролировать концентрации лития в плазме крови (см. раздел «Особые указания»).
Циклоспорин, такролимус: циклоспорин и такролимус могут вызвать нарушение функции почек и повысить риск развития гиперкалиемии. Следует избегать одновременного применения эплеренона и циклоспорина или такролимуса. Если во время лечения эплереноном потребуется назначение циклоспорина или такролимуса, рекомендуется тщательно контролировать содержание калия в сыворотке крови и функцию почек (см. раздел «Особые указания»).
Нестероидные противовоспалительные препараты (НПВП): лечение НПВП может привести к острой почечной недостаточности за счет прямого подавления клубочковой фильтрации, особенно у больных группы риска (пожилые пациенты и/или пациенты с дегидратацией). При совместном применении этих средств до начала и во время лечения необходимо обеспечивать адекватный водный режим и контролировать функцию почек.
Триметоприм: одновременное применение триметоприма с эплереноном повышает риск развития гиперкалиемии. Рекомендуется контролировать содержание калия в сыворотке крови и функцию почек, особенно у больных с почечной недостаточностью и у пожилых пациентов.
Ингибиторы АПФ и антагонисты рецепторов ангиотензина II: при применении эплеренона с ингибиторами АПФ или антагонистами рецепторов ангиотензина II следует тщательно контролировать содержание калия сыворотки крови. Подобная комбинация может привести к увеличению риска развития гиперкалиемии, особенно у пациентов с нарушением функции почек, в т.ч. у пожилых пациентов. Не следует применять тройную комбинацию ингибитора АИФ и антагонистов рецепторов ангиотензина II с эплереноном.
Альфа I-адреноблокаторы (празозин, альфузозин): при одновременном применении альфа1-адреноблокаторов с эплереноном может усилиться антигипертензивное действие и/или увеличиться риск развития ортостатической гипотензии, в связи с чем, рекомендуется контроль АД, особенно при изменении положения тела.
Трициклические антидепрессанты. нейролептики, амифостин, баклофен: при одновременном применении этих средств с эплереноном может усилиться антигипертензивный эффект или увеличиться риск развития ортостатической гипотензии.
Глюкокортикоиды, тетракозактид: одновременное применение этих средств с эплереноном может привести к задержке натрия и жидкости.
Фармакокинетические взаимодействия
Исследования in vitro свидетельствуют о том, что эплеренон не ингибирует изоферменты CYP1A2, CYP2C19, CYP2C9, CYP2D6 или CYP3A4. Эплеренон не является субстратом или ингибитором гликопротеина Р.
Дигоксин: AUC дигоксина при одновременном применении с эплереноном увеличивается на 16% (90% ДИ: 4% — 30%). Необходимо соблюдать осторожность, если дигоксин применяется в дозах, близких к максимальным терапевтическим.
Варфарин: клинически значимого фармакокинетического взаимодействия с варфарином не выявлено. Необходимо соблюдать осторожность, если варфарин применяется в дозах, близких к максимальным терапевтическим.
Субстраты изофермента CYP3A4: в специальных исследованиях признаков фармакокинетического взаимодействия эплеренона с субстратами изофермента CYP3A4, например, мидазоламом и цизапридом, выявлено не было.
Ингибиторы изофермента CYP3A4
Сильные ингибиторы изофермента CYP3A4: при применении эплеренона со средствами, ингибирующими изофермент CYP3A4, возможно значимое фармакокинетическое взаимодействие. Сильный ингибитор изофермента CYP3A4 (кетоконазол 200 мг два раза в сутки) вызывал увеличение AUC эплеренона на 441%. Одновременное применение эплеренона с сильными ингибиторами изофермента CYP3A4, такими как кетоконазол, итраконазол, ригонавир, нелфинавир, кларитромицин, телитромицин и нефазадон, противопоказано (см. раздел «Противопоказания»).
Слабые и умеренные ингибиторы изофермента CYP3A4: одновременное применение с эритромицином, саквинавиром, амиодароном, дилтиаземом. верапамилом и флуконазолом сопровождалось значимым фармакокинетическим взаимодействием (степень увеличения AUC варьировала от 98% до 187%). При одновременном применении этих средств с эплереноном доза последнего не должна превышать 25 мг в сутки (см. раздел «Способ применения и дозы»).
Индукторы изофермента CYP3A4
Одновременный прием препаратов, содержащих Зверобой продырявленный (St John’s Wort, сильный индуктор изофермента CYP3A4) с эплереноном вызывал снижение AUC последнего на 30%. При применении более сильных индукторов изофермента CYP3A4, таких как рифампицин, возможно более выраженное снижение AUC эплеренона.
Учитывая возможное снижение эффективности эплеренона, одновременное применение сильных индукторов изофермента CYP3A4 (рифампицина, карбамазепина, фенитоина, фенобарбитала, препаратов, содержащих Зверобой продырявленный) не рекомендуется (см. раздел «Особые указания»),
Антациды: на основании фармакокинетического клинического исследования значительного взаимодействия антацидов с эплереноном при их одновременном применении не предполагается.
Особые указания
Гиперкалиемия
При лечении препаратом Инспра® может развиться гиперкалиемия, которая обусловлена его механизмом действия. В начале лечения и при изменении дозы препарата у всех пациентов следует контролировать содержание калия в сыворотке крови. В дальнейшем периодический контроль содержания калия рекомендуется проводить пациентам с повышенным риском развития гиперкалиемии, например, пожилым, больным с почечной недостаточностью (см. раздел «Способ применения и дозы») и сахарным диабетом. Учитывая повышенный риск развития гиперкалиемии, назначение препаратов калия после начала лечения эплереноном не рекомендуется. Снижение дозы препарата Инспра® приводит к снижению содержания калия в сыворотке крови. В одном исследовании добавление гидрохлоротиазида к эплеренону препятствовало увеличению содержания калия в сыворотке крови.
Нарушение функции почек
У пациентов с нарушениями функции почек, в том числе диабетической микроальбуминурией, рекомендуется регулярно контролировать содержание калия в сыворотке крови. Риск развития гиперкалиемии увеличивается при снижении функции почек. Хотя число больных сахарным диабетом 2 типа и микроальбуминурией в исследованиях было ограниченным, тем не менее, в этой небольшой выборке было отмечено увеличение частоты гиперкалиемии (см. раздел «С осторожностью»). В связи с этим у таких больных лечение следует проводить с осторожностью. Препарат Инспра® не удаляется при гемодиализе. Применение препарата Инспра® противопоказано при тяжелой почечной недостаточности (см. раздел «Противопоказания»).
Нарушение функции печени
У больных с легкими или умеренными нарушениями функции печени (5-6 и 7-9 баллов по классификации Чайлд-Пью) увеличения содержания калия в сыворотке крови более 5,5 ммоль/л выявлено не было. В связи с повышенной экспозицией эплеренона у пациентов с легкими или умеренными нарушениями функции печени следует проводить частый и регулярный контроль содержания калия в сыворотке крови, особенно у пожилых пациентов. У больных с тяжелыми нарушениями функции печени эплеренон не изучался, поэтому его применение противопоказано (см. раздел «Противопоказания»).
Индукторы изофермента CYP3A4
Одновременное применение препарата Инспра® с сильными индукторами изофермента CYP3A4 не рекомендуется (см. раздел «Взаимодействие с другими лекарственными средствами»).
Циклоспорин, такролимус, препараты, содержащие литий
Во время лечения препаратом Инспра® следует избегать применения этих средств (см. раздел «Взаимодействие с другими лекарственными средствами»).
Лактоза
Таблетки препарата Инспра® содержат лактозу, поэтому их не следует назначать больным с редкими наследственными заболеваниями, такими как непереносимость лактозы, дефицит лактазы и синдром мальабсорбции глюкозы-галактозы.
Влияние па способность управлять автотранспортом и пользоваться техникой
Эффекты препарата Инспра® на способность управлять автотранспортом или пользоваться техникой не изучались. Однако, учитывая возможность препарата вызывать головокружения и обморочные состояния, следует соблюдать осторожность при управлении автотранспортом или пользовании техникой на фоне приема препарата Инспра®
Форма выпуска
Таблетки, покрытые пленочной оболочкой 25 мг или 50 мг.
По 14 таблеток в блистере из ПBX/A1 — фольги; но 2 блистера вместе с инструкцией по применению помещают в картонную пачку с контролем первого вскрытия.
По 10 таблеток в блистере ПВХ/А1 — фольги; по 2, 3, 5. 10 или 20 блистеров вместе с инструкцией по применению помещают в картонную пачку с контролем первого вскрытия.
Условия хранения
При температуре не выше 30°С.
Хранить в недоступном для детей месте.
Срок годности
3 года
Не использовать по истечении срока годности, указанного на упаковке.
Условия отпуска
Отпускается по рецепту
Производитель
«Неолфарма, Инк.», Пуэрто-Рико
Адрес: Яардинес Стрит № 99, Кагуас 00725, Пуэрто-Рико
«Пфайзер Фармасьютикалз ЭлЭлСи», Пуэрто-Рико 1,9 км №689, Вега Байя, Пуэрто-Рико 00693
Выпускающий контроль качества:
Фарева Амбуаз, Зон Эндюстриэль, 29 рут дез Эндюстри, 37530 Посэ Сюр Сис, Франция
Претензии потребителей направлять по адресу ООО «Пфайзер»:
123112 Москва, Пресненская наб., д. 10
БЦ «Башня на Набережной» (Блок С)
Купить Инспра в ГорЗдрав
Купить Инспра в megapteka.ru
Купить Инспра в Планета Здоровья
*Цены в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Состав
Активное вещество: эплеренон 25 мг.
Вспомогательные вещества: лактозы моногидрат — 35.7 мг, целлюлоза микрокристаллическая — 15.375 мг, натрия кроскармеллоза — 4.25 мг, гипромеллоза — 2.55 мг, натрия лаурилсульфат — 0.85 мг, тальк — 0.85 мг, магния стеарат — 0.425 мг.
Состав пленочной оболочки: опадрай желтый YS-1-12524-A — 3.825 мг (гипромеллоза, титана диоксид, макрогол, полисорбат 80, краситель железа оксид желтый, краситель железа оксид красный).
Фармакокинетика
Всасывание и распределение
Абсолютная биодоступность эплеренона составляет 69% после приема 100 мг эплеренона внутрь в виде таблеток. Сmax в плазме крови достигается примерно через 1.5-2 ч. Сmax и AUC линейно зависят от дозы в диапазоне от 10 до 100 мг и нелинейно — в дозе более 100 мг. Равновесное состояние достигается в течение 2 дней. Прием пищи не влияет на абсорбцию.
Эплеренон примерно на 50% связывается с белками плазмы крови, преимущественно с альфа1-кислотной группой гликопротеинов. Расчетный Vd в равновесном состоянии составляет 42-90 л. Эплеренон не связывается с эритроцитами.
Метаболизм и выведение
Метаболизм эплеренона осуществляется, в основном, под действием изофермента СУР3А4. Активные метаболиты эплеренона в плазме крови не идентифицированы.
В неизмененном виде через почки и кишечник выводится менее 5% дозы эплеренона. После однократного приема внутрь меченного эплеренона, около 32% дозы выводилось через кишечник и около 67% — через почки. Т1/2 эплеренона составляет около 3-5 ч, клиренс из плазмы крови — примерно 10 л/ч.
Фармакокинетика у особых групп пациентов
Фармакокинетику эплеренона в дозе 100 мг 1 раз/сут изучали у пожилых пациентов (старше 65 лет), мужчин и женщин. Фармакокинетика эплеренона существенно не отличалась у мужчин и женщин. В равновесном состоянии у пожилых пациентов Сmах и AUC были соответственно на 22% и 45% выше, чем у молодых пациентов (18-45 лет).
Фармакокинетику эплеренона изучали у пациентов с почечной недостаточностью различной степени тяжести и у пациентов, находящихся на гемодиализе. По сравнению с пациентами контрольной группы у пациентов с тяжелой почечной недостаточностью выявили увеличение равновесных AUC и Сmах на 38% и 24% соответственно, а у пациентов, находящихся на гемодиализе — их снижение на 26% и 3%. Корреляции между клиренсом эплеренона из плазмы крови и КК не обнаружено. Эплеренон не удаляется при гемодиализе.
Фармакокинетику эплеренона в дозе 400 мг сравнивали у пациентов с умеренным нарушением функции печени (7-9 баллов по классификации Чайлд-Пью) и здоровых добровольцев. Равновесные Сmах и AUC эплеренона были увеличены на 3.6% и 42% соответственно. У пациентов с тяжелой печеночной недостаточностью эплеренон не изучался, поэтому его применение в этой группе больных не показано.
Фармакокинетику эплеренона в дозе 50 мг изучали у пациентов с сердечной недостаточностью (II-IV ФК). Равновесные AUC и Сmах у пациентов с сердечной недостаточностью были соответственно на 38% и 30% выше, чем у здоровых добровольцев, подобранных по возрасту, массе тела и полу. Клиренс эплеренона у пациентов с сердечной недостаточностью сходен с таковым у здоровых пожилых людей.
Показания к применению
- Инфаркт миокарда: в дополнение к стандартной терапии с целью снижения риска сердечно-сосудистой смертности и заболеваемости у пациентов со стабильной дисфункцией левого желудочка (фракция выброса ≤40%) и клиническими признаками сердечной недостаточности после перенесенного инфаркта миокарда;
- хроническая сердечная недостаточность: в дополнение к стандартной терапии с целью снижения риска сердечно-сосудистой смертности и заболеваемости у пациентов с хронической сердечной недостаточностью II ФК по классификации NYHA, при дисфункции левого желудочка (фракция выброса ≤35%).
Противопоказания
- Клинически значимая гиперкалиемия;
- концентрация калия в сыворотке крови в начале лечения >5 ммоль/л;
- тяжелая почечная недостаточность (КК <30 мл/мин);
- тяжелая печеночная недостаточность (более 9 баллов по шкале Чайлд-Пью);
- одновременный прием калийсберегающих диуретиков или мощных ингибиторов CYP3A4, например, итраконазола, кетоконазола, ритонавира, нелфинавира, кларитромицина, телитромицина и нефазодона;
- редкие наследственные заболевания, такие как непереносимость лактозы, дефицит лактазы и синдром мальабсорбции глюкозы-галактозы;
- детский и подростковый возраст до 18 лет (опыта применения препарата у пациентов данной возрастной группы нет);
- повышенная чувствительность к эплеренону или другим компонентам препарата.
С осторожностью следует назначать препарат при сахарном диабете 2 типа и микроальбуминурии; нарушениях функции почек (КК <50 мл/мин); одновременном применении ингибиторов АПФ или антагонистов рецепторов ангиотензина II, сильных индукторов изофермента CYP3A4, препаратов, содержащих литий, циклоспорина или такролимуса, дигоксина и варфарина в дозах, близких к максимальным терапевтическим; пациентам пожилого возраста.
Не следует применять тройную комбинацию ингибитора АПФ и антагонистов рецепторов ангиотензина II с эплереноном.
Способ применения и дозы
Препарат принимают внутрь. Прием пищи не влияет на всасывание препарата Инспра®.
Для индивидуального подбора дозы можно применять дозировки 25 и 50 мг.
Инфаркт миокарда
Лечение следует начинать с дозы 25 мг 1 раз/сут и увеличивать ее до 50 мг 1 раз/сут в течение 4 недель с учетом концентрации калия в сыворотке крови (см. таблицу). Рекомендуемая поддерживающая доза препарата составляет 50 мг 1 раз/сут.
Хроническая сердечная недостаточность, начиная со II ФК по классификации NYHA
Лечение также следует начинать с дозы 25 мг 1 раз/сут и увеличивать ее до 50 мг 1 раз/сут через 4 недели с учетом концентрации калия в сыворотке крови (см. таблицу).
Максимальная суточная доза составляет 50 мг. После временного прекращения приема препарата в связи с повышением содержания калия в сыворотке крови до 6 ммоль/л или более, терапию препаратом можно возобновить в дозе 25 мг через день, когда содержание калия в сыворотке крови составит <5 ммоль/л.
Общие рекомендации
Содержание калия в сыворотке крови следует определять до назначения препарата Инспра®, в течение первой недели и через 1 месяц после начала терапии или при изменении дозы препарата. В дальнейшем также необходимо периодически контролировать содержание калия в сыворотке крови.
Коррекции начальной дозы у пациентов пожилого возраста не требуется. В связи с возрастным снижением функции почек у пожилых пациентов повышается риск развития гиперкалиемии, особенно при наличии сопутствующих заболеваний, способствующих увеличению концентраций эплеренона в сыворотке крови, в частности при нарушении функции печени от легкой до умеренной степени тяжести. Рекомендуется периодически определять содержание калия в сыворотке крови (см. таблицу).
Коррекции начальной дозы у пациентов с легкими нарушениями функции почек не требуется. Степень гиперкалиемии увеличивается при ухудшении функции почек. Рекомендуется периодически определять содержание калия в сыворотке крови. Препарат Инспра® не удаляется при гемодиализе. У пациентов с ХСН II ФК по классификации NYHA и нарушениями функции почек средней степени тяжести (КК 30-60 мл/мин) следует начинать терапию с дозы 25 мг через день с последующей коррекцией дозы в зависимости от содержания калия в сыворотке крови (см. таблицу). У пациентов с тяжелой недостаточностью функции почек (КК <30 мл/мин) применение препарата противопоказано.
Опыта применения препарата Инспра® у пациентов с сердечной недостаточностью после перенесенного инфаркта миокарда и КК <50 мл/мин нет. Следует с осторожностью применять препарат Инспра® у таких пациентов. У пациентов с КК <50 мл/мин применение препарата Инспра® в дозе выше 25 мг 1 раз/сут не исследовалось.
Коррекции начальной дозы у пациентов с нарушениями функции печени от легкой до умеренной степени тяжести не требуется. Учитывая увеличение концентрации эплеренона у таких пациентов, рекомендуется регулярно контролировать содержание калия в сыворотке крови, особенно у пациентов пожилого возраста. Применение препарата Инспра® у пациентов с тяжелыми нарушениями функции печени противопоказано.
Сопутствующая терапия
При одновременном применении препаратов, оказывающих слабое или умеренно выраженное ингибирующее действие на изофермент CYP3А4 (например, эритромицина, саквинавира, амиодарона, дилтиазема, верапамила и флуконазола), лечение препаратом Инспра® можно начать с дозы 25 мг 1 раз/сут, при этом доза последнего не должна превышать 25 мг 1 раз/сут.
Таблица. Подбор дозы после начала лечения
| Концентрация калия в сыворотке крови (ммоль/л) | Действие | Изменение дозы |
| <5 | Увеличение дозы |
с 25 мг через день до 25 мг 1 раз/сут с 25 мг 1 раз/сут до 50 мг 1 раз/сут |
| 5-5.4 | Поддерживающая доза | Доза остается прежней |
| 5.5-5.9 | Снижение дозы |
с 50 мг 1 раз/сут до 25 мг 1 раз/сут с 25 мг 1 раз/сут до 25 мг через день с 25 мг через день — временная отмена препарата |
| ≥6 | Отмена препарата | Не применимо |
Условия хранения
Препарат следует хранить в недоступном для детей месте при температуре не выше 30°С.
Срок годности
3 года. Не использовать по истечении срока годности, указанного на упаковке.
Особые указания
Гиперкалиемия
При лечении препаратом Инспра® может развиться гиперкалиемия, которая обусловлена его механизмом действия. В начале лечения и при изменении дозы препарата у всех пациентов следует контролировать содержание калия в сыворотке крови. В дальнейшем периодический контроль содержания калия рекомендуется проводить пациентам с повышенным риском развития гиперкалиемии, например, пациентам пожилого возраста, пациентам с почечной недостаточностью и сахарным диабетом. Учитывая повышенный риск развития гиперкалиемии, назначение препаратов калия после начала лечения эплереноном не рекомендуется. Снижение дозы препарата Инспра® приводит к снижению содержания калия в сыворотке крови. В одном исследовании добавление гидрохлоротиазида к эплеренону препятствовало увеличению содержания калия в сыворотке крови.
Нарушение функции почек
У пациентов с нарушениями функции почек, в т.ч. диабетической микроальбуминурией, рекомендуется регулярно контролировать содержание калия в сыворотке крови. Риск развития гиперкалиемии увеличивается при снижении функции почек. Хотя число больных сахарным диабетом 2 типа и микроальбуминурией в исследованиях было ограниченным, тем не менее, в этой небольшой выборке было отмечено увеличение частоты гиперкалиемии. В связи с этим у таких пациентов лечение следует проводить с осторожностью. Препарат Инспра® не удаляется при гемодиализе. Применение препарата Инспра® противопоказано при тяжелой почечной недостаточности.
Нарушение функции печени
У пациентов с легкими или умеренными нарушениями функции печени (5-6 и 7-9 баллов по классификации Чайлд-Пью) не выявлено увеличение содержания калия в сыворотке крови более 5.5 ммоль/л. В связи с повышенной экспозицией эплеренона у пациентов с легкими и умеренными нарушениями функции печени следует проводить частый и регулярный контроль содержания калия в сыворотке крови, особенно у пациентов пожилого возраста. У пациентов с тяжелыми нарушениями функции печени эплеренон не изучался, поэтому его применение противопоказано.
Индукторы изофермента CYP3А4
Одновременное применение препарата Инспра® с сильными индукторами изофермента CYP3А4 не рекомендуется.
Циклоспорин, такролимус, препараты, содержащие литий
Во время лечения препаратом Инспра® следует избегать применения этих средств.
Лактоза
Таблетки препарата Инспра® содержат лактозу, поэтому их не следует назначать пациентам с редкими наследственными заболеваниями, такими как непереносимость лактозы, дефицит лактазы и синдром мальабсорбции глюкозы-галактозы.
Описание
Диуретическое калийсберегающее средство.
Применение у детей
Опыта применения препарата у детей и подростков в возрасте до 18 лет нет, поэтому его назначение пациентам этой возрастной группы не рекомендуется.
Фармакодинамика
Эплеренон обладает высокой селективностью в отношении минералокортикоидных рецепторов у человека в отличие от глюкокортикоидных, прогестероновых и андрогенных рецепторов и препятствует связыванию минералокортикоидных с альдостероном — ключевым гормоном РААС, который участвует в регуляции АД и патогенезе сердечно-сосудистых заболеваний.
Эплеренон вызывает стойкое увеличение активности ренина в плазме крови и альдостерона в сыворотке крови. Впоследствии секреция ренина подавляется альдостероном по механизму обратной связи. При этом повышение активности ренина или концентрации циркулирующего альдостерона не влияет на эффекты эплеренона.
Эффективность эплеренона изучали в двойном слепом плацебо-контролируемом исследовании EPHESUS (Eplerenone Postacute myocardial infarction Heart failure Efficacy and Survival Study) у 6632 больных с острым инфарктом миокарда (ИМ), дисфункцией левого желудочка (ЛЖ) (фракция выброса (ФВ) <40%) и с клиническими признаками сердечной недостаточности. В течение 3-14 дней (в среднем 7 дней) после острого инфаркта миокарда больным назначали эплеренон или плацебо в дополнение к стандартной терапии. Лечение начинали с дозы 25 мг 1 раз/сут и к концу 4 недели увеличивали до 50 мг 1 раз/сут, если содержание калия в сыворотке крови оставалось менее 5 ммоль/л. Во время исследования пациенты получали стандартную терапию с применением ацетилсалициловой кислоты (92%), ингибиторов АПФ (90%), бета-адреноблокаторов (83%), нитратов (72%), «петлевых» диуретиков (66%) или ингибиторов 3-гидрокси-3-метилглутарилкоэнзим А редуктазы (ГМГ-KoA-редуктазы) (60%). Первичной конечной точкой в исследовании была общая смертность, а комбинированной конечной точкой — смертность или госпитализации по поводу сердечно-сосудистых заболеваний. В результате терапии эплереноном риск общей смертности был снижен на 15% (относительный риск 0.85; 95% доверительный интервал (ДИ), 0.75-0.96; р=0.008) по сравнению с плацебо, главным образом за счет снижения смертности в результате сердечно-сосудистых заболеваний. Риск летального исхода или госпитализации по поводу сердечно-сосудистых заболеваний при применении эплеренона был снижен на 13% (относительный риск 0.87; 95% ДИ, 0.79-0.95; р=0.002). Снижение абсолютного риска для двух конечных точек — общей смертности и смертности/госпитализации по поводу сердечно-сосудистых заболеваний — составило 2.3 и 3.3% соответственно.
В клиническое исследование EMPHASIS-HF (Eplerenone in Mild Patients Hospitalization And SurvIval Study in Heart Failure) были включены 2737 пациентов с хронической сердечной недостаточностью (ХСН) II функционального класса (ФК) по классификации NYHA и выраженной систолической дисфункцией (среднее значение ФВ ЛЖ в исследовании составило 26.1%). Средний период наблюдения — 21 месяц. В группе активного лечения эплереноном перед включением пациенты принимали ингибиторы АПФ или антагонисты рецепторов ангиотензина II (94%), бета-адреноблокаторы (86.6%). Первичная конечная точка: смерть от сердечно-сосудистых причин или госпитализация по поводу сердечной недостаточности (СН). Клиническое исследование EMPHASIS-HF продемонстрировало, что применение эплеренона в средней дозе 39.1±13.8 мг/сут (25-50 мг) у пациентов с ХСН II ФК по классификации NYHA снижает смертность, связанную с сердечно-сосудистыми заболеваниями на 37% (p<0.001). Клиническая эффективность была продемонстрирована, главным образом, при применении эплеренона у пациентов в возрасте до 75 лет. Эффективность терапии у пациентов в возрасте старше 75 лет не изучалась.
ЭКГ
В исследованиях по изучению динамики ЭКГ у здоровых добровольцев существенного влияния эплеренона на ЧСС, длительность интервалов QRS, PR или QT не выявлено.
Побочные действия
Ниже перечислены нежелательные явления, которые могли быть связаны с лечением, а также серьезные нежелательные явления, частота которых сопоставима с частотой нежелательных и серьезных нежелательных явлений в группе плацебо. Нежелательные явления распределены по системам организма и частоте: часто (>1/100, <1/10); нечасто (>1/1000, <1/100); частота неизвестна (не может быть подсчитана по имеющимся данным).
Со стороны системы кроветворения: нечасто — эозинофилия.
Со стороны обмена веществ: часто — гиперкалиемия, дегидратация, гиперхолестеринемия, гипертриглицеридемия; нечасто — гипонатриемия, гипотиреоз.
Психические расстройства: нечасто — бессонница.
Со стороны нервной системы: часто — головокружение, обморок; нечасто — головная боль, гипестезия.
Со стороны сердечно-сосудистой системы: часто — инфаркт миокарда, выраженное снижение АД; нечасто — фибрилляция предсердий, левожелудочковая недостаточность, тахикардия, ортостатическая гипотензия, тромбоз артерий нижних конечностей.
Со стороны дыхательной системы: часто — кашель; нечасто — фарингит.
Со стороны пищеварительной системы: часто — диарея, тошнота, запор; нечасто — метеоризм, рвота.
Со стороны печени и желчевыводящих путей: нечасто — холецистит.
Со стороны кожных покровов и подкожно-жировой клетчатки: часто — кожный зуд; нечасто — повышенное потоотделение, сыпь; частота неизвестна — ангионевротический отек.
Со стороны костно-мышечной системы: часто — судороги в икроножных мышцах ног, мышечно-скелетные боли; нечасто — боль в спине.
Со стороны мочевыделительной системы: часто — нарушение функции почек; нечасто — пиелонефрит.
Прочие: нечасто — гинекомастия, астения, недомогание.
Лабораторные показатели: нечасто — повышение концентрации остаточного азота мочевины, креатинина, снижение экспрессии рецептора эпидермального фактора роста, повышение концентрации глюкозы в сыворотке крови.
Применение при беременности и кормлении грудью
Сведений о применении препарата у беременных женщин нет. Препарат следует назначать с осторожностью и только в тех случаях, когда ожидаемая польза для матери значительно превышает возможный риск для плода/ребенка.
Сведений о выведении эплеренона после приема внутрь с грудным молоком нет. Возможные нежелательные эффекты эплеренона на новорожденных, находящихся на грудном вскармливании, неизвестны, поэтому целесообразно или прекратить кормление грудью, или отменить препарат, в зависимости от его важности для матери.
Взаимодействие
Фармакодинамическое взаимодействие
Калийсберегающие диуретики и препараты калия: учитывая повышенный риск развития гиперкалиемии, эплеренон не следует назначать пациентам, получающим калийсберегающие диуретики и препараты калия. Калийсберегающие диуретики могут усилить эффекты гипотензивных средств и других диуретиков.
Препараты, содержащие литий: взаимодействие эплеренона с препаратами лития не изучалось. Однако у пациентов, получавших препараты лития в сочетании с диуретиками и ингибиторами АПФ, описаны случаи повышения концентрации и интоксикации литием. Если подобная комбинация необходима, целесообразно контролировать концентрацию лития в плазме крови.
Циклоспорин, такролпмус: циклоспорин и такролимус могут вызвать нарушение функции почек и повысить риск развития гиперкалиемии. Следует избегать одновременного применения эплеренона и циклоспорина или такролимуса. Если во время лечения эплереноном потребуется назначение циклоспорина или такролимуса, рекомендуется тщательно контролировать содержание калия в сыворотке крови и функцию почек.
НПВП: лечение НПВП может привести к острой почечной недостаточности за счет прямого подавления клубочковой фильтрации, особенно у пациентов группы риска (пожилые пациенты и/или пациенты с дегидратацией). При совместном применении этих средств до начала и во время лечения необходимо обеспечивать адекватный водный режим и контролировать функцию почек.
Триметоприм: одновременное применение триметоприма с эплереноном повышает риск развития гиперкалиемии. Рекомендуется контролировать содержание калия в сыворотке крови и функцию почек, особенно у пациентов с почечной недостаточностью и у пожилых пациентов.
Ингибиторы АПФ и антагонисты рецепторов ангиотензина II: при применении эплеренона с ингибиторами АПФ или антагонистами рецепторов ангиотензина II следует тщательно контролировать содержание калия сыворотки крови. Подобная комбинация может привести к увеличению риска развития гиперкалиемии, особенно у пациентов с нарушением функции почек, в т.ч. у пожилых пациентов. Не следует применять тройную комбинацию ингибитора АПФ и антагонистов рецепторов ангиотензина II с эплереноном.
Альфа1-адреноблокаторы (празозин, альфузозин): при одновременном применении альфа1-адреноблокаторов с эплереноном может усилиться антигипертензивное действие и/или увеличиться риск развития ортостатической гипотензии, в связи с чем, рекомендуется контроль АД, особенно при изменении положения тела.
Трициклические антидепрессанты, нейролептики, амифостин, баклофен: при одновременном применении этих средств с эплереноном может усилиться антигипертензивный эффект или увеличиться риск развития ортостатической гипотензии.
Глюкокортикоиды, тетракозактид: одновременное применение этих средств с эплереноном может привести к задержке натрия и жидкости.
Фармакокинетическое взаимодействие
Исследования in vitro свидетельствуют о том, что эплеренон не ингибирует изоферменты CYP1А2, CYP2С19, CYP2С9, CYP2D6 и CYP3А4. Эплеренон не является субстратом или ингибитором гликопротеина Р.
Дигоксин: AUC дигоксина при одновременном применении с эплереноном увеличивается на 16% (90% ДИ: 4%-30%). Необходимо соблюдать осторожность, если дигоксин применяется в дозах, близких к максимальным терапевтическим.
Варфарин: клинически значимого фармакокинетического взаимодействия с варфарином не выявлено. Необходимо соблюдать осторожность, если варфарин применяется в дозах, близких к максимальным терапевтическим.
Субстраты изофермента CYP3А4: в специальных исследованиях признаков фармакокинетического взаимодействия эплеренона с субстратами изофермента CYP3А4, например, мидазоламом и цизапридом, выявлено не было.
Ингибиторы изофермента CYP3А4
Сильные ингибиторы изофермента CYP3А4: при применении эплеренона со средствами, ингибирующими изофермент CYP3А4, возможно значимое фармакокинетическое взаимодействие. Сильный ингибитор изофермента CYP3А4 (кетоконазол 200 мг 2 раза/сут) вызывал увеличение AUC эплеренона на 441%. Одновременное применение эплеренона с сильными ингибиторами изофермента CYP3А4, такими как кетоконазол, итраконазол, ритонавир, нелфинавир, кларитромицин, телитромицин и нефазадон, противопоказано.
Слабые и умеренные ингибиторы изофермента CYP3А4: одновременное применение с эритромицином, саквинавиром, амиодароном, дилтиаземом, верапамилом и флуконазолом сопровождалось значимым фармакокинетическим взаимодействием (степень увеличения AUC варьировала от 98% до 187%). При одновременном применении этих средств с эплереноном доза последнего не должна превышать 25 мг.
Индукторы изофермента CYP3А4
Одновременный прием препаратов, содержащих зверобой продырявленный (St John’s Wort, сильный индуктор изофермента CYP3А4) с эплереноном вызывал снижение AUC последнего на 30%. При применении более сильных индукторов изофермента CYP3А4, таких как рифампицин, возможно более выраженное снижение AUC эплеренона. Учитывая возможное снижение эффективности эплеренона, одновременное применение сильных индукторов изофермента CYP3А4 (рифампицина, карбамазепина, фенитоина, фенобарбитала, препаратов, содержащих зверобой продырявленный) не рекомендуется.
Антациды: на основании фармакокинетического клинического исследования значительного взаимодействия антацидов с эплереноном при их одновременном применении не предполагается.
Передозировка
Случаев передозировки эплеренона у человека не описано.
Симптомы: наиболее вероятными проявлениями передозировки могут быть снижение АД и гиперкалиемия.
Лечение: при чрезмерном снижении АД необходимо назначить поддерживающее лечение. В случае развития гиперкалиемии показана стандартная терапия. Эплеренон не удаляется при гемодиализе. Установлено, что эплеренон активно связывается с активированным углем.
Влияние на способность к вождению автотранспорта и управлению механизмами
Эффекты препарата Инспра® на способность управлять автотранспортом или пользоваться техникой не изучались. Однако, учитывая возможность препарата вызывать головокружение и обморочные состояния, следует соблюдать осторожность при управлении автотранспортом или использовании техники на фоне приема препарата Инспра®.
Список литературы (источники):
- Государственный реестр лекарственных средств
- Анатомо-терапевтическо-химическая классификация (ATX)
- Международная классификация болезней (МКБ-10)
- Официальная инструкция от производителя
Илсира® (Ilsira) инструкция по применению
📜 Инструкция по применению Илсира®
💊 Состав препарата Илсира®
✅ Применение препарата Илсира®
📅 Условия хранения Илсира®
⏳ Срок годности Илсира®
Препарат отпускается по рецепту
Входит в список «Жизненно необходимых и важнейших лекарственных
препаратов»
Температура хранения: от 2 до 8 °С
Описание лекарственного препарата
Илсира®
(Ilsira)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для электронного издания справочника Видаль 2024
года, дата обновления: 2023.09.24
Владелец регистрационного удостоверения:
Контакты для обращений:
БИОКАД АО
(Россия)
Код ATX:
L04AC
(Ингибиторы интерлейкина)
Лекарственная форма
|
Препарат отпускается по рецепту |
Илсира® |
Раствор для подкожного введения 180 мг/1 мл: шприцы 0.9 мл 2 или 4 шт. в компл. с салфетками рег. №: ЛП-006244 |
Форма выпуска, упаковка и состав
препарата Илсира®
Раствор для п/к введения прозрачный, желто-коричневого цвета; возможно наличие легкой опалесценции.
* предварительно наполненный шприц.
Вспомогательные вещества: натрия ацетата тригидрат — 0.392 мг, глицин — 6.8 мг, маннитол — 20.7 мг, кислота уксусная ледяная — до pH 5.0, вода д/и — до 0.9 мл.
0.9 мл — шприцы трехкомпонентные стерильные из бесцветного стекла (1) — упаковки ячейковые контурные (2) в комплекте с салфетками спиртовыми (2 шт.) — пачки картонные.
0.9 мл — шприцы трехкомпонентные стерильные из бесцветного стекла (1) — упаковки ячейковые контурные (4) в комплекте с салфетками спиртовыми (4 шт.) — пачки картонные.
На каждый шприц наклеивают самоклеящуюся этикетку.
Фармакологическое действие
Левилимаб — рекомбинантное моноклональное антитело подкласса IgG1, высокогомологичное нативным человеческим антителам, связывающееся с α-субъединицей рецептора к интерлейкину-6 (ИЛ-6). Молекула левилимаба содержит вариабельные фрагменты легких и тяжелых цепей глубокой оптимизации и константные домены с полностью человеческой последовательностью. Левилимаб связывается и блокирует как растворимые (рИЛР), так и мембранные рецепторы ИЛ-6 (мИЛ6Р). Блокада обеих форм рецептора позволяет предотвратить реализацию ИЛ-6-ассоциированного провоспалительного каскада, препятствует активации антиген-представляющих клеток, В- и Т-лимфоцитов, моноцитов и макрофагов, эндотелиальных клеток и фибробластов, и избыточной продукции других провоспалительных цитокинов. ИЛ-6 является ключевым элементом синдрома массивного высвобождения цитокинов (синдрома «цитокинового шторма», гемофагоцитарного лимфогистиоцитоза или синдрома активации макрофагов), который может привести к острому респираторному дистресс-синдрому, полиорганной недостаточности и являться причиной летального исхода. Массивное высвобождение цитокинов («цитокиновый шторм») наблюдается у пациентов, получающих иммуносупрессивную терапию, включая деплецирующие агенты (в частности моноклональные антитела к рецепторам Т- и В-лимфоцитов), а также при тяжелых инфекционных заболеваниях, в т.ч. у пациентов с COVID-19. Высокий уровень ИЛ-6 в крови ассоциирован с более тяжелым течением новой коронавирусной инфекции и выраженными изменениями легких, что обусловливает потребность в интенсивной терапии и увеличивает риск летального исхода при COVID-19. ИЛ-6 – единственный цитокин, непосредственно индуцирующий синтез острофазовых белков в гепатоцитах: С-реактивного белка (СРБ), фибриногена, сывороточного амилоидного белка А-SAA, гепсидина, лептина. Кроме того, ИЛ-6 участвует в активации и поддержании местных воспалительных реакций (образование паннуса в синовии, стимуляция остеокластогенеза — эрозии хрящевой ткани, остеопороз), что наблюдается в патогенезе ревматоидного артрита.
Специфическая противовоспалительная активность левилимаба продемонстрирована в тестах in vitro и in vivo. Левилимаб оказывает антипролиферативное действие на культуру клеток DS-1, вызывая дозозависимое ингибирование роста клеток. На модели коллаген-индуцированного артрита у яванских макак (Macaca fascicularis) многократное (1 раз в неделю в течение 7 недель) п/к введение левилимаба сопровождается снижением выраженности воспалительной реакции в суставах, что подтверждено при гистологическом исследовании (значимое снижение выраженности воспалительных и дегенеративных изменений хрящевой ткани).
Изменение параметров фармакодинамических маркеров (нарастание концентрации рИЛ6Р, насыщение мИЛ6Р, нарастание концентрации ИЛ-6) свидетельствует о высокоэффективной дозозависимой нейтрализации препаратом левилимаб обеих форм рецептора ИЛ-6, что в свою очередь сопровождается быстрым и выраженным снижением сывороточной концентрации СРБ, отражающим эффективное подавление воспалительного процесса. В клинических исследованиях левилимаба продемонстрировано блокирование до 90% мембранных рецепторов к ИЛ-6 в течение первых 2 часов от момента однократного п/к введения препарата в дозе 1.6 мг/кг и более.
Фармакокинетика
Всасывание и распределение
При однократном п/к введении левилимаба наблюдается дозозависимый рост его концентрации в сыворотке крови. После введения препарат начинает обнаруживаться в сыворотке крови пациентов через 2-12 ч, и его концентрация нарастает, достигая максимальных значений через 96 [72-168] ч. Дозы препарата, превышающие 2.0 мг/кг, продемонстрировали двухфазный характер увеличения концентрации: первый пик наблюдался в период 48-72 ч, второй – к 168 ч с последующим снижением до неопределяемых значений к 70 дню.
После однократного п/к введения препарата в дозе 162 мг Cmax левилимаба в сыворотке крови составляла 17543 [10975; 28323] нг/мл, а значения показателя AUC, рассчитанного в период 0-168 ч (AUC0-168) – 1866231 [1297632-3719014] нг/мл×ч.
При многократном введении левилимаба пациентам с ревматоидным артритом значения суммарной AUC, рассчитанной в период 0-2016 ч после введения (AUC0-2016), составили 189580779 [134794695; 230680771] нг/мл×ч при введении 1 раз в неделю и 50763951 [34465213.5; 65810194.5] нг/мл×ч при введении 1 раз в 2 недели. Показатель Сmax-mult при повторных введениях нарастал и достигал значений 201024 [151563-246408] нг/мл при еженедельном введении препарата и 51570 [37201-71740] нг/мл при введении 1 раз в 2 недели. При этом Tmax составляло 1848 [1512; 2016] ч при еженедельном введении препарата и 1848 [1512; 1848] ч при введении 1 раз в 2 недели соответственно. Стационарный Vd составил 7871.029 [4226.795; 13363.547] мл при введении препарата 1 раз в неделю и 7130.453 [5532.978; 11387.959] мл при введении 1 раз в 2 недели.
При повторных введениях отмечается накопление препарата, с ростом Cmax в 6.5-14.2 раза при еженедельном введении и в 1.9-4.2 раза при введении препарата 1 раз в 2 недели. Коэффициент кумуляции (AR) составил 10.932 [6.446; 14.178] для еженедельного введения препарата и 2.593 [1.902; 4.164] для введения 1 раз в 2 недели.
Таким образом, у пациентов с ревматоидным артритом многократное п/к введение левилимаба 1 раз в неделю обеспечивает более высокую сывороточную концентрацию и экспозицию по сравнению с введением 1 раз в 2 недели.
Выведение
Общий клиренс (Cl) левилимаба после однократного введения в дозе 2.2 мг/кг составил 35.288±11.7 мл/ч, а в дозе 2.9 мг/кг показатель Cl – 25.974±1.1 мл/ч. T1/2 однократной п/к дозы 2.9 мг/кг составил 133.683 [92.754; 197.197] ч. Значения показателей, характеризующих период элиминации, обладают дозозависимостью (показатели среднего времени пребывания препарата в организме (MRT) и T1/2 нарастают с увеличением введенной дозы, а Cl – снижается), что говорит о нелинейной фармакокинетике препарата, обусловленной мишень-опосредованными распределением и элиминацией.
Фармакокинетика у особых групп пациентов
Пациенты с почечной и печеночной недостаточностью: специальных исследований у данной категории пациентов не проводилось; фармакокинетические данные у больных с почечной и печеночной недостаточностью отсутствуют.
Пациенты в возрасте старше 65 лет: фармакокинетические данные у лиц в возрасте старше 65 лет отсутствуют.
Показания препарата
Илсира®
Новая коронавирусная инфекция (COVID-19)
- патогенетическая терапия синдрома высвобождения цитокинов при тяжелом течении новой коронавирусной инфекции (COVID-19).
Ревматоидный артрит
- ревматоидный артрит умеренной или высокой степени активности у взрослых с отсутствием адекватного ответа на терапию одним или несколькими болезнь-модифицирующими противоревматическими препаратами, в т.ч. для торможения рентгенологической прогрессии. Левилимаб применяется в комбинированной терапии с метотрексатом и/или другими синтетическими базисными противовоспалительными препаратами.
Режим дозирования
Для п/к введения.
Препарат Илсира® предназначен для введения как в амбулаторно-поликлинических, так и в стационарных условиях.
Применение левилимаба должно осуществляться под контролем врача. В случае длительного применения препарата, в частности для терапии ревматоидного артрита, если врач считает это возможным, после соответствующего обучения технике п/к инъекций пациенты могут самостоятельно вводить себе препарат.
Препарат Илсира® вводят п/к с помощью преднаполненного шприца в область передней брюшной стенки (отступая не менее 5 см от пупка), передней и боковой поверхности бедра или средней трети наружной части плеча.
Не следует вводить препарат в места с поврежденной или измененной кожей (с наличием уплотнений, покраснений, новообразований, гиперпигментаций или повышенной чувствительности).
С целью патогенетической терапии синдрома высвобождения цитокинов при тяжелом течении новой коронавирусной инфекции (COVID-19) рекомендуемая доза препарата Илсира® составляет 324 мг однократно в виде двух п/к инъекций по 162 мг каждая. В случае недостаточного эффекта первой дозы левилимаба возможно повторное введение препарата через 48–96 ч в дозе 324 мг в виде двух п/к инъекций по 162 мг каждая. Решение о необходимости повторного введения принимается исключительно врачом.
Для терапии ревматоидного артрита рекомендуемая доза препарата Илсира® составляет 162 мг п/к 1 раз в неделю.
При достижении ремиссии заболевания возможно применение в режиме 162 мг п/к 1 раз в 2 недели. Пациентам, не достигшим ремиссии, рекомендовано продолжить применение препарата в дозе 162 мг п/к 1 раз в неделю. Пациентам, имеющим нарастание активности заболевания после снижения кратности введений, рекомендовано возобновить применение препарата в дозе 162 мг п/к 1 раз в неделю.
При развитии нежелательных явлений в ходе терапии ревматоидного артрита, связанных с изменением лабораторных показателей, следует провести коррекцию дозы и режима введения в соответствии с рекомендациями в таблицах 1, 2 и 3.
Таблица 1. Рекомендации по коррекции дозы при повышении активности печеночных ферментов АЛТ или АСТ
Таблица 2. Рекомендации по коррекции дозы при снижении абсолютного числа нейтрофилов (АЧН)
Таблица 3. Рекомендации по коррекции дозы при снижении количества тромбоцитов
Пропуск дозы при терапии ревматоидного артрита
При пропуске очередного введения по любой причине инъекция препарата Илсира® должна быть произведена как можно быстрее. Новый отсчет для даты следующего введения начинают с момента фактически проведенной инъекции препарата Илсира®.
Указания по применению
Подготовка к проведению п/к инъекции
- Тщательно вымойте руки.
- Извлеките упаковку со шприцем из холодильника. Затем извлеките шприц с лекарственным препаратом из картонной пачки. Осмотрите шприц, а также лекарственный препарат, находящийся в нем. Нельзя использовать шприц в случае:
- помутнения раствора, наличия в препарате посторонних видимых частиц;
- изменения цвета;
- повреждения любых частей шприца;
- истечения срока годности (годен до …), указанного на картонной пачке, а также на этикетке шприца.
- Оставьте шприц при комнатной температуре приблизительно на 25-30 мин. Не следует согревать шприц с препаратом каким-либо другим способом.
- Подготовьте спиртовую салфетку/ватный тампон.
На данном этапе не следует снимать колпачок шприца.
Техника выполнения п/к инъекции препарата Илсира® в преднаполненном шприце
1. Выберите место инъекции (передняя брюшная стенка (отступая не менее 5 см от пупка), передняя и боковая поверхность бедра или средняя треть наружной части плеча (возможные места для инъекций закрашены на рисунке ниже)).
2. Нельзя вводить препарат в место на коже, где имеется болезненность, покраснение, уплотнение или кровоподтек. Эти признаки могут указывать на наличие инфекции. Также не следует вводить препарат в места родинок, гиперпигментаций и шрамов.
3. Место укола необходимо обработать спиртовой салфеткой круговыми движениями.
4. Шприц не встряхивать.
5. Снимите колпачок с иглы, не дотрагиваясь до иглы и избегая прикосновения к другим поверхностям.
6. Одной рукой возьмите в складку обработанную кожу.
7. В другую руку возьмите шприц, держа его градуированной поверхностью вверх. Введение препарата необходимо осуществлять под углом 45 или 90 градусов к поверхности кожи в зависимости от толщины кожи и выраженности подкожно-жирового слоя (у худощавых пациентов введение препарата осуществляется под углом 45 градусов, у пациентов с толщиной кожной складки более 1.5 см допустимо введение под углом 90 градусов).
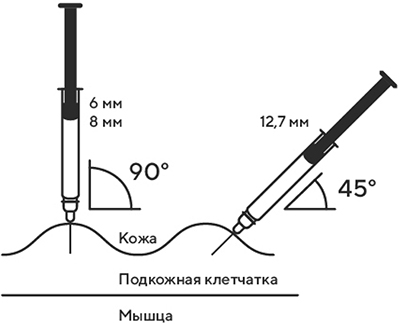
8. Одним быстрым движением полностью введите иглу в кожную складку.
9. После введения иглы отпустите складку кожи.
10. Введите весь раствор медленным постоянным надавливанием на поршень шприца в течение 2-5 сек.
11. Когда шприц будет пустым, выньте иглу из кожи под тем же углом.
12. Кусочком марли слегка прижмите область инъекции в течение 10 сек, но ни в коем случае не трите поверхность. Из места инъекции может выделиться небольшое количество крови. При желании можно воспользоваться пластырем.
13. После инъекции шприц повторно не использовать.
14. Вторую инъекцию препарата Илсира® для достижения общей дозы 324 мг выполнить аналогичным образом.
15. При последующих инъекциях следует менять место введения.
Утилизация расходного материала
Неиспользованный раствор препарата, использованные шприцы, салфетки/ватные тампоны и другие расходные материалы подлежат утилизации с применением закрывающегося контейнера, устойчивого к проколам для острых предметов из пластика или стекла.
Не допускать хранения использованных шприцев в местах, доступных для детей.
Побочное действие
В рамках проведенных клинических исследований у здоровых добровольцев, пациентов с ревматоидным артритом и тяжелым течением новой коронавирусной инфекции (COVID-19) препарат Илсира® показал благоприятный профиль безопасности. Наиболее частыми нежелательными реакциями в проведенных клинических исследованиях были повышение активности АЛТ и АСТ, нейтропения и повышение уровня липидов в крови. Спектр зарегистрированных нежелательных явлений, связанных с применением препарата Илсира®, был ожидаемым для класса ингибиторов рецепторов ИЛ-6. Летальных исходов, связанных с терапией препаратом Илсира®, в ходе клинических исследований не было.
В данной инструкции нежелательные реакции представлены в соответствии с международным словарем нежелательных реакций MedDRA. Ниже приведен перечень нежелательных реакций, зарегистрированных у пациентов, получавших левилимаб в рамках клинических исследований, и имеющих определенную, вероятную или возможную степень связи с приемом препарата. Частота указана с учетом следующих критериев: очень часто (≥1/10), часто (от ≥1/100 до <1/10), нечасто (от ≥1/1000 до <1/100), редко (от ≥1/10000 до <1/1000), очень редко (≤10000).
* В клинических исследованиях регистрировались местные реакции в виде эритемы и кожного зуда.
** Данное НР проявлялось повышением АСТ и АЛТ и не сопровождалось другими симптомами токсического гепатита на фоне множественной лекарственной терапии.
Также в ходе клинической разработки регистрировались единичные нежелательные явления, для которых в настоящее время связь с применением левилимаба не установлена достоверно: воспаление очага кожного поражения, астения, анемия, лимфаденит, лимфоцитоз, отклонение от нормы процедуры визуализации легких, снижение активности АСТ.
В качестве нарушений со стороны иммунной системы в пострегистрационном периоде наблюдались единичные реакции гиперчувствительности (анафилактический шок, ангиоотек), что согласуется с известным профилем безопасности препаратов класса ингибиторов рецепторов ИЛ-6.
Противопоказания к применению
- гиперчувствительность к левилимабу, а также к любому из вспомогательных веществ препарата;
- клинически значимые активные инфекции, включая туберкулез;
- сепсис, обусловленный патогенами, отличными от COVID-19;
- вирусный гепатит В;
- нейтропения менее 0.5×109/л;
- тромбоцитопения менее 50×109/л;
- повышение активности АСТ или АЛТ более чем в 5 раз;
- печеночная недостаточность тяжелой степени (класс С по классификации Чайлд-Пью);
- почечная недостаточность тяжелой степени и в терминальной стадии (СКФ менее 30 мл/мин);
- детский и подростковый возраст до 18 лет;
- беременность;
- период грудного вскармливания;
- комбинированное применение с ингибиторами ФНОα или применение в течение 1 месяца после терапии моноклональными антителами к ФНОα.
С осторожностью
Следует соблюдать осторожность при назначении левилимаба следующим категориям пациентов:
- с хроническими и рецидивирующими инфекциями или с указаниями в анамнезе на них;
- с сопутствующими заболеваниями, предрасполагающими к развитию инфекций;
- в периоде ранней реконвалесценции после тяжелых и среднетяжелых инфекционных заболеваний;
- после недавно проведенной вакцинации живыми аттенуированными вакцинами;
- с печеночной недостаточностью легкой и средней степени тяжести (класс А и В по классификации Чайлд-Пью);
- с почечной недостаточностью средней степени тяжести (СКФ <60 мл/мин и ≥30 мл/мин);
- с дивертикулитом, дивертикулезом и язвенным поражением органов ЖКТ, в т.ч. в анамнезе, в связи с риском перфорации ЖКТ;
- с демиелинизирующими заболеваниями;
- у получающих иммуносупрессивную терапию после трансплантации органов.
В связи со способностью левилимаба подавлять реакции острой фазы воспаления следует проявлять особую осторожность в отношении раннего выявления инфекционных заболеваний на фоне терапии.
В связи с ограниченными данными клинических исследований о применении левилимаба у пациентов пожилого возраста следует соблюдать осторожность при назначении препарата пациентам этой возрастной группы.
Применение при беременности и кормлении грудью
Беременность
Исследований влияния на плод у беременных женщин не проводилось. Известно, что моноклональные антитела могут проникать через плацентарный барьер. Препарат Илсира® противопоказан к применению во время беременности. Женщины детородного возраста и их половые партнеры должны использовать эффективные средства контрацепции в период проведения терапии левилимабом.
Период грудного вскармливания
Неизвестно, проникает ли левилимаб в грудное молоко. Учитывая то, что иммуноглобулины класса G, к которым относится левилимаб, могут выделяться с грудным молоком, препарат Илсира® противопоказан к применению в период грудного вскармливания.
Фертильность
Данные о влиянии препарата на фертильность у людей отсутствуют.
Применение при нарушениях функции печени
Противопоказано применение препарата при печеночной недостаточности тяжелой степени (класс С по классификации Чайлд-Пью).
С осторожностью следует назначать препарат пациентам с печеночной недостаточностью легкой и средней степени тяжести (класс А и В по классификации Чайлд-Пью).
Применение при нарушениях функции почек
Противопоказано применение препарата при почечной недостаточности тяжелой степени и в терминальной стадии (СКФ менее 30 мл/мин).
С осторожностью следует назначать препарат пациентам с почечной недостаточностью средней степени тяжести (СКФ <60 мл/мин и ≥30 мл/мин).
Применение у детей
Противопоказано применение препарата в детском и подростковом возрасте до 18 лет.
Применение у пожилых пациентов
Следует соблюдать осторожность при назначении препарата пациентам пожилого возраста.
Особые указания
Прослеживаемость
В целях улучшения прослеживаемости биотехнологических лекарственных препаратов наименование и номер серии назначаемого лекарственного препарата левилимаб должны указываться в медицинской документации пациента.
Инфекции
Наличие таких потенциально тяжелых инфекций как ВИЧ, активный гепатит В, сифилис, туберкулез, относится к противопоказаниям для назначения левилимаба. Левилимаб не следует применять у пациентов с активным течением инфекционных заболеваний, включая локализованные инфекции. Учитывая иммуносупрессивное действие левилимаба, терапия этим препаратом потенциально может приводить к обострению хронических инфекций и повышению риска первичного инфицирования.
При реактивации гепатита В или развитии серьезных инфекций терапию левилимабом следует прекратить и назначить соответствующую этиотропную терапию.
Соблюдение осторожности требуется в отношении пациентов с рецидивирующими инфекционными заболеваниями в анамнезе, а также лиц, имеющих факторы риска развития инфекций в виде сопутствующих заболеваний или сопутствующей терапии.
С учетом подавления левилимабом реакций острой фазы воспаления симптомы инфекционного заболевания могут быть стерты, что следует учитывать при раннем выявлении серьезных инфекций у пациентов, получающих препарат Илсира®. При появлении любых симптомов, свидетельствующих о развитии инфекционного заболевания на фоне применения левилимаба, пациенту следует немедленно обратиться к врачу для своевременной диагностики и назначения терапии.
Туберкулез
Пациентам с активным туберкулезом терапия препаратом Илсира® противопоказана. Перед назначением препарата Илсира® и в ходе терапии необходимо проводить стандартный скрининг на туберкулез. Пациентам с латентным туберкулезом рекомендуется пройти стандартный курс противотуберкулезной терапии перед началом терапии препаратом Илсира®.
Лабораторные показатели
Нейтропения. В клинических исследованиях препарата Илсира® отмечалось снижение числа нейтрофилов. При длительной терапии пациентов с ревматоидным артритом снижение АЧН не сопровождалось более высокой частотой развития инфекций, в т.ч. серьезных. Следует соблюдать осторожность при лечении препаратом Илсира® пациентов с АЧН <2×109/л. При снижении АЧН <0.5×109/л терапию препаратом Илсира® следует отменить. Следует оценивать число нейтрофилов через 4-8 недель после начала терапии, а в дальнейшем в соответствии с клинической практикой.
Тромбоцитопения. В клинических исследованиях препарата Илсира® отмечалось снижение числа тромбоцитов. При длительной терапии пациентов с ревматоидным артритом снижение числа тромбоцитов не сопровождалось развитием кровотечений. Следует соблюдать осторожность при назначении терапии препаратом Илсира® при числе тромбоцитов ниже 100×103/мкл. Лечение не рекомендуется при числе тромбоцитов <50×103/мкл. Следует оценивать число тромбоцитов через 4-8 недель после начала терапии, а в дальнейшем в соответствии с клинической практикой.
Ферменты печени. В клинических исследованиях препарата Илсира® отмечалось повышение активности печеночных трансаминаз без признаков печеночной недостаточности. Частота возникновения подобных изменений может возрастать при совместном использовании с препаратами, обладающими потенциальным гепатотоксическим действием (например, метотрексатом, антибактериальными препаратами и другими). Следует соблюдать осторожность при назначении терапии препаратом Илсира® у пациентов с показателями АЛТ или АСТ, превышающими ВГН более чем в 1.5 раза. Следует оценивать показатели активности печеночных трансаминаз (АЛТ и АСТ) через 4-8 недель после начала терапии, а в дальнейшем в соответствии с клинической практикой.
Изменение показателей липидного обмена. В клинических исследованиях препарата Илсира® отмечалось повышение концентрации липидов (холестерин общий и/или ТГ). Следует оценивать показатели липидного обмена через 4-8 недель после начала терапии левилимабом, а в дальнейшем в соответствии с клинической практикой. При ведении пациентов с гиперлипидемией следует учитывать национальные рекомендации.
Реакции гиперчувствительности
При использовании левилимаба потенциально возможно развитие реакции гиперчувствительности. В рамках проведенных клинических исследований левилимаба реакций гиперчувствительности не зарегистрировано. В ходе пострегистрационного периода оценки препарата Илсира® описаны единичные случаи анафилактических реакций и реакций гиперчувствительности. При возникновении анафилактических или других серьезных аллергических реакций применение препарата Илсира® следует немедленно прекратить и начать соответствующую симптоматическую терапию.
Злокачественные новообразования
У пациентов с РА наблюдается повышенный риск злокачественных новообразований, который может усугубляться при длительном применении иммуносупрессивных лекарственных средств. Объем клинических данных по препаратам класса ингибиторов рецептора ИЛ-6 в целом и левилимабу в частности недостаточен для установления частоты развития злокачественных образований и подтверждение наличия причинно-следственной связи с терапией. Продолжается изучение безопасности левилимаба в ходе долгосрочного применения.
Наличие алкогольной или наркотической зависимости
Наличие алкогольной или наркотической зависимости, а также психических расстройств может стать причиной несоблюдения пациентом графика лечения левилимабом, что, в свою очередь может привести к снижению эффективности терапии. Необходимо более тщательное наблюдение за пациентами с указанными состояниями в связи с отсутствием результатов клинических исследований у данной категории пациентов и возможностью повышенного риска развития гепатотоксичности и других неблагоприятных последствий.
Иммуногенность
В ходе клинических исследований препарата Илсира®, в т.ч. при долгосрочном (в течение года) лечении ревматоидного артрита, выработки связывающих антител к левилимабу выявлено не было.
Пациенты в возрасте старше 65 лет
Данные об эффективности и безопасности препарата у пациентов в возрасте старше 65 лет ограничены. Не предполагается наличия существенных возрастных различий в распределении и выведении препарата.
Пациенты с нарушениями функции почек и печени
Эффективность и безопасность препарата у данной категории пациентов не изучались.
Использование в педиатрии
Исследование эффективности и безопасности препарата у детей и подростков в возрасте до 18 лет не проводилось.
Вакцинация
Не следует проводить иммунизацию живыми аттенуированными вакцинами в ходе лечения препаратом Илсира®, т.к. клиническая оценка безопасности данного взаимодействия в рамках клинических исследований не проводилась. Вакцинация живыми аттенуированными вакцинами до начала терапии препаратом Илсира®, а также интервал между вакцинацией и началом терапии должны соответствовать действующим клиническим рекомендациям.
Демиелинизирующие заболевания
С учетом данных по профилю безопасности препаратов класса ингибиторов рецепторов ИЛ-6 следует соблюдать осторожность при применении левилимаба у пациентов с демиелинизирующими заболеваниями. Необходимо тщательно контролировать появление симптомов, указывающих на развитие демиелинизирующего заболевания ЦНС, несмотря на то, что способность левилимаба вызывать демиелинизирующие заболевания ЦНС в настоящее время не установлена.
Влияние на способность к управлению транспортными средствами и механизмами
Отсутствуют данные о влиянии препарата Илсира® на способность управлять транспортными средствами и работать с машинами и/или механизмами. Учитывая то, что при терапии другими ингибиторами рецептора ИЛ-6 отмечались эпизоды головокружения, пациентам, испытывающим головокружение при применении препарата Илсира®, не рекомендуется управлять транспортными средствами и механизмами до тех пор, пока головокружение не прекратится.
Передозировка
Клинические данные о передозировке препарата Илсира® отсутствуют. Максимальная переносимая доза левилимаба для человека не установлена. В клинических исследованиях при п/к введении левилимаба в максимальной суточной дозе 324 мг двукратно с интервалом 48-96 ч новых нежелательных реакций, изменяющих представление о профиле безопасности препарата, не зарегистрировано.
Лечение: специфический антидот отсутствует. Проводят симптоматическую терапию.
Лекарственное взаимодействие
Сведений о наличии неблагоприятного лекарственного взаимодействия левилимаба с другими лекарственными препаратами до настоящего времени не получено.
Смешивание препарата с другими лекарственными средствами строго запрещено.
Условия хранения препарата Илсира®
Препарат следует хранить в защищенном от света, недоступном для детей месте при температуре от 2° до 8°С; не замораживать.
Срок годности препарата Илсира®
Срок годности — 3 года. Не применять по истечении срока годности.
Условия реализации
Препарат отпускают по рецепту.
БИОКАД АО
(Россия)
|
198515 Санкт-Петербург, |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Общая информация
Устаревшее наименование
—
Владелец
Номер регистрационного удостоверения РФ
ЛСР-004052/10
Действующее вещество (МНН)
Форма выпуска / дозировка
Таблетки, покрытые пленочной оболочкой
Лекарственная форма ГРЛС
Таблетки внутрь
Состав
1 таблетка содержит:
действующее вещество: эплеренон 25 мг или 50 мг;
вспомогательные вещества: лактозы моногидрат 35,700/ 71,400 мг, целлюлоза микрокристаллическая (РН-101) 15,375/30,750 мг, кроскармеллоза натрия 4,250/8,500 мг, гипромеллоза 2,550/5,100 мг, натрия лаурилсульфат 0,850/1,700 мг, тальк 0,850/ 1,700 мг, магния стеарат 0,425/0,850 мг;
пленочная оболочка: Опадрай желтый YS-1-12524-А 3,825/ 5,10 мг [гипромеллоза, титана диоксид, макрогол, полисорбат-80, краситель железа оксид желтый, краситель железа оксид красный].
Описание препарата
Таблетки 25 мг: желтые, ромбовидные таблетки, покрытые пленочной оболочкой, с гравировкой «Pfizer» на одной стороне, «NSR» над цифрой «25» на другой стороне.
Таблетки 50 мг: желтые, ромбовидные таблетки, покрытые пленочной оболочкой, с гравировкой «Pfizer» на одной стороне, «NSR» над цифрой «50» на другой стороне.
Фармако-терапевтическая группа
Диуретическое калийсберегающее средство
