Интал® (Intal®) инструкция по применению
📜 Инструкция по применению Интал®
💊 Состав препарата Интал®
✅ Применение препарата Интал®
📅 Условия хранения Интал®
⏳ Срок годности Интал®
Препарат отпускается по рецепту
Входит в список «Жизненно необходимых и важнейших лекарственных
препаратов»
⚠️ Срок действия регистрационного удостоверения данного продукта истёк 08.12.11
Описание лекарственного препарата
Интал®
(Intal®)
Основано на официально утвержденной инструкции по применению препарата и подготовлено для электронного издания справочника Видаль 2009 года, дата обновления: 2020.07.21
Владелец регистрационного удостоверения:
Код ATX:
R03BC01
(Кромоглициевая кислота)
Лекарственная форма
|
Препарат отпускается по рецепту |
Интал® |
Капсулы с порошком для ингаляций 20 мг: 30 шт. рег. №: П N011788/01 |
Форма выпуска, упаковка и состав
препарата Интал®
Капсулы с порошком для ингаляций твердые желатиновые, прозрачные, размер №2, состоящие из прозрачного бесцветного корпуса и прозрачной желтой крышечки, с надписью «SODIUM CROMOGLYCATE 20 mg»; содержимое капсул — однородный порошок белого или почти белого цвета.
Состав оболочки капсулы: желатин 100%.
10 шт. — блистеры (1) — саше (3) — пачки картонные.
Фармакологическое действие
Противоаллергическое средство, оказывает мембраностабилизирующее действие, препятствует дегрануляции тучных клеток и выделению из них гистамина, лейкотриенов, медленно реагирующей субстанции, брадикинина, простагландинов и других биологически активных веществ, предупреждает развитие бронхоспазма.
В легких ингибирование медиаторного ответа предотвращает развитие как ранней, так и поздней стадии астматической реакции. Препарат наиболее эффективен для профилактики аллергических реакций немедленного типа у больных относительно молодого возраста, у которых еще не развились хронические необратимые изменения в легких. Препарат не устраняет развившийся бронхоспазм.
Длительное применение уменьшает частоту приступов бронхиальной астмы и облегчает их течение, снижает потребность в бронхолитических и глюкокортикостероидных средствах.
Фармакокинетика
Абсорбция из дыхательных путей в системный кровоток после ингаляции порошка составляет 5%-15% от принятой дозы, причем всасывание со слизистых оболочек дыхательных путей происходит довольно быстро, однако может снижаться при увеличении количества секрета.
Кромогликат натрия быстро выводится из системного кровотока, в связи с чем последующие дозы, принимаемые в соответствии с рекомендованным режимом дозирования, не кумулируют.
Кромогликат натрия обратимо связывается с белками плазмы (приблизительно 65%) и не метаболизируется.
Выведение происходит в неизмененном виде с мочой и желчью приблизительно в одинаковых пропорциях. T1/2 в среднем составляет около 80 мин. Остальная часть выводится через легкие с выдыхаемым воздухом или оседает на стенках ротоглотки, затем проглатывается и выводится через кишечник.
Показания препарата
Интал®
- профилактическое лечение бронхиальной астмы, включая астму физического напряжения.
Режим дозирования
Препарат применяется ингаляционно.
Капсулы Интал предназначены для применения только с ингалятором «Спинхалер». Их нельзя принимать внутрь.
Так как терапия Инталом по существу профилактическая, важно, чтобы пациент был проинструктирован о необходимости регулярного приема препарата в отличие от других препаратов, ингаляции которых служат для купирования приступов.
Взрослые и дети с 2-х лет
Режим дозирования одинаков для взрослых и детей.
Обычная доза: 1 капсула 4 раза/сут с интервалами 3-6 ч между ними. В более тяжелых случаях или повышенном содержании антигена во внешней среде частота приема может быть увеличена до 6-8 раз/сут (120-160 мг/сут).
Дополнительное дозирование может также иметь место для профилактики перед физической нагрузкой, вызывающей приступы удушья.
При достижении стойкого терапевтического эффекта возможен переход на минимальную поддерживающую дозу, обеспечивающую достаточный контроль над симптомами бронхиальной астмы.
Побочное действие
Со стороны дыхательной системы: раздражение слизистой оболочки дыхательных путей (охриплость, кашель). Крайне редко — легочные инфильтраты с эозинофилией.
Со стороны пищеварительного тракта: сухость во рту, тошнота.
Со стороны нервной системы: головокружение, головная боль.
Со стороны мочевыводящей системы: задержка мочи, нарушение функции почек.
Аллергические реакции: кожная сыпь, бронхоспазм, отек гортани, ангионевротический отек, анафилаксия наблюдались менее чем у 1 из 100 тыс. пациентов.
Противопоказания к применению
- беременность (I триместр);
- детский возраст до 2-х лет;
- повышенная чувствительность к кромоглициевой кислоте.
С осторожностью: почечная/печеночная недостаточность, беременность (II — III триместры), период лактации.
Применение при беременности и кормлении грудью
Препарат не следует назначать женщинам в I триместре беременности. Кромогликат натрия может назначаться врачом во II-III триместрах и в период лактации (грудного вскармливания) только тогда, когда ожидаемая польза для беременной или кормящей женщины превышает возможный риск для плода или младенца.
Применение при нарушениях функции печени
С осторожностью: печеночная недостаточность.
Применение при нарушениях функции почек
С осторожностью: почечная недостаточность.
Применение у детей
Режим дозирования одинаков для взрослых и детей старше 2 лет.
Особые указания
Капсулы Интала не применяются для купирования приступов бронхоспазма.
Так как лечение препаратом носит профилактический характер, важно не прерывать его у пациентов, на которых препарат оказывает благотворное воздействие.
При необходимости отмены лечения препаратом, это следует делать постепенно, в течение недели. При этом симптомы астмы могут возобновиться.
Для пациентов, принимающих глюкокортикостероиды, при приеме Интала можно снизить дозу или отменить прием глюкокортикостероидов полностью. Необходимо наблюдение за пациентами при снижении дозы глюкокортикостероидов; предпочтительная скорость снижения дозы глюкокортикостероидов — 10% в неделю. Увеличение дозы глюкокортикостероидов может быть необходимо при утяжелении течения астмы и при инфекции, повышенном содержании антигена во внешней среде. Если возможно снижение дозы глюкокортикостероидов, то не следует прекращать прием Интала до установления нового режима дозирования глюкокортикостероидов.
Лечение пациентов с почечной/печеночной недостаточностью должно проходить под постоянным врачебным контролем.
Передозировка
Кромоглициевая кислота обладает низкой токсичностью, поэтому риск передозировки и развития каких-либо токсических явлений небольшой. Не требует никаких действий, кроме медицинского наблюдения.
Лекарственное взаимодействие
Бета-адреностимуляторы, глюкокортикостероиды, антигистаминные лекарственные средства, теофиллин усиливают действие кромогликата натрия.
Сочетанное назначение кромоглициевой кислоты и глюкокортикостероидов позволяет уменьшить дозировку последних, а в отдельных случаях полностью их отменить.
Бронхолитики необходимо принимать (ингалировать) перед ингаляцией кромогликата натрия.
Условия хранения препарата Интал®
Хранить при температуре ниже 30°С. Не замораживать! Хранить в недоступном для детей месте.
Срок годности препарата Интал®
Срок годности — 5 лет. Не использовать позже срока, указанного на упаковке.
Условия реализации
Препарат отпускается по рецепту.
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Новости клинической фармакологии
и фармацевтики
Ингаляционные устройства, применяемые в терапии бронхиальной астмы
Е.П. Терехова
В обзоре представлена современная классификация ингаляционных систем доставки, дана подробная характеристика ингаляционных устройств. Описаны преимущества и недостатки использования ингаляционных систем доставки, факторы, влияющие на депозицию частиц в дыхательных путях. Изложены принципы выбора системы доставки в зависимости от возраста пациента, степени обструкции дыхательных путей, внутреннего сопротивления устройства. Представлено средство доставки — дозированный аэрозольный ингалятор со встроенным счетчиком доз лекарственного препарата Тевакомб (салметерол/флутиказон).
Ключевые слова: бронхиальная астма, ингаляционные системы доставки, дозированный аэрозольный ингалятор со встроенным счетчиком доз лекарственного препарата Тевакомб (салметерол/флутиказон).
Введение
Согласно клиническим рекомендациям, основной путь введения лекарственных средств (ЛС) при бронхиальной астме (БА) — ингаляционный [1, 2]. Главное преимущество ингаляционной терапии заключается в возможности доставки ЛС непосредственно в дыхательные пути, при этом достигается быстрый положительный эффект, а также отмечаются высокая местная концентрация препарата и низкая системная биодоступность, что и определяет высокий терапевтический индекс (отношение желаемых и нежелательных эффектов) и безопасность ЛС [3].
Залогом успешной ингаляционной терапии является не только правильный выбор препарата, но и такие факторы, как обучение пациента ингаляционной технике, а также подбор оптимальной системы доставки ЛС [4]. Идеальное устройство доставки предполагает достаточно высокую депозицию препарата в легких, надежность и простоту в использовании, возможность применения в любом возрасте и при тяжелых стадиях заболевания [5].
Ингаляционная терапия
Ингаляционная терапия (аэрозольтерапия) -метод лечения, заключающийся во введении аэрозолей ЛС в дыхательные пути.
Преимущества ингаляционной терапии: • непосредственное воздействие на орган-мишень — трахеобронхиальное дерево;
I Екатерина Петровна Терехова — канд. мед. наук, доцент кафедры клинической аллергологии Российской медицинской академии последипломного образования, Москва._
• высокая концентрация ЛС в легких;
• эффективность значительно меньшей (в 15-20 раз) дозы по сравнению с вводимой пер-орально;
• отсутствие при местном применении побочных явлений (неизбежных при системном действии препаратов);
• быстрый ответ на препарат;
• проникновение препарата в дистальные отделы дыхательных путей.
Недостатки ингаляционной терапии:
• технологические сложности при изготовлении специальных лекарственных форм и ингаляционных устройств;
• необходимость обучения пациента технике выполнения ингаляции;
• зависимость эффективности лечения не только непосредственно от препарата, но и от полноты его доставки к органу-мишени;
• возможность местного раздражающего действия — высокая депозиция препарата в ротоглотке (примерно 80%);
• невозможность доставки больших доз ЛС;
• ошибки, допускаемые пациентами.
Что должен знать специалист, назначающий
аэрозольную терапию:
• для ингаляций используют ЛС, которые разрешены для применения в этих целях регулятор-ными органами;
• в листке-вкладыше к препарату ингаляционный путь введения должен быть указан как допустимый или рекомендуемый;
• независимо от личного опыта врача и рекомендаций так называемой «старой школы» в настоящее время для ингаляций не рекомендова-
ны водорастворимые глюкокортикостероиды (ГКС) (преднизолон, гидрокортизон), эуфил-лин, антигистаминные препараты, многие антибактериальные препараты;
• создание произвольных смесей препаратов для ингаляций, не оговоренных в листке-вкладыше или в стандартах оказания медицинской помощи, недопустимо.
Один из главных параметров эффективности ингаляционного устройства — степень депонирования ЛС в дыхательных путях, которая зависит от системы ингаляционной доставки и колеблется в диапазоне от 4 до 60% отмеренной дозы [6]. На депонирование аэрозоля в дыхательных путях влияют следующие факторы [7]:
• размеры частиц;
• аэродинамический диаметр;
• морфология ротоглотки;
• морфология гортани;
• объем вдоха пациента;
• скорость воздушного потока при вдохе;
• скорость перемещения ингалируемых веществ.
Частицы размером более 5 мкм наиболее вероятно будут скапливаться в ротоглотке и проглатываться [8]. Частицы размером менее 5 мкм имеют наибольшую вероятность проникновения в более глубокие отделы дыхательных путей и депонирования в легких. Современные ингаляционные устройства создают аэрозоль с большой долей частиц, имеющих размер 1-5 мкм. Считается, что предпочтительный размер частиц ингаляционного препарата, обеспечивающий равномерное распределение его в крупных и дистальных бронхах, составляет для взрослых 1,0-5,0 мкм, а для детей — 1,1-3,0 мкм, и чем больше таких частиц генерируется при ингаляции, тем эффективнее распределение препарата в легких [9-11].
Частицы размерами 4-5 мкм депонируются в первую очередь в бронхах, а более мелкие остаются в воздушной струе и достигают периферических отделов дыхательных путей и альвеол.
Чем больше время пребывания аэрозоля в мелких периферических дыхательных путях, тем активнее депонирование за счет седиментации и броуновского движения [12]. Задержка дыхания после ингаляции аэрозоля увеличивает время его нахождения в дыхательных путях и усиливает депонирование в периферических отделах. Частицы аэрозоля, не осевшие в дыхательных путях, выводятся с выдыхаемым воздухом [8]. Для оценки аэродинамических характеристик исследуемых препаратов используют импакто-ры. С их помощью моделируется in vitro вдох пациента и производится количественный анализ частиц препарата, собранных на ступенях импактора.
Значимыми факторами являются морфология ротоглотки и гортани, объем вдоха пациента и скорость воздушного потока при вдохе. Скорость перемещения ингалируемых частиц обычно определяется скоростью инспираторного потока, что влияет на вероятность оседания аэрозоля в ротоглотке и гортани [13].
Классификация ингаляционных устройств
Ингаляционные устройства можно разделить на пять групп [7].
1. Дозированные аэрозольные ингаляторы (ДАИ) — ингаляторы под давлением, отмеряющие дозу (применяются самостоятельно, со спейсера-ми, с аэрокамерами, оснащенными клапаном).
2. Дозированные аэрозольные ингаляторы, активируемые вдохом (ДАИ-АВ) («Легкое Дыхание», Аутохалер).
3. Порошковые ингаляторы (ПИ) — ингаляторы сухого порошка, или дозированные ПИ (кап-сульные, резервуарные, блистерные).
4. «Мягкие» аэрозоли (soft-mist) (Респимат).
5. Небулайзеры (струйные, ультразвуковые, электронно-сетчатые).
Преимущества и недостатки разных типов ингаляционных устройств приведены в табл. 1.
Таблица 1. Преимущества и недостатки ингаляционных устройств
Тип устройства Преимущества Недостатки
ДАИ • Малые размеры • Короткое время, затрачиваемое на ингаляцию • Высокая воспроизводимость между дозами • Отсутствие риска контаминации • Необходимость координации вдоха и активации ингалятора • Большинство больных делают слишком быстрый вдох • Низкое депонирование в легких и высокое — в ротоглотке • Необходимо выпустить несколько доз в воздух перед первым применением нового ингалятора или после длительного перерыва в использовании • При ингаляции следует держать ингалятор в вертикальном положении • В большинстве ингаляторов трудно определить число оставшихся доз
Таблица 1. Окончание
Тип устройства Преимущества Недостатки
ДАИ + + спейсер • В меньшей степени требует координации вдоха с активацией ингалятора • Меньше депонирование препарата в ротоглотке • Лучше распределение препарата в легких • Эффективен для сохранения достаточной доставки лекарства в дыхательные пути при обострении • При использовании клапанного спейсера ингаляция может выполняться при спокойном дыхании • Некоторые спейсеры подают звуковой сигнал при слишком высокой скорости вдоха • Более дорогой и менее портативный, чем простой ДАИ • Высокая вероятность уменьшения или вариабельности ингалируемой дозы из-за электростатических свойств пластмассы • Специальные инструкции по обработке • Важно соблюдать инструкцию по ингаляции препарата через спейсер • Ошибки в ингаляционной технике могут привести к уменьшению или полному отсутствию поступления препарата в легкие (например, высвобождение в спейсер нескольких доз подряд до начала вдоха, пауза между высвобождением дозы и началом вдоха) • Некоторым детям нравится вызывать звуковой сигнал, специально могут делать слишком быстрый вдох
ДАИ-АВ • Эффективны у больных, которые не могут координировать вдох с активацией ингалятора, а также у пожилых • Высокая легочная депозиция • Невозможность использования при тяжелом обострении БА • Иногда пациенты останавливают вдох в момент активации ингалятора • При активации вдохом не контролируется скорость инспираторного потока, поэтому следует проинструктировать пациента делать медленный вдох • Возможна значительная орофарингеальная депозиция (если пациент не использует оптимизатор)
ПИ • Компактный. Многие ПИ многодозовые, некоторые — однодозовые (каждая доза в отдельной упаковке) • Активируются вдохом, поэтому не нуждаются во внешнем источнике энергии • В отличие от ДАИ не требуют координации вдоха и активации ингалятора • Большинство многодозовых ПИ снабжены счетчиком доз • Короткое время, затрачиваемое на ингаляцию • Однодозовые ПИ требуют повторной загрузки перед каждой ингаляцией, что повышает риск ошибок. Для ингаляции каждой дозы нужно сделать 2 вдоха • ПИ могут приводить к высокому депонированию лекарства в ротоглотке, потому что для активации ингалятора требуется большая скорость инспираторного потока • В некоторых ПИ высвобождение дозы зависит от скорости инспираторного потока. При низкой скорости, слишком медленном вдохе возможно плохое высвобождение дозы или полное отсутствие высвобождения лекарства из ингалятора • Прежде чем ингалировать лекарство, пациент должен сделать глубокий выдох до уровня функциональной остаточной емкости без ингалятора. Нельзя делать выдох в ингалятор, поскольку можно выдуть из ингалятора приготовленную дозу лекарства • Пациент должен с самого начала делать мощный вдох, а не наращивать скорость вдоха постепенно • Риск недополучения дозы лекарства во время обострения • Более высокая стоимость, чем у ДАИ • После подготовки дозы для ингаляции следует держать ингалятор вертикально. Во время ингаляции следует держать ингалятор вертикально или наклонив его горизонтально • Необходимо хранить ингалятор в прохладном сухом месте
Небулайзеры • Могут применяться в любом возрасте • Вибрационный электронно-сетчатый небулайзер портативный и не нуждается во внешнем источнике электроэнергии • Не требуется координации действий пациента • Могут использоваться для ингаляции лекарств, которые не выпускаются в виде ДАИ или ПИ • Не содержат пропеллента • В отличие от пневматических компрессорных небулайзеров у небулайзеров, активируемых вдохом, дозиметрических и электронно-сетчатых небулайзеров потеря лекарственного препарата в окружающую среду гораздо меньше • Дозиметрические небулайзеры продуцируют аэрозоль только во время вдоха в течение заданного периода и отключаются после высвобождения дозы • Пневматическим компрессорным небулайзерам для работы требуется источник энергии и компрессор • Время ингаляции может значительно увеличиваться • Суспензии небулизируются плохо • Функциональные характеристики (эмитируемая доза и размеры частиц) могут существенно различаться для разных приборов • В пневматических компрессорных небулайзерах часть лекарства теряется, диспергируясь в окружающую среду во время выдоха, при этом окружающие лица и медицинский персонал подвергаются воздействию этого лекарственного препарата • Из-за потерь лекарства во многих пневматических компрессорных ингаляторах некоторый объем раствора не диспергируется (так называемый «мертвый объем») • При недостаточно тщательной обработке небулайзера существует риск бактериального загрязнения • Более новые виды небулайзеров (вибрационные электронно-сетчатые небулайзеры) имеют высокую стоимость
Дозированные аэрозольные ингаляторы
Дозированные аэрозольные ингаляторы были введены в практику в 1956 г. как первые портативные многодозовые устройства для ингаляции бронходилататоров и по сей день остаются наиболее распространенными и часто назначаемыми ингаляторами [14]. При использовании ДАИ обычно возникают проблемы, связанные с неполной координацией вдоха и активацией ингалятора.
Как показали результаты клинических исследований, оптимальную технику ингаляции соблюдали только 22% взрослых и 20% детей. Характерными нарушениями были следующие: неправильное положение ингалятора, недостаточно глубокий выдох перед ингаляцией и недостаточно мощный и глубокий вдох, начатый одновременно с распылением препарата, неоднократное нажатие на баллончик, неправильная задержка дыхания, слишком быстрая ингаляция следующей дозы — менее чем через 1 мин после первой [15]. В метаанализе, проведенном M.G. Cochrane et al., было выявлено, что неадекватное использование ДАИ отмечается у 8-54% больных БА [4]. В то же время даже при адекватном применении ДАИ в легкие поступает только 10-15% от номинальной дозы препарата [10]. Дети младше 7 лет, пожилые люди, а также пациенты, неспособные произвести адекватный маневр вдоха (при выраженной обструкции, заболеваниях, ограничивающих подвижность грудной клетки, и т.д.), не могут пользоваться ДАИ.
Для пациентов, применяющих ДАИ, одним из серьезных затруднений является отслеживание количества израсходованных доз и определение времени замены ингалятора. Для того чтобы определить, не закончилось ли содержимое ДАИ, пациенты используют такие недостоверные методы, как встряхивание, оценка по массе баллончика или проверочные распыления, которые могут ввести их в заблуждение, поскольку пропелленты и другие инертные компоненты остаются в баллончике даже после полного употребления лекарственного вещества. Если в ингаляционном устройстве отсутствует счетчик доз (индикатор количества препарата, оставшегося внутри баллончика от начала его использования), пациент может ввести дозу, недостаточную для достижения терапевтического эффекта, выбросить не полностью использованный ингалятор или использовать его сверх номинального количества доз, когда качество ингаляции изготовителем уже не гарантируется.
В марте 2003 г. Управление по контролю качества пищевых продуктов и медикаментов США (Food and Drug Administration, FDA) вы-
пустило руководство «Встраивание в ДАИ с лекарственным средством устройства для подсчета доз», в котором рекомендуется установка счетчиков, показывающих количество доз, оставшихся в ДАИ [16].
Согласно рекомендациям FDA компания Teva разработала ДАИ со встроенным счетчиком доз и в июле 2013 г. зарегистрировала в России ДАИ со встроенным счетчиком доз лекарственного препарата Тевакомб (салметерол/флутика-зон) [17]. Установка счетчика доз в ДАИ позволяет повысить удовлетворенность пациентов, что подтверждено в исследовании с участием 268 пациентов, страдающих БА и хронической обструктивной болезнью легких и имевших не менее чем четырехлетний опыт применения ингаляторов [18]:
• 92% пациентов выразили удовлетворение от наличия счетчика доз;
• 92% пациентов согласились, что счетчик доз поможет предотвратить неожиданное окончание лекарства;
• 93% пациентов согласились, что счетчик доз давал бы возможность узнавать о необходимости замены баллончика;
• 90% пациентов согласились, что счетчик доз помог бы им отслеживать использование лекарства;
• 90% пациентов согласились, что счетчик доз дал бы им дополнительную уверенность в обеспеченности лекарственным средством.
При этом исходно 62% пациентов высказывали обеспокоенность по поводу того, что не знают, какое количество лекарства осталось у них в ингаляторе.
Приведенные результаты показывают, что дополнение ДАИ встроенным счетчиком доз является для пациентов надежным индикатором количества оставшихся в ингаляторе рекомендованных доз и повышает уверенность врача в том, что больной не будет применять ингалятор после того, как количество рекомендованных доз израсходовано.
Преимущества ДАИ со счетчиком доз:
• позволяет пациенту знать количество израсходованных и оставшихся доз;
• предупреждает пациента о необходимости приобрести новый ингалятор при малом количестве оставшихся доз;
• позволяет пациенту отслеживать потребление лекарства (особенно в случае контролирующих препаратов);
• позволяет родителям лучше следить за использованием ингалятора их ребенком, особенно если речь идет об ингаляторе, который ребенок берет с собой в школу;
• избавляет от беспокойства по поводу неожиданного окончания лекарства;
• уменьшает риск приема пациентом доз, недостаточных для достижения терапевтического эффекта;
• улучшает соблюдение предписанного режима приема лекарства и приверженность терапии;
• усиливает доверие пациента и его веру в эффективность препарата.
Характеристика ДАИ со встроенным счетчиком доз препарата Тевакомб:
• отображает численные показания;
• сохраняет прежний вид (благодаря привычному внешнему виду ингалятора не требуется дополнительного обучения пациентов его использованию);
• точен;
• имеет надежную конструкцию, которая не подведет в реальной жизни.
Таким образом, ДАИ со встроенным счетчиком доз предоставит пациентам надежный способ определения количества оставшихся доз лекарства в ингаляторе, повысит удовлетворенность пациентов, создаст условия для соблюдения предписанного режима приема лекарства и приверженности терапии. Кроме того, врачам будет обеспечено объективное средство контроля за выполнением предписаний в лечении. Счетчики доз должны помочь снизить расход денежных средств на необоснованное приобретение новых запасов препарата, а также уменьшить количество обращений в поликлинику.
Спейсеры
Чтобы решить проблему координации вдоха с активацией ДАИ, было предложено использовать ДАИ с дополнительным устройством -спейсером. Это могут быть как простые приспособления, увеличивающие расстояние между ДАИ и ротоглоткой пациента, тем самым уменьшающие депонирование ЛС в ротоглотке и снижающие системную биодоступность, так и более сложные. Некоторые спейсеры снабжены односторонним клапаном (клапанные спейсеры), позволяющим пациенту ингалировать статичное облако аэрозоля. Клапанные спейсеры не требуют координации вдоха с активацией ингалятора и повышают депонирование ЛС в легких у тех пациентов, которые не могут добиться оптимальной координации при пользовании ДАИ [19]. Спейсеры и клапанные спейсеры уменьшают нежелательное воздействие ЛС на ротоглотку и рекомендуются при назначении ингаляционных ГКС (ИГКС). Тем не менее, поскольку оро-фарингеальное депонирование всё же возможно, пациентам советуют полоскать рот после ин-
галяции ИГКС независимо от ингаляционного устройства.
Высвобождение в спейсер сразу нескольких доз ЛС повышает его потерю в результате усиления турбулентности, поэтому каждая доза должна высвобождаться в спейсер и ингалироваться из него отдельно. Более того, каждую дозу следует ингалировать из спейсера немедленно после ее высвобождения. Отсрочка ингаляции снижает эмитируемую дозу: чем дольше ЛС находится в спейсере, тем больше частиц оседает на его стенках [20]. На практике это означает, что больной должен сделать ингаляцию через 5 с после нажатия на баллончик, однако если на стенках спейсера не накопился заряд статического электричества, то эффективная доставка препарата возможна и через 30 с.
Дозированные аэрозольные ингаляторы,
активируемые вдохом
В 1990 г. был создан ДАИ-АВ Аутохалер (Easy Breathe). В России он зарегистрирован под названием «Легкое Дыхание». Такое ингаляционное устройство было разработано для того, чтобы решить проблему плохой координации вдоха с активацией ингалятора при использовании стандартных ДАИ. Особенностью подобной ингаляционной системы является наличие пружинного механизма, который взводится при открытии колпачка. В ответ на вдох в течение 0,2 с происходит высвобождение фиксированной дозы препарата. Для активации ингалятора пациенту достаточно развить скорость вдоха примерно 10-25 л/мин. Эта характеристика устройства делает его доступным для большинства больных БА [21].
Ингалятор «Легкое Дыхание», содержащий беклометазона дипропионат, комплектуется небольшим спейсером-оптимизатором (объем 50 мл). Особенностью спейсера этого типа является возможность выполнять вдох без предварительного впрыскивания дозы ЛС в спейсер. Использование оптимизатора имеет большое значение для уменьшения орофарингеальной депозиции ЛС и, следовательно, риска развития нежелательных эффектов [15].
Порошковые ингаляторы
Первый ПИ — Спинхалер был разработан в 1971 г. для ингаляции высоких доз кромоглика-та натрия, содержащегося в капсулах.
Принцип действия ПИ заключается в том, что ингаляция ЛС осуществляется за счет силы вдоха пациента. Это исключает проблемы координации, характерные для ДАИ, и определяет широкое использование ПИ как средств достав-
iНе можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
ки. Среди преимуществ ПИ можно отметить следующие:
— отсутствие пропеллентов (в отличие от ДАИ);
— отсутствие проблемы синхронизации;
— необходимая скорость вдоха 30-75 л/мин;
— низкая скорость выброса (фактически соответствует скорости вдоха);
— портативность, компактность;
— возможность использования у пациентов разных возрастных групп.
В ПИ препарат находится в чистом виде или в соединении с носителем (лактозой, бензоатом натрия) и является крупнодисперсным по своему составу (приблизительно 60 мкм). Во время вдоха часть ЛС вместе с турбулентным потоком, проходя через устройство ингалятора, измельчается до частиц респирабельных размеров. Эти частицы сухого вещества аэродинамически более стабильны, чем частицы ДАИ, поскольку транспортируются в легкие со скоростью потока воздуха, а не со скоростью струи пропеллента, не изменяют своего размера и формы после высвобождения из устройства, а потому обеспечивают большую депозицию препарата в легких — до 40% [1].
Существует два основных типа ПИ: многодо-зовые и однодозовые капсульные (Спинхалер, Ротахалер, Аэролайзер, ХандиХалер и др.).
Многодозовые ПИ представлены:
• ингаляторами, содержащими большое количество ЛС в резервуаре, которое дозируется пациентом при использовании ингалятора (Турбу-халер, Новолайзер, Изихейлер, Твистхейлер, Циклохалер, Кликхалер);
• ингаляторами, для которых ЛС расфасовано заводским способом в блистеры внутри ингаляционного устройства (Мультидиск, Дискха-лер) [7].
Все существующие ПИ функционируют за счет усилия вдоха больного (или инспираторного потока). В свою очередь, инспираторный поток зависит от внутреннего сопротивления устройства и инспираторного усилия пациента. Порошковые ингаляторы имеют разное внутреннее сопротивление. Это означает, что для получения необходимой дозы препарата пациент должен сделать глубокий мощный вдох через ингалятор. Недостаточно мощный вдох является одной из распространенных ошибок при применении ПИ. Именно поэтому при использовании капсульно-го ПИ важен инспираторный объем пациента. Необходимо сделать повторный вдох, чтобы убедиться, что получена вся доза препарата.
В исследованиях показано, что дети дошкольного возраста с БА могут сталкиваться с труд-
ностями при использовании некоторых ПИ, так как неспособны создать инспираторный поток необходимой мощности, и что инспираторный поток снижается при обострениях [22].
Ингаляторы, продуцирующие
«мягкий» аэрозоль (soft mist)
В настоящее время выпускается только один ингалятор, продуцирующий «мягкий» аэрозоль, — Респимат (Soft Mist). В России он используется для ингаляций тиотропия бромида (2,5 мкг в одной дозе). Респимат расщепляет раствор лекарства, используя механическую энергию пружины. Когда пружина распрямляется, раствор проталкивается через чрезвычайно тонкую форсунку [23]. Это создает мельчайший «туман» с медленной скоростью движения, обеспечивающей низкое депонирование препарата во рту и глотке и относительно высокое депонирование в легких (~39%) [24].
Небулайзеры
Небулайзерная терапия — метод ингаляционной терапии, в котором используется эффект преобразования жидких форм лекарственных препаратов в мелкодисперсный аэрозоль (от лат. nebula — «туман, облако»).
Важнейшей особенностью ингаляционной небулайзерной терапии является простота, доступность, необременительность и возможность проведения лечения в домашних условиях, в машине «скорой помощи», в больничной палате.
Важнейшее значение небулайзеры имеют в лечении детей и лиц пожилого возраста, для которых простота метода позволяет обеспечить высокую эффективность терапии [25].
В настоящее время в зависимости от вида энергии, превращающей жидкость в аэрозоль, различают три основных типа небулайзеров:
• компрессорные (струйные) — с использованием струи газа (воздух или кислород);
• ультразвуковые — с использованием энергии колебаний пьезокристалла;
• мембранные (mesh) — с использованием вибрирующей мембраны или пластины с множественными микроскопическими отверстиями (сито), через которую пропускается жидкая лекарственная субстанция [26, 27].
Лицевые маски и мундштуки. Чаще всего при применении небулайзеров используют мундштуки. Однако при лечении больных с тяжелым обострением, больных с нарушением сознания или грудных детей могут потребоваться лицевые маски.
К числу основных препаратов, используемых для небулайзерной терапии обструктивных забо-
Таблица 2. Корректный выбор ингаляционного устройства для пациентов с хорошей и плохой координацией вдоха с активацией ингалятора
Хорошая координация вдоха с активацией ингалятора Плохая координация вдоха с активацией ингалятора
скорость инспираторного потока*
>30 л/мин <30 л/мин >30 л/мин <30 л/мин
ДАИ ДАИ ДАИ + спейсер
ДАИ-АВ ДАИ-АВ
ПИ ПИ
Небулайзер Небулайзер Небулайзер Небулайзер
* Скорость инспираторного потока можно определить по кривой поток-объем во время спирометрии либо с помощью приборов, аналогичных In-Check Dial.
леваний легких, относятся бронходилататоры -короткодействующие Р2-агонисты (сальбутамол, фенотерол), короткодействующие антихолинер-гические препараты (ипратропий), их комбинации (сальбутамол/ипратропий, фенотерол/ипра-тропий), которые по сравнению с теофиллинами являются более мощными бронходилататорами и обладают меньшим числом побочных эффектов [28]. Кроме того, довольно часто при обструктив-ных заболеваниях легких применяется небулай-зерная терапия ГКС [29].
Необходимо помнить, что категорически запрещается использовать для ингаляций через не-булайзер эфирные масла и масляные растворы, а также суспензии и растворы, содержащие взвешенные частицы, в том числе настои и настойки трав, метилксантины, папаверин, платифиллин, антигистаминные препараты и системные ГКС (гидрокортизон, преднизолон).
Для проведения небулайзерной терапии используются только специально предназначенные для этих целей растворы ЛС, разрешенные к применению Фармакологическим комитетом Министерства здравоохранения Российской Федерации. Даже маленькая частица раствора в аэрозоле сохраняет все лекарственные свойства вещества, растворы не вызывают повреждения слизистой бронхов и альвеол, а упаковка в виде флаконов или небул позволяет удобно дозировать препараты как в стационарных, так и в домашних условиях [21].
Выбор ингаляционного устройства
Выбор ингалятора для конкретного ЛС определяется существующими устройствами, применяемыми для доставки данного препарата, а также способностью и желанием пациента использовать его правильно. Дозированные аэрозольные ингаляторы требуют хорошей координации вдоха с активацией ингалятора для оптимального депонирования лекарства, тогда как для ПИ
необходим соответствующий инспираторный поток. В табл. 2 представлена информация по поводу правильного выбора ингаляционного устройства для больных с хорошей координацией вдоха и активации ингалятора с достаточным инспира-торным усилием. К пациентам с плохой координацией вдоха и активации ингалятора относятся дети и пожилые больные.
Во всех клинических ситуациях выбор ингаляционного устройства зависит от:
• способности пациента правильно использовать ингалятор;
• предпочтений пациента;
• наличия необходимого ЛС в виде конкретных ингаляционных устройств;
• объемной скорости вдоха (скорость воздушного потока у больного на вдохе, в л/мин);
• внутреннего сопротивления (респираторного сопротивления) устройства (скорость воздушного потока, необходимая для приведения ингалятора в действие или проведения оптимальной ингаляции);
• возможности врача обучить больного правильному применению ингалятора и мониториро-вать приобретенные навыки впоследствии;
• стоимости терапии и возможности ее компенсации страховыми компаниями.
Был сделан важный вывод: в идеале пациент должен использовать только один тип ингалятора для всех назначенных ему ингаляционных ЛС, это упрощает обучение больного и снижает вероятность ошибок [7, 15]. Данное заключение соответствует рекомендациям Европейского респираторного общества и Международного общества по использованию аэрозолей в медицине при выборе ингаляционного устройства.
Заключение
Согласно клиническим рекомендациям, основной путь введения ЛС при БА — ингаляционный. Преимуществом ингаляционной терапии
является создание высокой концентрации лекарства в дыхательных путях при минимальных системных нежелательных эффектах. Эффективность лечения ингаляционными препаратами во многом зависит от характеристики средства доставки и отношения пациента к ингалятору. При выборе ингалятора среди прочих факторов следует учитывать степень обструкции дыхательных путей у пациента, его навыки обращения с различными типами ингаляторов.
Дозированный аэрозольный ингалятор со встроенным счетчиком доз лекарственного препарата Тевакомб (салметерол/флутиказон) предоставляет пациентам надежный способ определения количества оставшихся доз ЛС в ДАИ, создает условия для соблюдения предписанного режима приема ЛС и приверженности терапии.
Список литературы
1. Global Initiative for Asthma. Global Strategy for Asthma Management and Prevention. Workshop Report 2007 // http://www.ginasthma.org
2. Global Initiative for Asthma. Global Strategy for Asthma Management and Prevention. Updated 2009 // http://www.ginasthma.org
3. Цой А.Н. // Атмосфера. Пульмонология и аллергология. 2009. № 3. С. 16.
4. Cochrane M.G. et al. // Chest. 2000. V. 117. № 2. P. 542.
5. Авдеев С.Н. // Consilium Medicum. 2011. Т. 13. № 3. С. 36.
6. Авдеев С.Н. // Рус. мед. журн. 2002. Т. 10. № 5. С. 255.
7. Современные ингаляционные устройства для лечения респираторной патологии: отчет рабочей группы Европейского респираторного общества и Международного общества по использованию аэрозолей в медицине // Пульмонология. 2011. № 6. С. 17.
8. Labiris N.R., Dolovich M.B. // Br. J. Clin. Pharmacol. 2003. V. 56. № 6. P. 588.
9. Esposito-Festen J.E. et al. // Br. J. Clin. Pharmacol. 2007. V. 64. № 3. Р. 328.
10. Lindström M. Particles in Small Airways: Mechanisms for Deposition and Clearance & Pharmacokinetic Assessment of Delivered Dose to the Lung. Stockholm, 2004.
11. Schuepp K.G. et al. // J. Aerosol Med. 2005. V. 618. № 2. Р. 225.
12. Newman S.P. et al. // Eur. J. Respir. Dis. Suppl. 1982. V. 119. P. 57.
13. Usmani O.S. et al. // Am. J. Respir. Crit. Care Med. 2005. V. 172. № 12. P. 1497.
14. Laube B.L. et al. // Eur. Respir. J. 2011. V. 37. № 6. P. 1308.
15. Княжеская Н.П., Новиков Ю.К. // Атмосфера. Пульмонология и аллергология. 2007. № 3. С. 37.
16. Integration of Dose Counting Mechanisms into MDI Drug Products // http://www.fda.gov/drugs/guidancecompliance regulatoryinformation/guidances/ucm064981.htm
17. Инструкция по медицинскому применению препарата Тевакомб ЛСР-008795/10 (изменение № 2 от 03.07.2013 г.).
18. Wasserman R.L. et al. // Allergy Asthma Proc. 2006. V. 27. № 6. P. 486.
19. Roller C.M. et al. // Eur. Respir. J. 2007. V. 29. P. 299.
20. Barry P.W., O’Callaghan C. // Br. J. Clin. Pharmacol. 1995. V. 40. P. 76.
21. Локшина Э.Э. и др. // Атмосфера. Пульмонология и аллергология. 2012. № 4. С. 41.
22. Bentur L. et al. // Pediatr. Pulmonol. 2004. V. 38. P. 304.
23. Zierenberg B. // J. Aerosol Med. 1999. V. 12. Р. 19.
24. Newman S.P. et al. // Chest. 1998. V. 113. P. 957.
25. Татарский А.Р. и др. // Consilium Medicum. 2007. Т. 9. № 3. С. 70.
26. Dennis J.H. // J. Aerosol Med. 1998. V. 11. P. 73.
27. Dhand R. // Respir. Care. 2002. V. 47. P. 1406.
28. Siefkin A.D. // Am. J. Med. 1996. V. 100. Suppl. 1A. P. 54S.
29. Авдеев С.Н. Небулайзерная терапия суспензией Пульми-корта: место в лечении заболеваний дыхательных путей: Метод. пособ. для врачей. 2-е изд., перераб. и доп. М., 2008.
Статья подготовлена при поддержке ООО «Тева», Россия, Москва, 119049, ул. Шаболовка, 10, корп. 2, Бизнес-центр «Конкорд», сектор А, 3-й этаж.
ср ó о о
о eq
Н
К <<
м S о
о >
н н
н о
¡H
и о
НИИ пульмонологии МЗ РФ, Москва
При заболеваниях дыхательных путей (бронхиальная астма, хроническая обструктивная болезнь легких и др.) основной способ введения лекарственных препаратов – ингаляция медицинских аэрозолей (b2–агонисты, антихолинергические препараты, глюкокортикостероиды, кромоны). Ингаляционные устройства представляются наиболее логичными и эффективными, так как лекарственный препарат непосредственно направляется к тому месту, где он должен действовать – в дыхательные пути. Можно выделить следующие преимущества ингаляционного способа введения лекарств: более быстрое начало действия лекарственного средства, требуется меньшая доза препарата, снижается риск развития побочных эффектов.
Любая ингаляционная техника предназначена для доставки лекарственного препарата в дыхательные пути. Одним из главных параметров эффективности ингаляционного устройства является такая величина, как депозиция (т.е. отложение) препарата в дыхательных путях. Легочная депозиция препаратов при использовании различных систем доставки колеблется в пределах от 4 до 60% от отмеренной дозы.
Основные механизмы депозиции – инерционное столкновение, седиментация (оседание) и диффузия (Swift, 1985). Депозиция аэрозоля путем инерционного столкновения происходит, когда инерция частицы не в состоянии обеспечить ее дальнейшее движение с потоком воздуха при изменении направления потока. Такой механизм имеет место в верхних дыхательных путях, в глотке, гортани и в местах бифуркации дыхательных путей. Седиментация (оседание) ответственна за депозицию частиц аэрозоля, не подвергнувшихся столкновению при вхождении в легкие. Седиментация увеличивается при задержке дыхания и при медленном, спокойном дыхании. Броуновская диффузия является важнейшим механизмом, ответственным за депозицию в легких частиц размерами менее 0,5 мкм. Такая депозиция имеет место в дистальных, газообменных отделах легких и составляет очень малую долю общей легочной депозиции терапевтического аэрозоля.
Основным фактором, определяющим депозицию частиц в дыхательных путях, является размер частиц аэрозоля. В аэрозольной медицине принято использовать следующие понятия:
- Срединный массовый аэродинамический диаметр частиц (mass median aerodynamic diameter: MMАD) – определяется тем, что половина массы аэрозоля содержится в частицах большего диаметра, а другая половина – в частицах меньшего диаметра.
- Респирабельные частицы – частицы с аэродинамическим диаметром < 5 мкм.
- Респирабельная фракция – доля респирабельных частиц в аэрозоле, выраженная в процентах.
Условно распределение частиц аэрозоля в дыхательных путях в зависимости от их размера можно представить следующим образом (Task Group, 1966):
- 5–10 мкм – осаждение в ротоглотке, гортани и трахее
- 2–5 мкм – осаждение в нижних дыхательных путях
- 0,5–2 мкм – осаждение в альвеолах
- менее 0,5 мкм – не осаждаются в легких.
Существует четкая зависимость между легочной депозицией и клиническим эффектом препарата. Для бронхорасширяющих препаратов эта зависимость линейная. Так, при изучении клинической эффективности системы доставки Respimat было показано, что ингаляционная система, обеспечивающая 4–кратный рост легочной депозиции препарата по сравнению с дозированным ингалятором, позволяет уменьшить дозировку препарата беродуал также примерно в 4 раза (Goldberg et al., 2001).
Успешная ингаляционная терапия зависит не только от правильного выбора препарата, но и от адекватного способа доставки лекарства в дыхательные пути. Идеальное устройство доставки должно обеспечивать депозицию большой фракции препарата в легких, быть достаточно простым в использовании, надежным, доступным для применения в любом возрасте и при тяжелых формах заболевания.
В настоящее время существует несколько типов систем доставки:
- дозированные аэрозольные ингаляторы (ДАИ)
- комбинация дозированных ингаляторов со спейсерами
- порошковые ингаляторы
- небулайзеры.
Дозированные аэрозольные ингаляторы
Дозированные аэрозольные ингаляторы (ДАИ) являются наиболее известными и распространенными в мире системами доставки лекарственных аэрозолей. Первый ДАИ Medihaler™ был изготовлен в 1956 г., сначала в стеклянном, а с 1963 г. – в алюминиевом корпусе (Huchon, 1997).
В классическом ДАИ под давлением содержатся микронизированный препарат в виде суспензии и пропеллент фреон (Ф), представляющий собой хлорфторуглерод (chlorofluorocarbon – CFC). Кроме того, для смазывания клапана и сохранения лекарственного вещества в виде суспензии в состав ДАИ входит также и сурфактант (рис. 1). Обычно лишь около 30–40% всех частиц аэрозоля, генерируемого ДАИ, находятся в пределах респирабельных размеров (менее 5 мкм).
Рис. 1. Генерация аэрозоля с помощью ДИ. А — канистра, В — клапан, С — мундштук
Достоинствами ДАИ является их удобство, портативность, быстрота выполнения процедуры, низкая стоимость. Высвобождаемая из ДАИ доза препарата хорошо воспроизводима. Однако несмотря на относительную простоту, ДАИ имеют серьезные недостатки. Главные проблемы связаны с использованием фреона, который создает высокоскоростное «облако» аэрозоля (скорость более 30 м/с) в течение короткого отрезка времени. Высокая скорость аэрозоля приводит к массивной депозиции препарата на задней стенке глотки (около 80%), в то время как легочная депозиция обычно не превышает 10% от отмеренной дозы; еще около 10% дозы остается в ингаляторе (Newman et al., 1984). Другим недостатком, связанным с фреоном, является его низкая температура (до –30°С), что при его контакте с мягким небом может приводить к рефлекторному прерыванию вдоха – так называемый эффект холодного фреона.
Еще одно последствие высокой скорости аэрозоля – сложность координации вдоха с высвобождением препарата из ингалятора. Неправильно используют ДАИ от 8 до 54% всех больных бронхиальной астмой (БА) (мета–анализ Cochrane et al., 2000). Правильная ингаляционная техника позволяет добиться значительного эффекта при доставке препарата в легкие. У больных с хорошей координацией вдоха и высвобождения аэрозоля легочная депозиция препарата (18,6%) почти втрое больше, чем у пациентов с неадекватной техникой использования ДАИ (7,2%) (Newman et al., 1991). Обучение больных правилам ингаляции значительно снижает остроту проблемы координации, хотя до 20% всех пациентов все же не способны правильно пользоваться ДАИ. Озабоченность вызывает то, что даже медицинский персонал при демонстрации ингаляционной техники допускает порой не меньше ошибок, чем больные (табл. 1).
Оптимальная техника ингаляции – медленный вдох (инспираторный поток около 30 л/мин) с последующей задержкой дыхания до 10 сек (Pedersen, 1996). При этом требуется встряхивать ДАИ перед каждой ингаляцией: лекарственный препарат в резервуаре ингалятора находится в виде суспензии, а по тому необходимо равномерно распределять его перед ингаляцией.
К недостаткам ДАИ относятся также постепенное снижение эффективности препарата по мере его хранения и непредсказуемые колебания его дозы после использования заданного количества доз – «феномен остатка». Данный феномен означает, что после высвобождения номинальных 200 доз препарата в камере ДАИ может оставаться еще до 20 доз, однако содержание в них лекарственного вещества очень сильно варьирует (June, 1997), что негативно влияет на результативность терапии в целом.
Наконец, существенный недостаток классических ДАИ – наличие в них фреонов, участвующих в повреждении озонового слоя атмосферы, что ведет к глобальному потеплению климата («парниковый эффект»).
Бесфреоновые ДАИ
Для замены фреонов были предложены другие пропелленты – гидрофторалканы (HFA–134a) (June, 1997). В отличие от фреона, HFA не содержит атома хлора, не вызывает разрушения озонового слоя, имеет очень низкую химическую реактоспособность; период сохранения в стратосфере составляет около 15 лет, и к тому же он обладает меньшим (примерно в 6 раз) потенциалом создания «парникового эффекта» (Tashkin, 1998). Новый пропеллент HFA абсолютно не токсичен, имеет очень низкую растворимость в воде и липидах (Leach, 1997). Создание новых ДАИ с пропеллентом HFA привело не просто к замене наполнителя, а к полному изменению технологии ДАИ. В бесфреоновых ДАИ лекарственный препарат содержится не в виде суспензии, а в виде раствора (для его стабилизации используется этанол, олеиновая кислота или цитраты). Новшество сделало ненужным предварительное взбалтывание содержимого ингалятора, однако больной может ощущать появившийся привкус алкоголя.
Достоинством бесфреоновых ДАИ является создание низкоскоростного «облака» аэрозоля, что приводит к значительно меньшей депозиции препарата в ротоглотке и меньшему риску развития эффекта холодного фреона (температура «облака» около 3°С) (Lipworth, 2000). Бесфреоновые ДАИ лишены таких недостатков классических ДАИ, как потеря дозы, «феномен остатка»; они могут функционировать даже при низких температурах окружающей среды (June, 1997).
Создание новых ДАИ с наполнителем HFA позволило также уменьшить и размер частиц аэрозоля. Например, MMAD частиц, образуемых ДАИ с беклометазоном–HFA, значительно меньше, чем у обычного ДАИ с беклометазоном–Ф – 1,1 мкм против 3,5 мкм (Lipworth, 2000). Изменение размера частиц аэрозоля влияет на величину легочной депозиции препарата. Так, при использовании ДАИ беклометазона–HFA депозиция у больных БА достигает 56% по сравнению с 4% при применении ДАИ беклометазона–Ф (Leach, 1998). Очевидно, такое различие требует пересмотра доз ингаляционных глюкокортикостероидов – для обеспечения контроля симптомов БА с помощью ДАИ беклометазона–HFA достаточно дозы в 2,6–3,2 раза меньше обычной (Lipworth, 2000).
ДАИ, активируемые вдохом
ДАИ, активируемые вдохом, были созданы для преодоления проблемы координации вдоха и активации ингалятора. К таким ингаляторам относятся Autohaler (3M Pharmaceutical), Easy–Breath (зарегистрирован в России под названием «Легкое Дыхание», Baker Norton) и Breath–Operated Inhaler (Baker Norton). Их главным отличием является пружинный механизм, который взводится либо открытием колпачка (Легкое Дыхание, рис. 2), либо поднятием специального рычажка (Autohaler). В ответ на вдох (средний инспираторный поток 20 и 30 л/мин) в течение 0,2 с происходит высвобождение дозы препарата. Легочная депозиция препаратов достигает значений в 2 раза больших по сравнению с обычными ДАИ (18–21%) (Newman, 1991).
Рис. 2. Устройство ДАИ <Легкое Дыхание>А — клапан, В — пружина, С — диафрагма, D — пусковое устройство, E — держатель баллончика
Клинические исследования показали, что больные очень быстро обучаются ингаляционной технике с использованием ДАИ, активируемых вдохом (Crompton & Duncan, 1989). В исследовании Lenney et al. (2000) хорошая техника ингаляции с помощью ДАИ «Легкое Дыхание» и Autohaler была продемонстрирована у 91% больных. Кроме того, активируемые вдохом ДАИ являются устройствами, которым больные чаще всего отдают предпочтение по сравнению со всеми другими системами для ингаляций.
Комбинация ДАИ со спейсерами
Спейсер представляет собой объемную камеру, которая соединяет дозированный ингалятор и дыхательные пути больного. Спейсеры позволяют решать проблемы координации вдоха пациента и высвобождения лекарственного препарата, а также уменьшить орофарингеальную депозицию препарата и связанные с ней местные побочные эффекты. Выполняя роль аэрозольного резервуара, спейсеры замедляют скорость струи аэрозоля и увеличивают время и дистанцию пути аэрозоля от ДАИ до рта пациента, в результате чего в дыхательные пути больного проникают частицы малого размера, а более крупные оседают на стенках камеры (рис. 3).
Рис. 3. Схема спейсеров. А — ДИ, В — камера спейсера, С — однонаправленный клапан, D — загубник (сверху), Е — маска
Спейсеры снижают риск эффекта «холодного фреона» и преждевременного прекращения вдоха. Техника использования спейсеров намного проще по сравнению с ДАИ, что делает возможным их применение у пациентов практически всех возрастных категорий, включая и детей.
Оптимальной техникой ингаляции аэрозоля через спейсер является глубокий медленный вдох (инспираторный поток около 30 л/мин) или два спокойных глубоких вдоха (до 4–5 вдохов для детей) после высвобождения одной дозы в камеру небулайзера, или даже обычное спокойное дыхание – для детей. Достоинством спейсера является возможность отсрочки выполнения ингаляции после высвобождения препарата до нескольких секунд без снижения клинического эффекта аэрозольной терапии. Однако очень длительная пауза (более 5–10 секунд) снижает количество респирабельных частиц, поэтому следует стремиться к максимально быстрому выполнению вдоха после активации ингалятора, особенно при использовании спейсеров малого объема. Необходимо также помнить: ингаляция аэрозоля из спейсера должна производиться после каждого высвобождения препарата в камеру спейсера (одна доза – один вдох).
Все спейсеры значительно снижают орофарингеальную депозицию лекарственных препаратов – до 17% (Newman SP et al., 1984), что ведет к уменьшению местных побочных эффектов при использовании глюкокортикостероидов (кандидоз и дисфония) и системных эффектов при применении b2–агонистов вследствие уменьшения абсорбции препарата со слизистых желудочно–кишечного тракта.
Спейсеры приводят к значительному увеличению депозиции препарата в легких по сравнению с ДАИ (в 2–4 раза). По данным исследований с использованием радиоактивной метки, легочная депозиция препаратов при ингаляции через систему спейсер–ДАИ составляла 21–45% (Newman SP et al., 1984; Pierart et al., 1999).
Объем спейсера является важной характеристикой. Считается, что спейсеры большого объема (750 мл: Volumatic, Nebuhaler) более эффективны по сравнению со спейсерами меньших объемов. Однако Agerhort и Pedersen (1994) показали сходную клиническую эффективность ингаляционного будесонида при сравнении ингаляций через Babyspacer (200 мл, 23 см) и Nebuhaler (750 см, 23 см), а в исследовании Bisgaard et al. (1995) поликарбоновые спейсеры по степени эффективности были расположены в следующем порядке: Babyhaler (350 мл, 23 см), Nebuhaler и Aerochamber (145 мл, 11 см). Эти данные говорят в пользу того, что эффективность спейсера определяется не столько объемом, сколько его длиной.
Металлические спейсеры (Nebuchamber), по сравнению с пластиковыми (поликарбоновыми) системами, обладают антистатическими свойствами, т.е. не имеют электростатического заряда на своей поверхности и не вызывают повышенного осаждения частиц аэрозоля (Barry & O’Callaghan, 1999). Электростатический заряд является значимым фактором, влияющим на выход аэрозоля при использовании пластиковых спейсеров. Для решения данной проблемы предлагается создание антистатического покрытия на поверхности спейсера, что может быть достигнуто либо «примированием» устройства лекарственным препаратом, либо обработкой спейсера ионными детергентами. «Примирование» нового или вымытого спейсера создается впрыскиванием в него нескольких доз из ДАИ (обычно около 15 доз), вследствие чего образуется тонкий антистатический слой (Pedersen, 1996). Обработка спейсера ионными детергентами является очень эффективным методом: она обеспечивает повышение легочной депозиции препаратов от 11,5 до 45,6% – в 4 раза (Pierart et al., 1999).
Оборудование спейсеров лицевыми масками позволяет использовать данный тип доставки аэрозоля у детей до 3 лет (O’Callaghan & Barry, 1995).
Основным недостатком спейсеров является их относительная громоздкость, что затрудняет их использование больными вне дома.
Порошковые ингаляторы
Первым порошковым ингалятором (ПИ) явился ингалятор Spinhaler, созданный для доставки в легкие высоких доз кромогликата натрия (Bell et al., 1971). Новый тип ингалятора сразу привлек к себе внимание, так как в основу работы устройства был положен принцип высвобождения лекарственного препарата в ответ на инспираторное усилие больного (активация вдохом). Тем самым решалась проблема координации.
ПИ используют лекарственное вещество в сухом виде (порошок), которое при помощи энергии вдоха пациента доставляется в его дыхательные пути. В ПИ препарат находится в виде больших агрегатов (около 60 мкм) либо в чистом виде – Turbuhaler (AstraZeneca), либо, в большинстве случаев, в соединении с носителем – лактозой или бензоатом натрия – Циклохалер (Пульмомед). Во время вдоха больного в ингаляторе создаются турбулентные потоки и часть лекарственного вещества, проходя через устройство, «разбивается» до частиц респирабельных размеров. Эти респирабельные частицы сухого вещества аэродинамически более стабильны, нежели частицы ДАИ, так как транспортируются в легкие со скоростью потока воздуха, а не со скоростью струи пропеллента, не меняют своего размера и формы после высвобождения из устройства, а по тому обеспечивают большую депозицию препарата в легких – до 40% (табл. 2). Частицы, которые не подверглись микронизации, в т.ч. и с носителем, оседают в ротоглотке, причем для ПИ орофарингеальная депозиция по–прежнему остается довольно значимой проблемой (50–80%) (Pedersen, 1996).
Достоинствами ПИ являются (как и у ДАИ) их портативность, компактность, удобство и относительная простота использования (не у всех моделей!). В отличие от ДАИ порошковые ингаляторы не используют фреоны. Нельзя не отметить, что переход на бесфреоновые формы ингаляционных устройств в течение последнего десятилетия значительно стимулировал появление новых моделей ПИ.
Зависимость функционирования ПИ от инспираторного потока больного может быть не только достоинством (хорошая координация), но и недостатком, поскольку доставка препарата в дыхательные пути может находиться в прямой связи с величиной инспираторного потока. Некоторые ПИ для преодоления сопротивления ингалятора требуют относительно высокого инспираторного потока (60 л/мин), что иногда становится проблемой при их использовании у детей и в случаях тяжелого бронхоспазма. Например, Newman et al. (1991) показали, что при использовании Turbuhaler (AstraZeneca) легочная депозиция тербуталина составляла 35% при инспираторном потоке 60 л/мин и 8,9% – при потоке 15 л/мин. Другой проблемой ПИ, связанной с инспираторным усилием больного, является более высокая вариабельность высвобождаемой дозы препарата по сравнению с ДАИ. Ингалятор Aerolizer (Novartis), ранее называвшийся Ciclohaler, имеет умеренное сопротивление, что позволяет применять его при более низких инспираторных потоках (30 л/мин) (Chew et al., 2001). Однако эффективность Aerolizer также зависит от величины потока. В исследовании in vitro показано снижение фракции респирабельных частиц с уменьшением инспираторного потока: MMAD аэрозольных частиц составлял 7,2 и 5,3 мкм при потоках 40 л/мин и 80 л/мин, соответственно (Zanen et al., 1992).
Новые ПИ, такие как HandiНaler (Boehringer Ingelheim) и Clickhaler (ML Laboratories PLC), не меняют свой профиль функционирования и при таких низких потоках, как 15–30 л/мин (Chodosh et al., 2001; Newhouse et al., 1999).
Эффективность работы практически всех ПИ зависит от инспираторного потока. В свою очередь, инспираторный поток через ингаляционную систему зависит от двух факторов – внутреннего сопротивления устройства и инспираторного усилия пациента. По уровню внутреннего сопротивления потоку ПИ можно расположить в следующем порядке: Inhaler M (Boehringer Ingelheim) > Easyhaler (Orion) > Turbuhaler (AstraZeneca) > Novolizer (Sofotec) > Diskus (GlaxoSmithKline) > Aerolizer (Novartis) > Diskhaler (GlaxoSmithKline) > Rotahaler (GlaxoSmithKline) (Fyrnys et al., 2001). Низкое сопротивление устройства, безусловно, дает возможность достичь высокого инспираторного потока при менее интенсивном усилии больного и позволяет использовать ПИ с низким сопротивлением даже при тяжелом бронхоспазме.
С другой стороны, при ингаляции через ПИ с низким сопротивлением инспираторный поток может достичь очень высоких значений, вследствие чего депозиция респирабельных частиц в ротоглотке значительно увеличивается, а в периферических дыхательных путях – снижается. Поэтому, например, оптимальные значения легочной депозиции достигаются при использовании ПИ с высокими-средними внутренними сопротивлениями потоку: Turbuhaler (20–35%), Novolizer (20–32%), Easyhaler (18– 29%), а худшие показатели – при использовании ПИ с низкими сопротивлениями: Rotahaler (6–11%), Spinhaler (6–12%), Diskhaler (11–15%).
При использовании ПИ больным рекомендовано вдыхать через устройство с максимальным усилием – такой прием позволяет обеспечить максимальный инспираторный поток, что ведет к повышению респирабельной фракции аэрозоля. Однако, с другой стороны, очень быстрая ингаляция снижает депозицию в периферических отделах бронхиального дерева, что особенно актуально для ПИ с низким сопротивлением. Задержка дыхания после ингаляции, наклон головы и вдох от уровня более низких легочных объемов не влияют на эффективность ПИ (Pedersen, 1996). Необходимо помнить, что при использовании ПИ пациент не должен выдыхать в ингалятор перед ингаляцией, чтобы не «выдуть» дозу из ингалятора.
По типу дозирования лекарственного препарата все ПИ можно разделить на несколько классов (Цой, 1997; Огородова, 1999):
- однодозовые капсульные
- мультидозовые резервуарные
- мультидозовые блистерные.
Самые ранние модели ПИ (Rotahaler и Spinhaler) и более современные (Aerolizer и Handihaler) используют желатиновую капсулу с лекарственным препаратом. Достоинством капсульных моделей ПИ является точность дозирования препарата, компактный размер устройств, защита лекарственной субстанции от влажности, возможность назначения большой дозы препарата (до 20–30 мг) и низкая стоимость ингалятора. К недостаткам можно отнести неудобство, связанное с частой заправкой ингалятора, и технические проблемы: неадекватное вскрытие капсулы, застревание капсулы в камере ингалятора и возможность ингаляции частиц капсулы (Nielsen et al., 1997). Необходимость заправки ПИ перед каждой ингаляцией не становится большой проблемой при ингаляции бронхолитиков пролонгированного действия – формотерола (Foradil Aerolizer) или тиотропиума бромида (Spiriva HandiНaler), когда требуется использование ингалятора не чаще 1–2 раз в сутки, однако это может вызвать достаточные неудобства при использовании ПИ с другими препаратами, требующими ингаляции чаще 3 раз в сутки.
Более удобны с этой точки зрения мультидозовые резервуарные ПИ (Turbuhaler, Easyhaler, Novolizer, Clickhaler, Airmax, Pulvinal, Циклохалер, Twisthaler), которые по концепции дозирования приближаются к ДАИ. Недостатки резервуарных ПИ – вариабельность дозы, ограничение дозы размером резервуара, сложность устройства и более высокая стоимость. Кроме того, проблемой данного класса ПИ является их влагочувствительность. Абсорбция влаги из окружающей среды или во время использования ингалятора пациентом может повлиять на взаимодействие между частицами препарата или носителя, значительно уменьшив образование респирабельного аэрозоля.
Компромиссом между капсульными и резервуарными ПИ являются мультидозовые блистерные ПИ, в которых используется несколько запакованных в блистеры доз, в виде диска (4 и 8 доз) – Diskhaler или полоски (60 доз) – Diskus. Блистерные ингаляторы успешно решают проблему защиты лекарственного вещества от влаги и обеспечивают довольно высокую точность дозирования.
Немаловажный аспект использования ПИ – их простота и удобство. Наиболее сложной системой является Diskhaler, использование которого требует выполнения особого 5–ступенчатого алгоритма. Достаточно просты Easyhaler, Clickhaler и Airmax™, которые по своей форме напоминают ДАИ. Впрочем, и сама процедура ингаляции через них требует таких же навыков, как при использовании ДАИ: встряхивание и нажатие на дно устройства (или просто открывание мундштука – при использовании Airmax) с последующим вдохом. Такой фактор, как наличие цифрового счетчика доз (Turbuhaler, Easyhaler, Clickhaler, Novolizer, Diskus), также значительно облегчает использование ПИ и улучшает комплайнс к ингаляционной терапии.
Небулайзеры
Самую длительную историю использования имеют небулайзеры – они применяются уже почти 150 лет. Слово «небулайзер» происходит от латинского «nebula» (туман, облачко), впервые было употреблено в 1874 г. для обозначения «инструмента, превращающего жидкое вещество в аэрозоль для медицинских целей» (Muers, 1997). Один из первых портативных «аэрозольных аппаратов» был создан J.Sales–Girons в Париже в 1859 г. Небулайзеры тогда использовали в качестве источника энергии струю пара, и применялись они для ингаляции паров смол и антисептиков у больных туберкулезом.
В настоящее время в зависимости от вида энергии, превращающей жидкость в аэрозоль, различают два основных типа небулайзеров: 1) струйные или компрессорные, пневматические – использующие струю газа (воздух или кислород); 2) ультразвуковые – использующие энергию колебаний пьезокристалла.
Продукция аэрозоля в ультразвуковом небулайзере практически бесшумная и более быстрая по сравнению со струйными. К числу недостатков относятся: неэффективность образования аэрозоля из суспензий и вязких растворов; как правило, больший остаточный объем; повышение температуры лекарственного раствора во время небулизации и вероятность разрушения структуры лекарственного препарата (Nikander, 1994).
Преимущества небулайзеров: легкая техника ингаляция (спокойное дыхание), отсутствие потребности в форсированном маневре, возможность использования системы даже при самых тяжелых состояниях (астматический статус), у пожилых и у детей, при двигательных расстройствах, при нарушениях уровня сознания.
Достоинством небулайзеров является возможность доставки большой дозы препарата (в случае необходимости во время ингаляции допускается использование кислорода).
Задачей ингаляционной терапии при помощи небулайзера является продукция аэрозоля с высокой пропорцией (> 50%) респирабельных частиц (менее 5 мкм) в течение довольно короткого временного интервала, обычно не более 10–15 минут (Muers, 1997).
Эффективность продукции аэрозоля, свойства аэрозоля и его доставка в дыхательные пути зависят от типа небулайзера, его конструкционных особенностей, объема наполнения и остаточного объема, величины потока рабочего газа, «старения» небулайзера, сочетания системы компрессор–небулайзер и др. (Авдеев, 2001).
Несмотря на сходный дизайн и конструкцию, небулайзеры разных моделей могут существенно отличаться по своим показателям. В исследовании Loffert et al. (1994) при сравнении 17 типов струйных небулайзеров in vitro было установлено, что различия в выходе аэрозоля достигали 2 раз, в величине респирабельной фракции аэрозоля – 3,5 раз, а в скорости доставки частиц респирабельной фракции препаратов – 9 раз. В другом исследовании при сравнении эффективности доставки аэрозоля (8 небулайзеров) было показано, что средняя депозиция препарата в легких различалась в 5 раз, а средняя орофарингеальная депозиция – в 17 раз (Thomas et al., 1991).
Типы струйных небулайзеров. Различают три основных типа струйных небулайзеров (Knoch & Sommer E. 2000).
Конвекционный (обычный) небулайзер является наиболее распространенным типом систем доставки. Такой небулайзер производит аэрозоль с постоянной скоростью, во время вдоха происходит вовлечение воздуха через Т–трубку и разведение аэрозоля. Аэрозоль поступает в дыхательные пути только во время вдоха, а во время выдоха аэрозоль попадает во внешнюю среду, т.е. происходит потеря большей его части (около 55–70%) (Jackson W.F., 1998). Легочная депозиция препаратов при использовании таких небулайзеров относительно невелика – до 10%.
Небулайзеры, активируемые вдохом (известные также, как небулайзеры Вентури): продуцируют аэрозоль постоянно на протяжении всего дыхательного цикла, однако высвобождение аэрозоля усиливается во время вдоха. Такой эффект достигается благодаря поступлению дополнительного потока воздуха во время вдоха через специальный клапан в область продукции аэрозоля, общий поток увеличивается, что ведет и к увеличению образования аэрозоля. Таким образом, соотношение выхода аэрозоля во время вдоха и выдоха увеличивается (до 70:30), повышается количество вдыхаемого препарата, снижается потеря препарата, а время небулизации сокращается (Jackson W.F, 1998). Небулайзеры Вентури позволяют добиться вдвое большей депозиции препарата в дыхательных путях по сравнению с обычным небулайзером (до 19%) (Devadason SG, 1997).
Небулайзеры, синхронизованные с дыханием (дозиметрические небулайзеры), производят аэрозоль только во время фазы вдоха. Генерация аэрозоля во время вдоха обеспечивается при помощи электронных сенсоров потока либо давления, и теоретически выход аэрозоля во время вдоха достигает 100%. Основным достоинством дозиметрического небулайзера является снижение потери препарата во время выдоха (Nicander, 1997).
Новые виды ингаляционных систем
Ингалятор Respimat (Boehringer Ingelheim) является представителем нового класса ингаляционных систем – жидкостных дозированных ингаляторов (Ganderton, 1999). Устройство имеет съемные картриджи, поворот корпуса взводит пружину. При активации ингалятора раствор проходит через сопло с двумя сходящимися каналами. На выходе из них образуются две жидкостных струи, их столкновение друг с другом формирует медленнодвижущееся «облако» аэрозоля (10 м/с). Устройство имеет компактный дизайн и снабжено цифровым счетчиком доз. Легочная депозиция аэрозоля при использовании достигает 45%, а орофарингеальная депозиция колеблется от 26 до 54% (Dolovich, 1999).
Заключение
На сегодняшний день практически все рассмотренные выше системы доставки аэрозолей имеют не только достоинства, но и недостатки (табл. 3). Аэрозольные технологии – бурно развивающееся направление медицины. Практически каждый год на мировом рынке появляется несколько новых ингаляционных устройств, приближающих нас к заветной цели – созданию «идеального ингалятора». Идеальный ингалятор характеризуют свойства аэрозольного «облака», удобство устройства для больного и общие фармакологические аспекты (Ganderton, 1999).
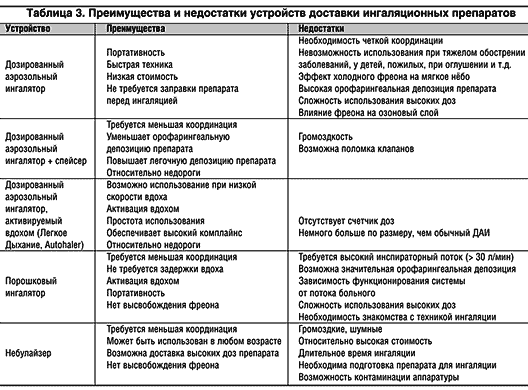
Условно требования к идеальному ингалятору можно представить следующим образом.
1. Свойства аэрозольного «облака».
- Генерация аэрозольного «облака» должна быть независимой от инспираторного потока больного.
- Генерация аэрозоля должна быть довольно продолжительной, в среднем время генерации аэрозоля более 1 секунды позволяет решить проблему координации вдоха.
- Аэрозоль должен состоять из частиц менее 5 мкм. Частицы меньших размеров необходимы для доставки препарата в периферические отделы дыхательных путей. Возможность варьировать средний размер частиц аэрозоля и распределение может стать дополнительным преимуществом.
- Скорость аэрозольного «облака» должна быть низкой для снижения орофарингеальной депозиции препарата и обеспечения большей доставки препарата в легкие.
2. Удобство использования ингалятора пациентом.
- Простота использования.
- Размеры, близкие к размерам ДАИ.
- Ингалятор должен содержать большое количество доз (более 50).
- Предпочтительно наличие цифрового счетчика доз.
3. Общие фармакологические аспекты.
- Разумная цена ингаляционного устройства.
- Ингалятор должен создавать одинаковую дозу препарата на протяжении всего срока использования, не быть подверженным контаминации и иметь длительный срок службы.
- Отсутствие пропеллента.
Литература:
1. Swift DL. Aerosol characteristics and generation. In: Moren F, Dolovich MB, Newhouse MT, et al., eds. Aerosols in medicine; principles, diagnosis and therapy. Elsevier Science (Biomedical Division), New York, 1985; 53–76
2. Task Group on Lung Dynamics. Deposition and retention models for internal dosimetry of the human respiratory flow; tract. Health Physics 1966;12:173–208.
3. Goldberg J, Freund E, Beckers B, Hinzmann R. Improved delivery of fenoterol plus ipratropium bromide using Respimat( compared with conventional metered dose inhaler. Eur Respir J 2001; 17: 225– 232.
4. Huchon G. Metered dose inhalers part and present: advantages and limitations. Eur Respir Rev 1997; 7: 41, 26– 28.
5. Newman SP, Millar AB, Lennard–Jones TR, et al. Improvement of pressurised aerosol deposition with Nebuhaler spacer device. Thorax 1984; 39:935–941
6. Cochrane MG, Bala MV, Downs KE, Mauskopf J, Ben–Joseph RH. Inhaled corticosteroids for asthma therapy. Patient compliance, devices, and inhalation technique. Chest 2000; 117: 542– 550.
7. Newman SP, Weisz AWB, Talaee N, et al. Improvement of drug delivery with a breath actuated pressurised aerosol for patients with poor inhaler technique. Thorax 1991; 46:712–716
8. Pedersen S. Inhalers and nebulizers: which to choose and why. Respi Med 1996; 90: 69– 77.
9. June D. Achieving to change: challenges and successes in the formulation of CFC–free MDIs. Eur Respir Rev 1997; 7, 41: 32– 34.
10. Tashkin DP. New devices for asthma. J Allerg Clin Immunol 1998; 101: S409– S416.
11. Leach CL. Safety asessment of the HFA propellant and the new inhaler. Eur Respir Rev 1997; 7: 41, 35– 36.
12. Lipworth BJ. Targets for inhaled treatment. Respir Med 2000; 94(suppl D): S13– S16.
13. Leach CL. Safety asessment of the HFA propellant and the new inhaler. Improved delivery of inhaled steroids to the large and small airways. Respir.Med. 1998; 92(Suppl.A): 3– 8.
14. Lenney J, Innes JA, Crompton GK. Inappropriate inhaler use: assessment of use and patient preference of seven inhalation devices. EDICI. Respir Med 2000; 94: 496– 500.
15. Crompton G, Duncan J. Clinical assessment of a new breath–actuated inhaler. Practitioner 1989;233:268–9.
16. Newman SP, Millar AB, Lennard–Jones TR, et al. Improvement of pressurised aerosol deposition with Nebuhaler spacer device. Thorax 1984; 39:935–941
17. Pierart F, Wildhaber JH, Vrancken I, Devadason SG, Le Souel PN. Washing plastic spacers in household detergent reduces electrostatic charge and greatly improves delivery. Eur Respir J 1999; 13: 673– 678.
18. Agertoft L, Pedersen S. Influence of spacer device on drug delivery to young children with asthma. Arch Dis Child 1994;71:217–20.
19. Bisgaard H, Anhoj J, Klug B, Berg E. A non–electrostatic spacer for aerosol delivery. Arch Dis Child 1995;73:226–30.
20. Barry PW, O’Callaghan C. The output of budesonide from spacer devices assessed under simulated breathing conditions. J Allergy Clin Immunol 1999; 104: 1205– 1210.
21. Barry PW, O’Callaghan C. The optimum size and shape of spacer devices for inhalational therapy. J Aerosols Med 1995;8:303–5.
22. Bell JH, Hartley PS, Cox JSG. Dry powder aerosols. I. A new powder inhalation device. J Pharm Sci 1971; 78: 176– 180.
23. Newman SP, Moren F, Trofast E, Talaee N, Clarke SW. Terbutaline sulphate Turbuhaler effect of inhaled flow rate on drug deposition and efficacy. Int J Pharmaceutics 1991;74:209–13
24. Chew NY, Chan HK. In vitro aerosol performance and dose uniformity between the Foradile Aerolizer and the Oxis Turbuhaler. J Aerosol Med 2001 Winter; 14: 495–501
25. Zanen P, van Spiegel PI, van der Kolk H, Tushuizen E, Enthoven R. The effect of the inhalation flow on the performance of a dry powder inhalation systems. Int J Pharmaceut 1992; 81: 199– 203.
26. Chodosh S, Flanders JS, Kesten S, Serby CW, Hochrainer D, Witek TJ Jr. Effective delivery of particles with the HandiHaler dry powder inhalation system over a range of chronic obstructive pulmonary disease severity. J Aerosol Med 2001 Fall; 14: 309– 315.
27. Newhouse MT, Nantel NP, Chambers CB, Pratt B, Parry–Billings RN, Parry–Billings M. Clickhaler (a novel dry powder inhaler) provides similar bronchodilation to pressurized metered–dose inhaler, even at low flow rates. Chest. 1999; 115: 952– 956.
28. Fyrnys B, Stang N, Wolf–Heuss E. Stability and performance characteristics of a budesonide powder for inhalation with a novel dry powder inhaler device. Curr Opin Pulm Med 2001; 7(suppl 1): S7– S11.
29. Огородова ЛМ. Системы ингаляционной доставки препаратов в дыхательные пути. Пульмонология 1999; № 1: 84– 87.
30. Цой АН. Преимущества и недостатки приспособлений для индивидуальной ингаляционной терапии. Пульмонология 1997; № 3: 71– 74.
31. Nielsen KG, Auk IL, Bojsen K, Ifversen M, Klug B, Bisgaard H. Clinical effect of Diskus dry–powder inhaler at low and high inspiratory flow–rates in asthmatic children. Eur Respir J 1998; 11: 350– 354.
32. Muers M.F. Overview of nebulizer treatment. Thorax 1997; 52 (Suppl.2): S25– S30.
33. Sales–Girons J. Traitement de la phtisie pulmonaire par l’inhalation des liquides pulverises et apr les fumigation de gudron. Paris, F. Savy, 1859; p. 528.
34. Nikander K. Drug delivery systems. J Aerosol Med 1994; 7(Suppl 1): S19– 24
35. Muers M.F. The rational use of nebulizers in clinical practice. Eur. Respir. Rev. 1997; 7: 189– 197.
36. Авдеев С.Н. Использование небулайзеров в клинической практике. Русский Медицинский Журнал 2001; 9, № 5(124): 189– 196.
37. Loffert D.T., Ikle D., Nelson H.S. A comparison of commercial jet nebulisers. Chest 1994; 106: 1788– 1793.
38. Thomas S.H., O’Doherty M..J., Page C.J., Nunan T.O., Bateman N.T. Which apparatus for inhaled pentamidine? A comparison of pulmonary deposition via eight nebulisers. Eur.Respir.J. 1991; 4: 616– 622.
39. Knoch M., Sommer E. Jet nebulizer design and function. Eur.Respir.Rev. 2000; 10: 183– 186.
40. Jackson W.F., Nebulised Pulmocort therapy. A scientific and practical review. Clinical visison Ltd, Oxford 1998: p. 83.
41. Devadason S.G., Everald M.L., Linto J.M., Le Souef P.N. Comparison of drug delivery from conventional versus «Venturi» ulizers. Eur.Respir.J. 1997; 10: 2479– 2483.
42. Nicander K. Adaptive aerosol delivery: the principles. Eur.Respir.Rev. 1997; 7: 385– 387
43. Ganderton D. Targeted delivery of inhaled drugs: current challenges and future goal. J Aerosol Med 1999(Suppl 1) 12: S3– S8.
44. Dolovich MB. New propellant–free technologies under investigation. J Aerosol Med 1999; 12(Suppl 1):S9–S17.
В одной капсуле содержится:
активное вещество: натрия кромогликат — 20 мг.
состав капсулы: желатин 100%.
Твердые желатиновые капсулы №2, состоящие из прозрачного бесцветного корпуса и прозрачной желтой крышечки. На капсулу нанесена надпись «SODIUM CROMOGLICATE 20 mg». Капсула содержит однородный порошок от белого до почти белого цвета.
противоаллергическое средство, стабилизатор мембран тучных клеток.
Код ATX
— R03BC01.
Фармакологические свойства
Фармакодинамика
Противоаллергическое средство, оказывает мембраностабилизирующее действие, препятствует дегрануляции тучных клеток и выделению из них гистамина, лейкотриенов, медленно реагирующей субстанции, брадикинина, простагландинов и других биологически активных веществ, предупреждает развитие бронхоспазма. В легких ингибирование медиаторного ответа предотвращает развитие как ранений, так и поздней стадии астматической реакции. Препарат наиболее эффективен для профилактики аллергических реакций немедленного типа у больных относительно молодого возраста, у которых еще не развились хронические необратимые изменения в легких. Препарат не устраняет развившийся бронхоспазм. Длительное применение уменьшает частоту приступов бронхиальной астмы и облегчает их течение, снижает потребность в бронхолитических и глюкокортикостероидных средствах.
Фармакокинетика
Абсорбция из дыхательных путей в системный кровоток после ингаляции порошка составляет 5% — 15% от принятой дозы, причем всасывание со слизистых оболочек дыхательных путей происходит довольно быстро, однако может снижаться при увеличении количества секрета. Кромогликат натрия быстро выводится из системного кровотока, в связи с чем последующие дозы, принимаемые в соответствии с рекомендованным режимом дозирования, не кумулируют. Кромогликат натрия обратимо связывается с белками плазмы (приблизительно 65%) и не метаболизируется. Выведение происходит в неизмененном виде с мочей и желчью приблизительно в одинаковых пропорциях. Период полувыведения в среднем составляет около 80 минут. Остальная часть выводится через легкие с выдыхаемым воздухом или оседает на стенках ротоглотки, затем проглатывается и выводится через кишечник.
Профилактическое лечение бронхиальной астмы, включая астму физического напряжения.
Повышенная чувствительность к кромоглициевой кислоте, беременность (I триместр), детский возраст — до 2-х лет.
С осторожностью
Почечная/печеночная недостаточность, беременность (II-III триместры), период лактации.
Способ применения и дозировка
Препарат применяется ингаляционно.
Капсулы Интала предназначены для применения только с ингалятором «Спинхалер». Их нельзя принимать внутрь.
Так как терапия Инталом по существу профилактическая, важно, чтобы пациент был проинструктирован о необходимости регулярного приема препарата в отличие от других препаратов, ингаляции которых служат для купирования приступов.
Взрослые и дети с 2-х лет
Режим дозирования одинаков для взрослых и детей.
Обычная доза: одна капсула 4 раза в день с интервалами 3-6 часов между HИМИ. В более тяжелых случаях или повышенном содержании антигена во внешней среде частота приема может быть увеличена до 6-8 раз в день (120-160 мг/сутки). Дополнительное дозирование может также иметь место для профилактики перед физической нагрузкой, вызывающей приступы удушья.
При достижении стойкого терапевтического эффекта возможен переход на минимальную поддерживающую дозу, обеспечивающую достаточный контроль над симптомами бронхиальной астмы.
Со стороны дыхательной системы: раздражение слизистой оболочки дыхательных путей (охриплость, кашель). Крайне редко — легочные инфильтраты с эозинофилией.
Со стороны пищеварительного тракта: сухость во рту, тошнота.
Со стороны нервной системы: головокружение, головная боль.
Со стороны мочевыводящей системы: задержка мочи, нарушение функции почек.
Аллергические реакции: кожная сыпь, бронхоспазм, отек гортани, ангионевротический отек, анафилаксия наблюдались менее чем у 1 из 100 тыс. пациентов.
Кромоглициевая кислота обладает низкой токсичностью, поэтому риск передозировки и развития каких-либо токсических явлений небольшой. Не требует никаких действий, кроме медицинского наблюдения.
Взаимодействие с другими лекарственными средствами
Бета-адреностимуляторы, глюкокортикостероиды, антигистаминные лекарственные средства, теофиллин усиливают действие кромогликата натрия.
Сочетанное назначение кромоглициевой кислоты и глюкокортикостероидов позволяет уменьшить дозировку последних, а в отдельных случаях полностью их отменить.
Бронхолитики необходимо принимать (ингалировать) перед ингаляцией кромогликата натрия.
Капсулы Интала не применяются для купирования приступов бронхоспазма. Так как лечение препаратом носит профилактический характер, важно не прерывать его у пациентов, на которых препарат оказывает благотворное воздействие. При необходимости отмены лечения препаратом, это следует делать постепенно, в течение недели. При этом симптомы астмы могут возобновиться. Для пациентов, принимающих глюкокортикостероиды, при приеме Интала можно снизить дозу или отменить прием глюкокортикостероидов полностью. Необходимо наблюдение за пациентами при снижении дозы глюкокортикостероидов: предпочтительная скорость снижения дозы глюкокортикостероидов — 10% в неделю. Увеличение дозы глюкокортикостероидов может быть необходимо при утяжелении течения астмы и при инфекции, повышенном содержании антигена во внешней среде. Если возможно снижение дозы глюкокортикостероидов, то не следует прекращать прием Интала до установления нового режима дозирования глюкокортикостероидов.
Лечение пациентов с почечной/печеночной недостаточностью должно проходить под постоянным врачебным контролем.
По 10 капсул в блистер из ПВХ/алюминиевой фольги.
Каждый блистер упакован в герметично закрытый пакет-саше из алюминиевой фольги/ламинированной бумаги/ полиэтилена низкой плотности.
По 3 пакет-саше вместе с инструкцией по применению в картонную пачку.
Список Б.
При температуре ниже + 30°С.
Не замораживать.
Хранить в недоступном для детей месте.
5 лет.
Не использовать по истечении срока годности, указанного на упаковке.
Условия отпуска из аптек
По рецепту.
Название и адрес изготовителя
Файсонс Лимитед (Великобритания), произведено Ай Ти Си Фарма CP Л, Италия. Виа Понтина км. 29, Помеция, Рим, Италия
Претензии потребителей направлять по адресу в России
Москва, 115035, Садовническая ул. д. 82, стр. 2.
Регистрационный номер:
П N011788/01-230108
Торговое название: Интал ®
Международное непатентованное название:
кромоглициевая кислота.
Лекарственная форма:
капсулы с порошком для ингаляций.
Состав
В одной капсуле содержится:
активное вещество: натрия кромогликат — 20 мг.
состав капсулы: желатин 100%.
Описание
Твердые желатиновые капсулы №2, состоящие из прозрачного бесцветного корпуса и прозрачной желтой крышечки. На капсулу нанесена надпись «SODIUM CROMOGLICATE 20 mg». Капсула содержит однородный порошок от белого до почти белого цвета.
Фармакотерапевтическая группа:
противоаллергическое средство, стабилизатор мембран тучных клеток.
Код ATX — R03BC01.
Фармакологические свойства
Фармакодинамика
Противоаллергическое средство, оказывает мембраностабилизирующее действие, препятствует дегрануляции тучных клеток и выделению из них гистамина, лейкотриенов, медленно реагирующей субстанции, брадикинина, простагландинов и других биологически активных веществ, предупреждает развитие бронхоспазма. В легких ингибирование медиаторного ответа предотвращает развитие как ранений, так и поздней стадии астматической реакции. Препарат наиболее эффективен для профилактики аллергических реакций немедленного типа у больных относительно молодого возраста, у которых еще не развились хронические необратимые изменения в легких. Препарат не устраняет развившийся бронхоспазм. Длительное применение уменьшает частоту приступов бронхиальной астмы и облегчает их течение, снижает потребность в бронхолитических и глюкокортикостероидных средствах.
Фармакокинетика
Абсорбция из дыхательных путей в системный кровоток после ингаляции порошка составляет 5% — 15% от принятой дозы, причем всасывание со слизистых оболочек дыхательных путей происходит довольно быстро, однако может снижаться при увеличении количества секрета. Кромогликат натрия быстро выводится из системного кровотока, в связи с чем последующие дозы, принимаемые в соответствии с рекомендованным режимом дозирования, не кумулируют. Кромогликат натрия обратимо связывается с белками плазмы (приблизительно 65%) и не метаболизируется. Выведение происходит в неизмененном виде с мочей и желчью приблизительно в одинаковых пропорциях. Период полувыведения в среднем составляет около 80 минут. Остальная часть выводится через легкие с выдыхаемым воздухом или оседает на стенках ротоглотки, затем проглатывается и выводится через кишечник.
Показания
Профилактическое лечение бронхиальной астмы, включая астму физического напряжения.
Противопоказания
Повышенная чувствительность к кромоглициевой кислоте, беременность (I триместр), детский возраст — до 2-х лет.
С осторожностью
Почечная/печеночная недостаточность, беременность (II-III триместры), период лактации.
Способ применения и дозы
Препарат применяется ингаляционно.
Капсулы Интала предназначены для применения только с ингалятором «Спинхалер». Их нельзя принимать внутрь.
Так как терапия Инталом по существу профилактическая, важно, чтобы пациент был проинструктирован о необходимости регулярного приема препарата в отличие от других препаратов, ингаляции которых служат для купирования приступов.
Взрослые и дети с 2-х лет
Режим дозирования одинаков для взрослых и детей.
Обычная доза: одна капсула 4 раза в день с интервалами 3-6 часов между HИМИ. В более тяжелых случаях или повышенном содержании антигена во внешней среде частота приема может быть увеличена до 6-8 раз в день (120-160 мг/сутки). Дополнительное дозирование может также иметь место для профилактики перед физической нагрузкой, вызывающей приступы удушья.
При достижении стойкого терапевтического эффекта возможен переход на минимальную поддерживающую дозу, обеспечивающую достаточный контроль над симптомами бронхиальной астмы.
Побочное действие
Со стороны дыхательной системы: раздражение слизистой оболочки дыхательных путей (охриплость, кашель). Крайне редко — легочные инфильтраты с эозинофилией.
Со стороны пищеварительного тракта: сухость во рту, тошнота.
Со стороны нервной системы: головокружение, головная боль.
Со стороны мочевыводящей системы: задержка мочи, нарушение функции почек.
Аллергические реакции: кожная сыпь, бронхоспазм, отек гортани, ангионевротический отек, анафилаксия наблюдались менее чем у 1 из 100 тыс. пациентов.
Передозировка
Кромоглициевая кислота обладает низкой токсичностью, поэтому риск передозировки и развития каких-либо токсических явлений небольшой. Не требует никаких действий, кроме медицинского наблюдения.
Взаимодействие с другими лекарственными средствами
Бета-адреностимуляторы, глюкокортикостероиды, антигистаминные лекарственные средства, теофиллин усиливают действие кромогликата натрия.
Сочетанное назначение кромоглициевой кислоты и глюкокортикостероидов позволяет уменьшить дозировку последних, а в отдельных случаях полностью их отменить.
Бронхолитики необходимо принимать (ингалировать) перед ингаляцией кромогликата натрия.
Особые указания
Капсулы Интала не применяются для купирования приступов бронхоспазма. Так как лечение препаратом носит профилактический характер, важно не прерывать его у пациентов, на которых препарат оказывает благотворное воздействие. При необходимости отмены лечения препаратом, это следует делать постепенно, в течение недели. При этом симптомы астмы могут возобновиться. Для пациентов, принимающих глюкокортикостероиды, при приеме Интала можно снизить дозу или отменить прием глюкокортикостероидов полностью. Необходимо наблюдение за пациентами при снижении дозы глюкокортикостероидов: предпочтительная скорость снижения дозы глюкокортикостероидов — 10% в неделю. Увеличение дозы глюкокортикостероидов может быть необходимо при утяжелении течения астмы и при инфекции, повышенном содержании антигена во внешней среде. Если возможно снижение дозы глюкокортикостероидов, то не следует прекращать прием Интала до установления нового режима дозирования глюкокортикостероидов.
Лечение пациентов с почечной/печеночной недостаточностью должно проходить под постоянным врачебным контролем.
Форма выпуска
По 10 капсул в блистер из ПВХ/алюминиевой фольги.
Каждый блистер упакован в герметично закрытый пакет-саше из алюминиевой фольги/ламинированной бумаги/ полиэтилена низкой плотности.
По 3 пакет-саше вместе с инструкцией по применению в картонную пачку.
Условия хранения
Список Б.
При температуре ниже + 30°С.
Не замораживать.
Хранить в недоступном для детей месте.
Срок годности
5 лет.
Не использовать по истечении срока годности, указанного на упаковке.
Условия отпуска из аптек
По рецепту.
Название и адрес изготовителя
Файсонс Лимитед (Великобритания), произведено Ай Ти Си Фарма CP Л, Италия. Виа Понтина км. 29, Помеция, Рим, Италия
Претензии потребителей направлять по адресу в России:
Москва, 115035, Садовническая ул. д. 82, стр. 2.
