Тимексон® (Timexon) инструкция по применению
📜 Инструкция по применению Тимексон®
💊 Состав препарата Тимексон®
✅ Применение препарата Тимексон®
📅 Условия хранения Тимексон®
⏳ Срок годности Тимексон®
Препарат отпускается по рецепту
Входит в список «Жизненно необходимых и важнейших лекарственных
препаратов»
Температура хранения: от 2 до 8 °С
Описание лекарственного препарата
Тимексон®
(Timexon)
Основано на общей характеристике лекарственного препарата (ОХЛП), утверждено
компанией-производителем и подготовлено для печатного справочника Видаль 2021 года.
Дата обновления: 2024.09.04
Владелец регистрационного удостоверения:
Контакты для обращений:
БИОКАД АО
(Россия)
Код ATX:
L03AX13
(Глатирамера ацетат)
Лекарственная форма
|
Препарат отпускается по рецепту |
Тимексон® |
Раствор для подкожного введения 20 мг/1 мл: шприцы 1 мл 28 шт. в компл. с салфетками спиртовыми рег. №: ЛП-(003579)-(РГ-RU) Предыдущий рег. №: ЛП-003875 |
Форма выпуска, упаковка и состав
препарата Тимексон®
Раствор для п/к введения от бесцветного до светло-желтого цвета, слегка опалесцирующий.
Вспомогательные вещества: маннитол — 40 мг, вода д/и — до 1 мл.
1 мл — шприцы трехкомпонентные из бесцветного стекла (1) — упаковки ячейковые контурные (28*) с вкладышами картонными — пачки картонные×.
1 мл — шприцы трехкомпонентные из бесцветного стекла (1) — упаковки ячейковые контурные (28*) с вкладышами картонными — пачки картонные.
1 мл — шприцы трехкомпонентные из бесцветного стекла (1) — упаковки ячейковые контурные (28**) с вкладышами картонными — пачки картонные.
* Допускается комплектация пачки спиртовыми салфетками в количестве 28 шт.
** 4 комплекта по 7 упаковок ячейковых контурных, скрепленных между собой.
× Допускается наклеивание этикетки контроля первого вскрытия.
Фармакологическое действие
Механизм действия глатирамера ацетата у пациентов с рассеянным склерозом (РС) не до конца изучен. Полагают, что глатирамера ацетат изменяет иммунные процессы, предположительно играющие основную роль в патогенезе рассеянного склероза. Данная гипотеза подтверждается результатами исследований, проведенных с целью изучения патогенеза экспериментального аллергического энцефаломиелита (ЭАЭ). ЭАЭ часто используют в качестве экспериментальной модели рассеянного склероза. Исследования, проведенные на животных и с участием пациентов с рассеянным склерозом, показали, что введение глатирамера ацетата вызывает периферическую индукцию и активацию глатирамера ацетат-специфических супрессорных Т-лимфоцитов.
Рецидивирующе-ремиттирующий рассеянный склероз (РРРС)
В трех контролируемых исследованиях 269 пациентов получали лечение глатирамера ацетатом. Первое двухлетнее исследование включало 50 пациентов (глатирамера ацетат – 25 пациентов, плацебо – 25 пациентов) с определенным РРРС в соответствии с действовавшими на тот момент времени критериями постановки диагноза и имевших, по крайней мере, 2 обострения заболевания за предыдущие 2 года. Второе исследование включало 251 пациента, получавших лечение в течение 35 месяцев (глатирамера ацетат – 125 пациентов, плацебо – 126 пациентов), третье исследование проводилось в течение 9 месяцев и включало 239 пациентов (глатирамера ацетат – 119 пациентов, плацебо – 120 пациентов), в этом исследовании были те же критерии включения, что и в первых двух исследованиях, и один дополнительный критерий – наличие у пациента по меньшей мере одного очага, накапливающего контраст (Gd+), визуализируемого на T1- взвешенных МРТ изображениях.
В клинических исследованиях было отмечено значимое уменьшение количества обострений у пациентов с РС, получавших лечение глатирамера ацетатом, по сравнению с группой плацебо.
В самом крупном контролируемом исследовании частота обострений в группе глатирамера ацетата по сравнению с группой плацебо снизилась на 32% (1.98 в группе плацебо и 1.34 в группе глатирамера ацетата).
В настоящее время имеются данные о 103 пациентах, получающих лечение глатирамера ацетатом в течение 12 лет.
Глатирамера ацетат также продемонстрировал превосходство над плацебо во влиянии на МРТ параметры, характерные для РРРС.
Нет доказательств того, что лечение глатирамера ацетатом влияет на прогрессирование инвалидизации, продолжительность и тяжесть рецидивов.
В настоящее время нет данных относительно применения препарата у пациентов с первично- или вторично-прогрессирующим рассеянным склерозом.
Клинически изолированный синдром (КИС)
Было проведено одно плацебо-контролируемое клиническое исследование (КИ), включавшее 481 пациента (глатирамера ацетат – 243 пациента, плацебо – 238 пациента) с достоверным единичным монофокальным неврологическим проявлением и МРТ признаками, более вероятными для РС (по крайней мере 2 очага в головном мозге, более 6 мм в диаметре на Т2-взвешенных МРТ изображениях) (КИС). Пациенты исключались из исследования, если симптом(ы) можно было объяснить любыми другими заболеваниями, нежели РС. После плацебо-контролируемой фазы исследования, пациенты продолжали лечение в открытой фазе (без плацебо): после перехода в клинически достоверный рассеянный склероз (КДРС) или после 3 лет лечения, в зависимости от того, что наступит раньше. Открытая фаза лечения продолжалась 2 года, при этом общая продолжительность лечения не должна была превышать 5 лет. Из 243 пациентов, изначально распределенных в группу лечения глатирамера ацетатом, 198 пациентов продолжили терапию в открытой фазе исследования. Из 238 пациентов, изначально распределенных в группу плацебо, 211 пациентов перешли в группу лечения глатирамера ацетатом во время открытой фазы исследования.
Во время плацебо-контролируемой фазы КИ продолжительностью 3 года, глатирамера ацетат статистически достоверно замедлял переход от КИС в клинически диагностируемый РС (в соответствии с критериями Позера), снижая риск трансформации на 45% (Hazard Ratio = 0.55; 95% ДИ [0.40; 0.77], p=0.0005). Доля пациентов, у которых КИС переходил в КДРС, составила 43% в группе плацебо и 25% в группе пациентов, получавших глатирамера ацетат.
Положительный лечебный эффект по сравнению с плацебо был также продемонстрирован во влиянии на количество новых очагов в головном мозге, визуализируемых на Т2-взвешенных изображениях и объем очагов на Т2-взвешенных изображениях по данным МРТ.
Фармакокинетика
Исследований фармакокинетики у пациентов не проводилось. Данные in vitro, а также ограниченные данные, полученные при участии здоровых добровольцев, показывают, что при п/к введении действующее вещество быстро абсорбируется, при этом большая часть его распадается на мелкие фрагменты в подкожной клетчатке.
Данные доклинических исследований
Доклинические данные, основанные на исследованиях фармакологической безопасности, токсичности при многократном введении, репродуктивной токсичности, генотоксичности или канцерогенности, не указывают на наличие особых вредных факторов для человека, кроме данных, уже включенных в разделы данной инструкции по медицинскому применению препарата. Ввиду отсутствия данных по фармакокинетике, невозможно определить допустимые пределы концентрации у человека в сравнении с животными.
У небольшого количества крыс и обезьян, которым вводили препарат по меньшей мере в течение 6 месяцев, отмечалось отложение иммунных комплексов в почечных клубочках. В 2-летнем исследовании на крысах не наблюдалось отложения иммунных комплексов в почечных клубочках.
У сенсибилизированных животных (морских свинок и мышей) после введения препарата отмечалась анафилаксия. Актуальность этих данных для человека неизвестна.
Токсическое действие в месте инъекции после повторного введения препарата животным относится к распространенным реакциям.
Показания препарата
Тимексон®
- рецидивирующе-ремиттирующий рассеянный склероз.
Режим дозирования
Препарат применяют в виде п/к инъекций.
Рекомендуемая доза — по 20 мг глатирамера ацетата (один заполненный раствором препарата шприц для инъекций) 1 раз/сут ежедневно, предпочтительно в одно и то же время дня, минимальный интервал между инъекциями – 24 ч.
Препарат не предназначен для в/в или в/м введения.
В настоящее время данные о длительности курса лечения отсутствуют. Решение о назначении длительного курса лечения должен принимать лечащий врач в каждом конкретном случае.
Пациентам рекомендуется пройти обучение по технике самостоятельного проведения инъекций. Первая инъекция (а также 30 мин после нее) должна проходить под наблюдением квалифицированного специалиста. Для снижения риска появления раздражения или боли в области инъекций каждый раз необходимо менять место инъекции.
Каждый шприц с глатирамера ацетатом предназначен только для однократного применения.
Проспективные, рандомизированные, клинически контролируемые исследования среди детей и подростков не проводились. Тем не менее, немногочисленные опубликованные данные свидетельствуют о том, что профиль безопасности у подростков в возрасте от 12 до 18 лет, ежедневно получавших глатирамера ацетат п/к, аналогичен профилю, наблюдаемому у взрослых. Нет достоверной информации о возможности применения глатирамера ацетата у детей младше 12 лет для того, чтобы рекомендовать лечение. Таким образом, глатирамера ацетат не должен применяться для данной возрастной группы.
Эффективность и безопасность препарата у пациентов пожилого возраста не изучались.
Эффективность и безопасность препарата у пациентов с почечной недостаточностью не изучались.
Рекомендации для пациентов по применению препарата
- Следует убедиться в том, что есть все необходимое для инъекции: одноразовый шприц, заполненный раствором препарата, контейнер для использованных шприцев, ватный тампон, смоченный спиртом.
- Перед инъекцией удалить этикетку с контурной ячейковой упаковки и извлечь одноразовый шприц.
- Выдержать шприц с раствором при комнатной температуре не менее 20 мин.
- Перед введением препарата тщательно вымыть руки водой с мылом.
- Внимательно осмотреть раствор в шприце. При наличии взвешенных частиц или изменений цвета раствора препарат не следует применять.
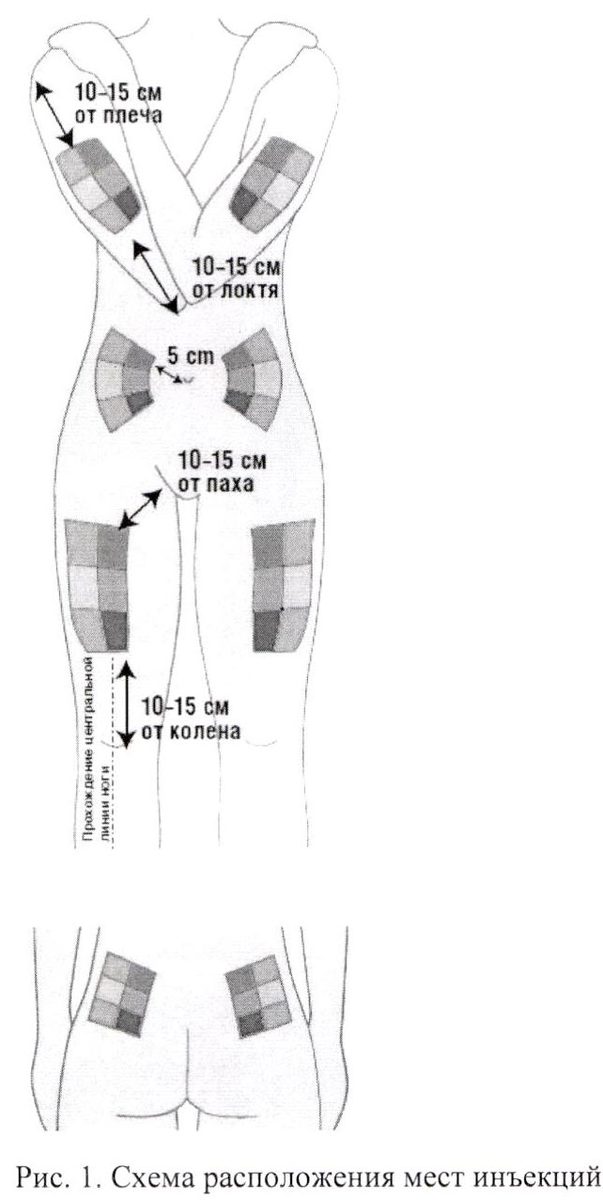
- Выбрать место для инъекции. Возможные зоны для инъекций обозначены на рис.1 и 2: руки, бедра, ягодицы, живот (следует избегать зоны примерно 5 см вокруг пупка). Не следует проводить инъекцию в болезненные места, обесцвеченные, покрасневшие участки кожи или области с уплотнениями и узелками. Выбирая новое место, можно уменьшить неприятные ощущения и боль во время инъекции. Внутри каждой инъекционной зоны достаточно места для нескольких инъекций. Рекомендуется составить схему мест инъекций и иметь ее при себе. Для инъекций на ягодицах и руках потребуется помощь другого человека.
Рис. 1. Схема расположения мест инъекций.
Рис. 2. Схема расположения мест инъекций в ягодичную область.
- Снять защитный колпачок с иглы.
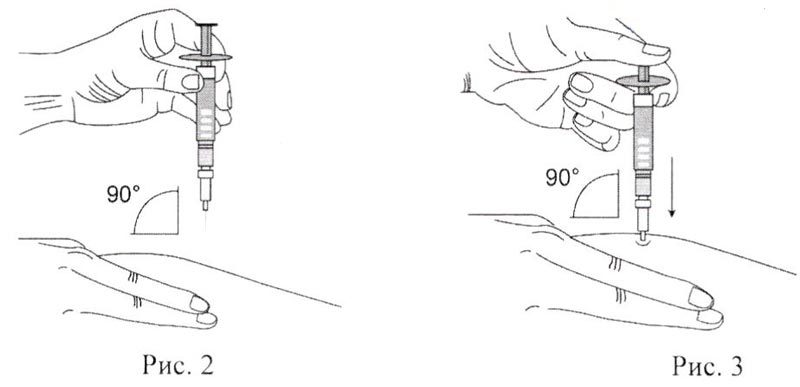
- Предварительно обработав место инъекции ватным тампоном, смоченным спиртовым раствором, слегка собрать кожу в складку большим и указательным пальцами (рис.3).
- Располагая иглу шприца перпендикулярно месту инъекции (рис. 4), проколоть кожу и, равномерно надавливая на поршень шприца, ввести его содержимое в место инъекции.
Рис. 3.
Рис. 4.
- Удалить иглу движением шприца перпендикулярно месту инъекции.
- Поместить шприц в контейнер для использованных шприцев.
Если пациент забыл ввести препарат Тимексон®, необходимо сделать инъекцию немедленно, как только пациент вспомнит об этом. Нельзя вводить двойную дозу препарата.
Побочное действие
Наиболее часто в ходе клинических исследований глатирамера ацетата отмечались реакции в месте инъекции. Проведенные плацебо-контролируемые исследования показали, что доля пациентов, сообщивших о данных нежелательных явлениях минимум один раз, составляла 70% для глатирамера ацетата и 37% — для плацебо. Чаще всего в клинических и пострегистрационных исследованиях наблюдались реакции в месте введения: покраснение, боль, уплотнение, зуд, отек, воспаление и гиперчувствительность; редко — липоатрофии и некроз кожи.
Реакция, ассоциированная, по крайней мере, с одним или более симптомов (вазодилатация, боль в груди, одышка, учащенное сердцебиение или тахикардия), которая проявляется через несколько минут после инъекции, называется немедленной постинъекционной реакцией. По крайней мере один из симптомов указанной реакции наблюдается минимум один раз у 31% пациентов, получавших глатирамера ацетат, по сравнению с 13% пациентов с плацебо.
Все нежелательные реакции, наиболее часто наблюдаемые у пациентов, получавших глатирамера ацетат по сравнению с группой плацебо, представлены ниже.
Частота развития нежелательных реакций классифицируется следующим образом: очень часто (≥1/10); часто (≥1/100, но <1/10); нечасто (≥1/1000, но <1/100); редко (≥/10000, но <1/1000).
Инфекции и инвазии: очень часто – инфекции, грипп; часто – бронхит, гастроэнтерит, средний отит, инфекция, вызванная Herpes simplex, ринит, периодонтальный абсцесс, вагинальный кандидоз*; нечасто – абсцесс, воспаление подкожно-жировой клетчатки, фурункулез, пиелонефрит, инфекция, вызванная Varicella zoster.
Новообразования, включая полипы и кисты: часто – доброкачественные новообразования кожи, новообразования; нечасто – рак кожи.
Со стороны кроветворной и лимфатической системы: часто – лимфаденопатия*; нечасто – лейкоцитоз, лейкопения, спленомегалия, тромбоцитопения, изменение морфологии лимфоцитов.
Со стороны иммунной системы: часто – реакции гиперчувствительности.
Со стороны эндокринной системы: нечасто – зоб, гипертиреоз.
Со стороны обмена веществ: часто – анорексия, повышение массы тела*; нечасто – непереносимость алкоголя, подагра, гиперлипидемия, гипернатриемия, снижение концентрации ферритина в сыворотке крови.
Со стороны психики: очень часто – тревога*, депрессия; часто – нервозность; нечасто – необычные сновидения, спутанность сознания, эйфория, галлюцинации, агрессивность, мания, расстройство личности, суицидальные попытки.
Со стороны нервной системы: очень часто – головная боль; часто – извращение вкуса, гипертонус мышц, мигрень, нарушения речи, обмороки, тремор*; нечасто – туннельный синдром запястья, когнитивные расстройства, судороги, дисграфия, дислексия, дистония, нарушение моторных функций, миоклонус, неврит, нейромышечная блокада, нистагм, паралич, в т.ч. малоберцового нерва, ступор, дефект полей зрения; частота неизвестна – головокружение****.
Со стороны органа зрения: часто – диплопия, нарушение зрения*; нечасто – катаракта, повреждение роговицы, сухость склеры и роговицы, кровоизлияние в глаз, птоз века, мидриаз, атрофия зрительного нерва.
Со стороны органа слуха и равновесия: часто – нарушение слуха.
Со стороны сердечно-сосудистой системы: очень часто – вазодилатация*; часто – ощущение сердцебиения*, тахикардия*; нечасто – экстрасистолия, синусовая брадикардия, пароксизмальная тахикардия, варикозное расширение вен.
Со стороны дыхательной системы: очень часто – одышка*; часто – кашель, сезонный ринит; нечасто – апноэ, ощущение удушья, носовое кровотечение, гипервентиляция легких, ларингоспазм, легочные нарушения.
Со стороны пищеварительной системы: очень часто – тошнота*; часто – аноректальные нарушения, запор, кариес, диспепсия, дисфагия, недержание каловых масс, рвота*; нечасто – колит, энтероколит, полипоз толстой кишки, отрыжка, язвенная болезнь пищевода, периодонтит, ректальное кровотечение, увеличение слюнных желез.
Со стороны печени и желчевыводящих путей: часто – отклонение показателей печеночных проб; нечасто – желчнокаменная болезнь, гепатомегалия.
Со стороны кожи и подкожных тканей: очень часто – кожная сыпь*; часто – экхимоз, гипергидроз, кожный зуд, заболевания кожи*, крапивница; нечасто – ангионевротический отек, контактный дерматит, узловатая эритема, кожные узелки.
Со стороны костно-мышечной системы: очень часто – артралгия, боль в спине*; часто – боль в шее; нечасто – артрит, бурсит, боль в боку, мышечная атрофия, остеоартрит.
Со стороны мочевыделительной системы: часто – императивные позывы к мочеиспусканию, поллакиурия, задержка мочи; нечасто – гематурия, нефролитиаз, заболевания мочевыделительного тракта, отклонения от лабораторных норм анализа мочи.
Беременность, послеродовое и перинатальное состояния: нечасто – самопроизвольный аборт.
Со стороны репродуктивной системы и молочной железы: нечасто – нагрубание молочных желез, эректильная дисфункция, пролапс тазовых органов, приапизм, заболевания простаты, отклонения в результатах цитологического исследования шейки матки, нарушение функции яичек, вагинальное кровотечение, вульвовагинальные нарушения.
Общие расстройства и нарушения в месте введения: очень часто – астения, боль в груди*, реакции в месте инъекции* и **, боль*; часто – озноб*, отек лица*, атрофия в месте инъекции***, местные реакции*, периферический отек, отек, лихорадка; нечасто – гипотермия, немедленная постинъекционная реакция, воспаление, киста, похмельный синдром, заболевания слизистых оболочек, поствакцинальный синдром, некроз в месте инъекции.
У пациентов с рассеянным склерозом, получавших глатирамера ацетат при проведении неконтролируемых клинических исследований, а также в период пострегистрационного применения, были зафиксированы редкие (≥1/10000, но <1/1000) случаи анафилактоидных реакций.
* Вероятность возникновения таких случаев у пациентов, принимавших глатирамера ацетат, составляет более 2% (>2/100) по сравнению с группой плацебо. Нежелательная реакция без знака «*» указывает на разницу, меньшую или равную 2%.
** «Реакции в месте введения» (различные виды) включает любые нежелательные явления, возникающие в месте инъекции, за исключением атрофии и некроза, которые приведены отдельно.
*** Относится к локализованной липоатрофии в месте инъекции.
**** Сообщалось о единичных случаях головокружений при применении препарата Тимексон® на этапе пострегистрационных неконтролируемых наблюдений.
Противопоказания к применению
- гиперчувствительность к глатирамера ацетату или маннитолу;
- детский и подростковый возраст до 18 лет (эффективность и безопасность не изучены).
С осторожностью: предрасположенность к развитию аллергических реакций, сердечно-сосудистые заболевания, нарушение функции почек, беременность, период грудного вскармливания.
Применение при беременности и кормлении грудью
Беременность
Исследования на животных не показали репродуктивной токсичности.
Опыт применения препарата у беременных женщин свидетельствует об отсутствии мальформативной или неонатальной токсичности (фетотоксичности). Эпидемиологические данные отсутствуют. Не рекомендуется применять препарат во время беременности за исключением случаев, когда ожидаемая польза терапии для матери превышает потенциальный риск для плода.
Период грудного вскармливания
Данные, свидетельствующие о выведении глатирамера ацетата, его метаболитов или антител с грудным молоком, отсутствуют.
Следует соблюдать осторожность при применении глатирамера ацетата в период грудного вскармливания. При необходимости применения препарата в период грудного вскармливания следует оценить ожидаемую пользу терапии для матери и потенциальный риск для ребенка.
Применение при нарушениях функции почек
С осторожностью следует назначать препарат при нарушении функции почек.
Применение у детей
Противопоказано применение препарата в детском и подростковом возрасте до 18 лет.
Применение у пожилых пациентов
Эффективность и безопасность препарата у пациентов пожилого возраста не изучались.
Особые указания
Начало лечения препаратом Тимексон® должно проводиться под контролем невролога и врача, имеющего опыт лечения рассеянного склероза.
Препарат не показан для первично- или вторично-прогрессирующего рассеянного склероза.
Пациенты должны быть проинформированы о возможности появления нежелательных реакций, в т.ч. немедленных постинъекционных реакций (приливы, боль в груди, одышка, учащенное сердцебиение), возникающих непосредственно после инъекции глатирамера ацетата (см. раздел «Побочное действие»). Большинство этих симптомов непродолжительны, спонтанно разрешаются без последствий.
При развитии серьезных нежелательных реакций пациенту следует немедленно прекратить терапию и обратиться к лечащему врачу или вызвать скорую медицинскую помощь. Решение о применение симптоматической терапии принимает врач.
Нет доказательств того, что определенные группы пациентов в большой степени подвержены риску возникновения таких реакций. Тем не менее, пациенты с сердечно-сосудистыми заболеваниями должны находиться под наблюдением врача на протяжении всего периода лечения.
Было выявлено несколько случаев судорог и/или анафилактоидных или аллергических реакций. Также могут редко встречаться серьезные реакции гиперчувствительности (бронхоспазм, анафилактическая реакция или крапивница). В случае тяжелых реакций необходимо назначить соответствующее лечение и отменить прием препарата.
В сыворотке крови пациентов были обнаружены антитела к глатирамера ацетату. После курса лечения средней продолжительностью 3-4 месяца была зафиксирована их максимальная концентрация, которая впоследствии снижалась и стабилизировалась на уровне, чуть выше базового. Нет данных, что антитела к глатирамера ацетату обладают нейтрализующим действием или оказывают влияние на клиническую эффективность препарата.
У пациентов с почечной недостаточностью следует контролировать функцию почек, хотя нет убедительных доказательств, что отложение иммунных комплексов оказывает воздействие на клубочковую фильтрацию.
Шприцы следует хранить в холодильнике при температуре 2-8°С.
Влияние на способность к управлению транспортными средствами и механизмами
Исследований по изучению влияния глатирамера ацетата на способность управлять транспортными средствами и механизмами не проводилось.
Передозировка
Получено несколько сообщений о передозировке (до 300 мг глатирамера ацетата). Никаких побочных реакций, кроме перечисленных в разделе «Побочное действие», при этом не наблюдалось.
Лечение: в случае передозировки показано тщательное наблюдение, симптоматическое и поддерживающее лечение.
Лекарственное взаимодействие
Взаимодействие между глатирамера ацетатом и другими лекарственными препаратами отдельно не оценивалось.
При одновременном применении глатирамера ацетата с препаратами, применяющимися для лечения рассеянного склероза, включая применение ГКС до 28 дней, клинически значимого взаимодействия не наблюдалось.
В исследовании in vitro было сделано предположение, что глатирамера ацетат имеет высокий уровень связывания с белками плазмы крови и не вытесняется из связи с белком плазмы крови самостоятельно, а также фенитоином или карбамазепином. Тем не менее, поскольку глатирамера ацетат обладает потенциальным воздействием на протеинсвязывающие вещества, необходимо контролировать его одновременное применение с другими лекарственными препаратами.
Условия хранения препарата Тимексон®
Препарат следует хранить в недоступном для детей месте при температуре от 2° до 8°С.
Срок годности препарата Тимексон®
Срок годности — 3 года. Не применять по истечении срока годности.
Условия реализации
Препарат отпускается по рецепту.
БИОКАД АО
(Россия)
|
198515 Санкт-Петербург, |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Синонимы, аналоги
Статьи
Внимательно прочтите эту инструкцию перед тем, как начать прием/использование лекарственного средства.
Сохраните инструкцию, она может потребоваться вновь.
Если у Вас возникли вопросы, обратитесь к врачу.
Регистрационный номер:
ЛП-005103
Торговое наименование:
Тимексон®
Международное непатентованное или группировочное наименование:
глатирамера ацетат
Лекарственная форма:
раствор для подкожного введения
Состав
1 мл раствора содержит:
действующее вещество: глатирамера ацетат – 40 мг;
вспомогательные вещества: маннитол – 40 мг, вода для инъекций – до 1 мл.
Описание
От бесцветного до светло-желтого цвета слегка опалесцирующий раствор.
Фармакотерапевтическая группа
Иммуномодулирующее средство.
Код ATX:
L03AX13
Фармакологические свойства
Фармакодинамика
Механизм действия глатирамера ацетата у пациентов с рассеянным склерозом не до конца изучен. Полагают, что глатирамера ацетат изменяет иммунные процессы, предположительно играющие основную роль в патогенезе рассеянного склероза. Данная гипотеза подтверждается результатами исследований, проведенных с целью изучения патогенеза экспериментального аллергического энцефаломиелита (ЭАЭ). ЭАЭ часто используют в качестве экспериментальной модели рассеянного склероза. Исследования, проведенные на животных и с участием пациентов с рассеянным склерозом, показали, что введение глатирамера ацетата вызывает периферическую индукцию и активацию глатирамера ацетат-специфических супрессорных Т-лимфоцитов.
Рецидивирующе-ремиттирующий рассеянный склероз
Результаты 12-месячного плацебо-контролируемого исследования подтвердили эффективность глатирамера ацетата в дозировке 40 мг/мл при подкожном введении три раза в неделю в отношении снижения частоты обострений.
При проведении клинического исследования критериями включения пациентов с рецидивирующе-ремиттирующим рассеянным склерозом были по меньшей мере одно документально подтвержденное клиническое обострение за последние 12 месяцев, или два обострения за последние 24 месяца, или одно обострение за последние 12-24 месяца при наличии по меньшей мере одного очага, накапливающего контраст (Gd+) и визуализируемого на Т1-взвешенных МРТ изображениях за последние 12 месяцев.
Первичной целью исследования было определение общего количества подтвержденных обострений. Вторичной целью – определение совокупного числа новых/увеличившихся очагов, выявляемых на Т2-взвешенных МРТ изображениях, и совокупное число очагов, накапливающих контраст и визуализируемых на Т1-взвешенных изображениях на 6-м и 12-м месяце исследования.
В исследование было рандомизировано 1404 пациента в соотношении 2:1 в группу, получавшую лечение глатирамера ацетатом в дозе 40 мг/мл (n=943) или в группу плацебо (n=461) соответственно. Обе группы были сопоставимы по исходным демографическим показателям, особенностям течения рассеянного склероза и МРТ параметрам. Пациенты имели в среднем 2,0 обострения заболевания в течение 2-х лет до скрининга.
По сравнению с группой плацебо у пациентов, получавших глатирамера ацетат в дозе 40 мг/мл три раза в неделю, наблюдалось статистически значимое снижение частоты обострений и совокупного количества очагов на Т2-взвешенных изображениях и очагов, накапливающих контраст на Т1-взвешенных изображениях, что соответствует терапевтическому эффекту глатирамера ацетата в дозе 20 мг/мл при его ежедневном введении. Прямой сравнительный анализ эффективности и безопасности глатирамера ацетата в дозе 20 мг/мл (при ежедневном введении) и 40 мг/мл (при 3-кратном еженедельном введении) в рамках данного исследования не проводился.
При проведении данного 12-месячного исследования не было получено доказательств влияния препарата на прогрессирование инвалидизации или длительности обострений. В настоящее время нет данных относительно применения препарата у пациентов с первично- или вторично-прогрессирующим рассеянным склерозом.
Фармакокинетика
Исследований фармакокинетики у пациентов не проводилось. Данные in vitro, а также ограниченные данные, полученные при участии здоровых добровольцев показывают, что при подкожном введении активное вещество быстро абсорбируется, при этом большая часть его распадается на мелкие фрагменты в подкожной клетчатке.
Данные доклинических исследований
Доклинические данные, основанные на исследованиях фармакологической безопасности, токсичности при многократном введении, репродуктивной токсичности, генотоксичности или канцерогенности, не указывают на наличие особых вредных факторов для человека, кроме данных, уже включенных в разделы данной инструкции по медицинскому применению препарата. Ввиду отсутствия данных по фармакокинетике, невозможно определить допустимые пределы концентрации у человека в сравнении с животным.
У небольшого количества крыс и обезьян, которым вводили препарат по меньшей мере в течение 6 месяцев, отмечалось отложение иммунных комплексов в почечных клубочках. В 2-летнем исследовании на крысах не наблюдалось отложения иммунных комплексов в почечных клубочках.
У сенсибилизированных животных (морских свинок и мышей) после введения препарата отмечалась анафилаксия. Актуальность этих данных для человека не известна. Токсическое действие в месте инъекции после повторного введения препарата животным относится к распространенным реакциям.
Показании для применения
Рецидивирующе-ремиттирующий рассеянный склероз.
Противопоказания
Гиперчувствительность к глатирамера ацетату или маннитолу; детский возраст до 18 лет (эффективность и безопасность не изучены): беременность.
С осторожностью
Предрасположенность к развитию аллергических реакций, сердечно-сосудистые заболевания, нарушение функции почек.
Применение при беременности и в период грудного вскармливания
Данных о применении глатирамера ацетата во время беременности нет, возможный риск такого применения во время беременности не установлен.
Проведенные исследования на животных недостаточны для установления влияния препарата на беременность, развитие эмбриона/плода, роды и постнатальное развитие. Глатирамера ацетат противопоказан во время беременности. Во время лечения глатирамера ацетатом необходимо использовать надежные методы контрацепции.
Неизвестно, выделяется ли глатирамера ацетат с грудным молоком, поэтому при необходимости применения в период лактации следует оценить ожидаемую пользу терапии для матери и потенциальный риск для ребенка.
Способ применения и дозы
В виде подкожных инъекций по 40 мг препарата Тимексон® (один заполненный раствором препарата шприц для инъекций) 3 раза в неделю, минимальный интервал между инъекциями – 48 часов. Препарат не предназначен для внутривенного или внутримышечного введения. В настоящее время данные о длительности курса лечения отсутствуют. Решение о назначении длительного курса лечения должен принимать лечащий врач в каждом конкретном случае.
Пациентам рекомендуется пройти обучение по технике самостоятельного проведения инъекций. Первая инъекция (а также 30 минут после нее) должна проходить под наблюдением квалифицированного специалиста. Для снижения риска появления раздражения или боли в области инъекции каждый раз необходимо менять зону для введения инъекции.
Каждый шприц с препаратом Тимексон® предназначен только для однократного применения.
Рекомендации для пациентов по применению препарата:
- Убедитесь в том, что у Вас есть все необходимое для инъекции: одноразовый шприц, заполненный раствором препарата Тимексон®, контейнер для использованных шприцев, ватный тампон, смоченный спиртом.
- Перед инъекцией извлеките одноразовый шприц из контурной ячейковой упаковки, удалив защитную бумажную полоску.
- Выдержите шприц с раствором при комнатной температуре не менее 20 минут.
- Перед введением препарата Тимексон® тщательно вымойте руки с мылом.
- Внимательно осмотрите раствор в шприце. При наличии взвешенных частиц или изменений цвета раствора его не следует применять.
- Выберите место для инъекции. Возможные зоны для самостоятельных инъекций обозначены на рис. 1: руки, бедра, ягодицы, живот (примерно 5 см вокруг пупка). Не следует проводить инъекцию в болезненные места, обесцвеченные, покрасневшие участки кожи или области с уплотнениями и узелками. Внутри каждой инъекционной зоны достаточно места для нескольких инъекций. Рекомендуется составить схему мест инъекций и иметь ее при себе. Для инъекций на ягодицах и руках Вам может потребоваться помощь другого человека.
- Снимите защитный колпачок с иглы.
- Предварительно обработав место инъекции ватной салфеткой, смоченной спиртовым раствором, слегка соберите кожу в складку большим и указательным пальцами.
- Располагая иглу шприца перпендикулярно месту инъекции (рис. 2), проколите кожу и, равномерно надавливая на поршень шприца, введите его содержимое в место инъекции (рис 3.).
- Удалите иглу движением шприца перпендикулярно месту инъекции.
- Поместите шприц в контейнер для использованных шприцев.
Если Вы забыли ввести препарат Тимексон®, сделайте инъекцию немедленно, как только вспомнили об этом. Нельзя вводить двойную дозу препарата.
Детский возраст
Препарат не рекомендован к применению у пациентов до 18 лет, поскольку клинические исследования у этих возрастных групп не проводились.
Пациенты пожилого возраста
Эффективность и безопасность препарата у пожилых людей не изучались.
Пациенты с нарушением функции почек
Эффективность и безопасность препарата у пациентов с почечной недостаточностью не изучались.
Побочное действие
Большинство данных по безопасности применения глатирамера ацетата 40 мг/мл были накоплены на основании использования препарата глатирамера ацетата 20 мг/мл в виде ежедневных инъекций. В этом разделе представлены данные, накопленные за время проведения 4-х плацебо-контролируемых клинических исследований по применению препарата глатирамера ацетата в виде раствора для подкожных инъекций в дозе 20 мг/мл 1 раз в день и 1 плацебо-контролируемого исследования применения глатирамера ацетата в виде раствора для подкожных инъекций в дозе 40 мг/мл 3 раза в неделю.
Глатирамера ацетат 20 мг/мл (применяется ежедневно)
Наиболее часто в ходе клинических исследований препарата глатирамера ацетата отмечались реакции в месте введения инъекции. Проведенные плацебо контролируемые исследования показали, что доля пациентов, сообщивших о данных нежелательных явлениях, минимум один раз в неделю составляла 70% для препарата глатирамера ацетата и 37% для плацебо. Чаще всего наблюдались покраснение, боль, уплотнение, зуд, отек, воспаление и гиперчувствительность.
Реакция, ассоциированная, по крайней мере, с одним или более симптомов (вазодилатация, боль в груди, одышка, учащенное сердцебиение или тахикардия), которая проявляется через несколько минут после инъекции, называется немедленной постинъекционной реакцией. По крайней мере один из симптомов указанной реакции наблюдался минимум один раз у 31% пациентов, получавших препарат глатирамера ацетат, по сравнению с 13% пациентов, получавших плацебо.
Все нежелательные реакции, наиболее часто наблюдаемые у пациентов, получавших глатирамера ацетат, по сравнению с группой плацебо, представлены ниже. Эти данные были получены в ходе четырех двойных слепых, плацебо контролируемых исследований с участием 512 пациентов, получавших глатирамера ацетат ежедневно и 509 пациентов, получавших плацебо, в течение 36 месяцев. В трех исследованиях участвовали 269 пациентов с диагнозом рецидивирующе-ремиттирующий рассеянный склероз, которые получали глатирамера ацетат ежедневно в течение 35 месяцев и 271 пациент из группы плацебо. В четвертом исследовании участвовали 243 пациента (группа глатирамера ацетата) с первым клиническим эпизодом заболевания, у которых был установлен высокий риск развития клинически подтверждённого рассеянного склероза, и 238 пациентов, получавших плацебо. Продолжительность исследования составляла 36 месяцев.
Частота развития нежелательных реакций классифицирована следующим образом: очень часто (≥1/10); часто (≥1/100, но <1/10); нечасто (≥1/1000, но <1/100); редко (≥1/10000, но <1/1000).
Инфекции и инвазии: очень часто – инфекции, грипп; часто – бронхит, гастроэнтерит, средний отит, Herpes simplex, ринит, периодонтальный абсцесс, вагинальный кандидоз*; нечасто – абсцесс, воспаление подкожно-жировой клетчатки, фурункулез, пиелонефрит, Herpes zoster.
Новообразования, включая полипы и кисты: часто – доброкачественные новообразования кожи, новообразования; нечасто – рак кожи.
Со стороны кроветворной и лимфатической систем: часто – лимфаденопатия*; нечасто – лейкоцитоз, лейкопения, спленомегалия, тромбоцитопения, изменение морфологии лимфоцитов.
Со стороны иммунной системы: часто – реакции гиперчувствительности.
Со стороны эндокринной системы: нечасто – зоб, гипертиреоз.
Со стороны обмена веществ и питания: часто – анорексия, увеличение массы тела*; нечасто – непереносимость алкоголя, подагра, гиперлипидемия, гипернатриемия, снижение концентрации ферритина в сыворотке крови.
Нарушение психики: очень часто – тревога*, депрессия; часто – нервозность, нечасто – необычные сновидения, психоз, эйфория, галлюцинации, агрессивность, мания, расстройства личности, суицидальные попытки.
Со стороны нервной системы: очень часто – головная боль; часто – извращение вкуса, гипертонус мышц, мигрень, нарушения речи, обмороки, тремор*; нечасто – туннельный синдром запястья, когнитивные расстройства, судороги, дисграфия, дислексия, дистония, нарушение моторных функций, миоклонус, неврит, нейромышечная блокада, нистагм, паралич, паралич малоберцового нерва, ступор, дефект полей зрения.
Со стороны органов зрения: часто – диплопия, нарушение зрения*; нечасто – катаракта, повреждение роговицы, сухость склеры и роговицы, кровоизлияние в глаз, птоз век, мидриаз, атрофия зрительного нерва.
Со стороны органов слуха и равновесия: часто – нарушение слуха.
Со стороны сердечно-сосудистой системы: очень часто – вазодилатация*; часто – ощущение сердцебиения*, тахикардия*; нечасто – экстрасистолия, синусовая брадикардия, пароксизмальная тахикардия, варикозное расширение вен.
Со стороны дыхательной системы: очень часто – одышка*; часто – кашель, сезонный ринит; нечасто – апноэ, ощущение удушья, носовое кровотечение, гипервентиляция легких, ларингоспазм, легочные нарушения.
Со стороны желудочно-кишечного тракта: очень часто – тошнота*; часто – аноректальные нарушения, запор, кариес, диспепсия, дисфагия, недержание каловых масс, рвота*; нечасто – колит, энтероколит, полипоз толстой кишки, отрыжка, язвенная болезнь пищевода, периодонтит, ректальное кровотечение, увеличение слюнных желез.
Со стороны печени и желчевыводящих путей: часто – отклонение показателей печеночных проб; нечасто – желчнокаменная болезнь, гепатомегалия.
Со стороны кожи и подкожно-жировой клетчатки: очень часто – кожная сыпь*; часто – экхимоз, гипергидроз, кожный зуд, заболевания кожи*, крапивница; нечасто – ангионевротический отек, контактный дерматит, узловатая эритема, кожные узелки.
Со стороны скелетно-мышечной системы и соединительной ткани: очень часто – артралгия, боль в спине*; часто – боль в шее; нечасто – артрит, бурсит, боль в боку, мышечная атрофия, остеоартрит.
Со стороны почек и мочевыделительной системы: часто – императивные позывы, Поллакиурия, задержка мочи; нечасто – гематурия, нефролитиаз, заболевания мочевыделительного тракта, отклонения от лабораторных норм анализа мочи.
Беременность, послеродовое и перинатальное состояние: нечасто – самопроизвольный аборт.
Со стороны половых органов и молочной железы: нечасто – нагрубание молочных желез, эректильная дисфункция, пролапс тазовых органов, приапизм, заболевания простаты, отклонение лабораторных показателей в мазках из канала шейки матки, нарушение функции яичек, вагинальное кровотечение, вульвовагинальные нарушения.
Прочие: очень часто – астения, боль в груди*, реакции в месте инъекции* и **, боль*; часто – озноб*, отек лица*, атрофия в месте инъекции***, местные реакции*, периферический отек, отек, лихорадка; нечасто – гипотермия, немедленная постинъекционная реакция, воспаление, киста, похмельный синдром, заболевания слизистых оболочек, поствакцинальный синдром, некроз в месте инъекции.
* Вероятность развития таких случаев у пациентов, принимавших глатирамера ацетат, составляет более 2% (>2/100) по сравнению с группой плацебо. Нежелательная реакция без знака «*» указывает на разницу, меньшую или равную 2%.
** «Реакции в месте инъекции» (различные виды) включает любые нежелательные явления, возникающие в месте инъекции, за исключением атрофии и некроза, которые приведены отдельно.
*** Относится к локализованной липоатрофии в месте инъекции.
В ходе четвертого клинического исследования, указанного выше, после плацебо-контролируемой фазы следовала «открытая» фаза исследования, которая длилась 5 лет. В течение этого исследования не было выявлено изменений установленного ранее профиля безопасности препарата глатирамера ацетата.
У пациентов с рассеянным склерозом, получавших глатирамера ацетат, при проведении неконтролируемых клинических исследований, а также в период постмаркетингового применения, были зафиксированы редкие (≥1/10000, но <1/1000) случаи анафилактоидных реакций.
Глатирамера ацетат в дозировке 40 мг/мл (применяется три раза в неделю)
В ходе двойного слепого, плацебо контролируемого исследования, которое длилось 12 месяцев, оценивалась безопасность препарата глатирамера ацетата (40 мг/мл) у 943 пациентов с диагнозом рецидивирующе-ремиттирующий рассеянный склероз в сравнении с группой плацебо, включавшей 461 пациента.
В целом у пациентов, которые принимали глатирамера ацетат 40 мг/мл три раза в неделю, нежелательные реакции в месте инъекции совпадали с теми, которые были отмечены при ежедневном введении глатирамера ацетата 20 мг/мл.
В частности, реакции в месте инъекции (РМИ) и немедленные постинъекционные реакции (НПИР) при введении глатирамера ацетата 40 мг/мл три раза в неделю наблюдались реже, чем при ежедневных инъекциях глатирамера ацетата (35,5% по сравнению с 70% для РМИ и 7,8% по сравнению с 31% для НПИР соответственно).
У 36% пациентов при применении глагирамера ацетата 40 мг/мл по сравнению с 5% пациентов на фоне приема плацебо наблюдались РМИ. У 8% пациентов, получавших препарат глатирамера ацетат 40 мг/мл, по сравнению с 2% пациентов, принимавших плацебо, были выявлены НПИР.
При этом были отмечены несколько специфических нежелательных реакций:
— у пациентов с рассеянным склерозом, получавших препарат глатирамера ацетата 20 мг/мл при проведении неконтролируемых клинических исследований, а также по результатам постмаркетингового опыта применения в редких случаях (≥1/10000, но <1/1000) наблюдалась анафилактическая реакция. У пациентов, принимавших препарат глатирамера ацетата 40 мг/мл, таких случаев было 0,3% (нечасто: ≥1/1000, но <1/100): – ни одного случая некроза в месте инъекции выявлено не было;
— у 2,1% пациентов, получавших глатирамера ацетат 40 мг/мл (часто: ≥1/100, но <1/10), наблюдались случаи покраснения кожи и боли в конечностях, которые не выявлялись в случае применения препарата глатирамера ацетата в дозе 20 мг/мл;
— у одного пациента (0,1%), получавшего препарат глатирамера ацетата 40 мг/мл (нечасто: ≥1/1000, но <1/100), наблюдалось лекарственно-индуцированное поражение печени и токсический гепатит, которые также редко встречались у пациентов с рассеянным склерозом, принимавших препарат глатирамера ацетата 20 мг/мл в период постмаркетингового наблюдения.
Передозировка
Получено несколько сообщений о передозировке (до 300 мг глатирамера ацетата). Никаких побочных реакций, кроме перечисленных в разделе Побочное действие, при этом не наблюдалось.
В случае передозировки показано тщательное наблюдение, симптоматическое и поддерживающее лечение.
Взаимодействие с другими лекарственными средствами
Взаимодействие между глатирамера ацетатом (40 мг/мл) и другими лекарственными препаратами отдельно не оценивалось. Нет данных о взаимодействии с интерфероном бета. Выявлено увеличение случаев реакции в месте инъекции при одновременном введении препарата глатирамера ацетата в дозе 40 мг/мл с глюкокортикоидами.
В исследовании in vitro было сделано предположение, что глатирамера ацетат имеет высокий уровень связи с белками плазмы крови и не вытесняется из связи с белком плазмы крови самостоятельно, а также фенитоином или карбамазепином. Тем не менее, поскольку препарат глатирамера ацетат (40 мг/мл) обладает потенциальным воздействием на протеин-связывающие вещества, необходимо контролировать его одновременное применение с другими лекарственными препаратами.
Особые указания
Начало лечения препаратом Тимексон® должно проводиться под контролем невролога и врача, имеющего опыт лечения рассеянного склероза. Препарат не показан для лечения первично- или вторично-прогрессирующего рассеянного склероза.
Пациенты должны быть проинформированы о возможности появления побочных реакций, в том числе возникающих непосредственно после инъекции препарата Тимексон®. Большинство этих симптомов непродолжительны, спонтанно разрешаются без последствий. При развитии серьезных побочных реакций следует немедленно прекратить терапию и обратиться к лечащему врачу или вызвать скорую медицинскую помощь. Решение о применении симптоматической терапии принимает врач.
Нет доказательств того, что определенные группы пациентов в большей степени подвержены риску возникновения таких реакций. Тем не менее, пациенты с сердечно-сосудистыми заболеваниями должны находиться под наблюдением врача на протяжении всего периода лечения.
Было выявлено несколько случаев судорог и/или анафилактоидных или аллергических реакций. Также могут редко встречаться серьезные реакции гиперчувствительности (бронхоспазм, анафилактическая реакция или крапивница). В случае тяжелых реакций необходимо назначить соответствующее лечение и отменить прием препарата.
В сыворотке крови пациентов были обнаружены антитела к глатирамера ацетату. После курса лечения средней продолжительностью 3-4 месяца была зафиксирована их максимальная концентрация, которая впоследствии снижалась и стабилизировалась на уровне, чуть выше базового.
Нет данных, что антитела к глатирамера ацетату обладают нейтрализующим действием или оказывают влияние на клиническую эффективность препарата.
У пациентов с почечной недостаточностью следует контролировать функцию почек, хотя нет убедительных доказательств, что отложение иммунных комплексов оказывает воздействие на клубочковую фильтрацию.
Влияние на способность управлять транспортными средствами, механизмами
Исследований по изучению влияния на способность управлять транспортными средствами и механизмами не проводилось.
Форма выпуска
Раствор для подкожного введения 40 мг/мл.
По 1 мл в трёхкомпонентные стерильные шприцы из бесцветного нейтрального стекла I гидролитического класса.
По 1 шприцу в контурную ячейковую упаковку из пленки полимерной. По 6 или 12 контурных ячейковых упаковок с инструкцией по применению и салфетками спиртовыми по 6 или 12 шт. помещают в пачку из картона.
Условия хранения
При температуре от 2 до 8 °С.
Хранить в недоступном для детей месте.
Срок годности
2 года.
Не применять по истечении срока годности, указанного на упаковке.
Условия отпуска
Отпускают по рецепту.
Владелец регистрационного удостоверения
ЗАО «БИОКАД», Россия, 198515, г. Санкт-Петербург, Петродворцовый район, пос. Стрельна, ул. Связи, д. 34, лит. А.
Производитель
ЗАО «БИОКАД», Россия, 143422, Московская обл.. Красногорский район, с. Петрово-Дальнее.
Организация, принимающая претензии потребителей
ЗАО «БИОКАД», Россия. 198515, г. Санкт-Петербург, Петродворцовый район, пос. Стрельна, ул. Связи, д. 34, лит. А.
*Цены в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Общая информация
Устаревшее наименование
—
Владелец
Номер регистрационного удостоверения РФ
ЛП-№(003579)-(РГ-RU)
Действующее вещество (МНН)
Форма выпуска / дозировка
Раствор для подкожного введения
Лекарственная форма ГРЛС
Раствор п/к
Состав
Действующим веществом является глатирамера ацетат.
1 мл раствора содержит 20,0 мг глатирамера ацетата.
Прочими вспомогательными веществами являются маннитол, вода для инъекций.
Описание препарата
От бесцветного до светло-желтого цвета слегка опалесцирующий раствор.
Фармако-терапевтическая группа
Иммуностимуляторы, другие иммуностимуляторы
Инструкция по применению Тимексон 20 мг/мл 1 мл 28 шт. раствор для подкожного введения
Состав, форма выпуска и упаковка
Раствор — 1 мл.:
активное вещество: глатирамера ацетат — 20 мг;
вспомогательные вещества: маннитол — 40 мг, вода для инъекций — до 1 мл.
Раствор для подкожного введения 20 мг/мл.
По 1 мл в трёхкомпонентные стерильные шприцы из бесцветного нейтрального стекла I гидролитического класса.
По 1 шприцу в контурную ячейковую упаковку из пленки полимерной. По 28 контурных ячейковых упаковок вместе с инструкцией по применению и салфетками спиртовыми в количестве 28 шт. в пачку из картона.
Аналог Копаксон.
Лекарственная форма
|
ТИМЕКСОН® |
Р-р д/п/к введения 20 мг/мл: 1 мл шприцы 28 шт. рег. №: ЛП-003875 от 03.10.16 — Действующее Дата перерегистрации: 20.07.17 |
Форма выпуска, упаковка и состав
Раствор для п/к введения от бесцветного до светло-желтого цвета, слегка опалесцирующий.
| 1 мл | |
|
глатирамера ацетат |
20 мг |
Вспомогательные вещества: маннитол — 40 мг, вода д/и — до 1 мл.
1 мл — шприцы бесцветного стекла (1) — упаковки ячейковые контурные (28) в компл. со спирт. салфетками — пачки картонные.
Фармакотерапевтическая группа
Иммуномодулирующее средство.
Фармакокинетика
В связи с особенностями химического строения глатирамера ацетата, представляющего собой смесь полипептидов, образованных природными аминокислотами, а так же низкой терапевтической дозировкой данные по фармакокинетике глатирамера ацетата имеют лишь ориентировочное значение. Основываясь на них, а так же на экспериментальных данных, считают, что после подкожной инъекции препарат быстро гидролизуется в месте введения. Продукты гидролиза, а также незначительная часть неизмененного глатирамера ацетата могут поступать в лимфатическую систему и частично достигать сосудистого русла. Определяемая концентрация глатирамера ацетата или его метаболитов в крови не коррелирует с терапевтическим действием.
Фармакодинамика
Тимексон® (глатирамера ацетат) является уксусно-кислой солью смеси синтетических полипептидов, образованных 4 природными аминокислотами: L-глутаминовой кислотой, L-аланином, L-тирозином и L-лизином и по химическому строению имеет элементы сходства с основным белком миелина.
Глатирамера ацетат изменяет течение патологического процесса при демиелинизирующем заболевании центральной нервной системы (ЦНС) — рассеянном склерозе, который относится к аутоиммунным заболеваниям, изменяющим соотношение Т-супрессоров в организме. Глатирамера ацетат осуществляет иммуномодулирующее действие в месте инъекции. Его терапевтический эффект опосредуется через системное распространение активированных Т-супрессоров. Глатирамера ацетат обладает специфическим механизмом действия, в основе которого лежит способность конкурентно замещать антигены миелина — основной белок миелина, миелиновый олигодендроцитарный гликопротеин и протеолипидный протеин в местах связывания с молекулами главного комплекса гистосовместимости класса 2, расположенных на антигенпредставляющих клетках. Следствием конкурентного вытеснения являются две реакции: стимуляция антиген-специфических супрессорных Т-лимфоцитов (Тh2-типа) и торможение антиген- специфических эффекторных Т-лимфоцитов (Тh1-типа). Активированные Т-супрессорные лимфоциты поступают в системную циркуляцию и проникают в ЦНС. Попадая в участок воспаления в ЦНС, указанные Т-лимфоциты реактивируются антигенами миелина, что приводит к продукции ими противовоспалительных цитокинов (ИЛ-4, ИЛ-6, ИЛ-10 и др.). Эти цитокины уменьшают локальное воспаление, подавляя местный воспалительный Т- клеточный ответ, что ведет к накоплению специфических противовоспалительных клеток Тh2-типа и торможению провоспалительной системы Тh1 — клеток.
Кроме того, глатирамера ацетат стимулирует синтез нейротрофического фактора Th-2 клетками и защищает мозговые структуры от повреждения (нейропротективное действие). Препарат не оказывает генерализованного влияния на основные звенья нормальных иммунных реакций организма, что принципиально отличает его от неспецифических иммуномодуляторов, включая препараты бета-интерферонов. Образующиеся антитела к глатирамера ацетату не обладают нейтрализующим действием, снижающим клинический эффект препарата.
Инструкция
Перед введением препарата убедитесь в том, что у Вас есть все необходимое для инъекции:
шприц, заполненный раствором препарата;
спиртовая салфетка.
Возьмите одну контурную ячейковую упаковку с заполненным шприцем из общей упаковки, которая должна храниться в холодильнике, и выдержите ее при комнатной температуре в течение не менее 20 минут.
Перед введением препарата тщательно вымойте руки водой с мылом.
Перед использованием следует осмотреть раствор в шприце. При наличии взвешенных частиц или изменении цвета раствора или повреждении шприца его не следует применять.
Выберите область тела для инъекции:
Руки (задняя поверхность плеча);
Бедра (передняя поверхность бедер кроме паха и колена);
Живот (кроме белой линии и пупочной области);
Ягодицы.
Достаньте шприц из индивидуальной контурной ячейковой упаковки, удалив бумажную маркировку (полоску).
Возьмите шприц в руку, которой Вы пишете. Снимите защитный колпачок с иглы.
Предварительно обработав место инъекции спиртовой салфеткой, слегка соберите кожу в складку большим и указательным пальцами.
Располагая шприц перпендикулярно месту инъекции, введите иглу в кожу под углом 90°; вводите препарат, равномерно нажимая на поршень шприца вниз до конца (до его полного опорожнения).
Удалите шприц с иглой движением вертикально вверх, сохраняя прежний угол наклона.
К месту инъекции можно приложить сухой стерильный ватный шарик. При необходимости можно заклеить пластырем. Не рекомендуется растирать или массировать место инъекции после введения препарата.
Использованные шприцы выбрасывайте только в специально отведенное место, недоступное для детей.
Не следует использовать для инъекции болезненные точки, обесцвеченные, покрасневшие участки кожи или области с уплотнениями и узелками.
Каждый день выбирайте новое место для укола, так Вы сможете уменьшить неприятные ощущения и боль на участке кожи в месте инъекции. Внутри каждой инъекционной области есть много точек для укола. Постоянно меняйте точки инъекций внутри конкретной области.
Рекомендуется составить схему смены мест инъекций и иметь ее при себе. На теле есть ряд областей, в которые трудно делать инъекции самостоятельно (ягодицы, руки), для этого Вам может потребоваться помощь другого человека.
Если Вы забыли ввести препарат Тимексон®, сделайте инъекцию немедленно, как только вспомнили об этом. Не допускается вводить двойную дозу препарата. Используйте следующий шприц только через 24 часа.
Не прекращайте применение препарата Тимексон® без консультации с врачом.
Показания к применению
Клинически изолированный синдром (единственный клинический эпизод демиелинизации, позволяющий предположить рассеянный склероз) с выраженностью воспалительного процесса, требующий применения внутривенных глюкокортикостероидов (для замедления перехода в клинически достоверный рассеянный склероз).
Рецидивирующе-ремиттирующий рассеянный склероз (для уменьшения частоты обострений, замедления развития инвалидизирующих осложнений).
Противопоказания к применению
Гиперчувствительность к глатирамера ацетату или маннитолу; детский возраст до 18 лет (эффективность и безопасность не изучены); беременность.
С осторожностью: предрасположенность к развитию аллергических реакций, сердечно-сосудистые заболевания, нарушение функции почек.
Беременность и лактация
Данных о применении глатирамера ацетата во время беременности нет, возможный риск такого применения во время беременности не установлен. Глатирамера ацетат противопоказан во время беременности. Во время лечения глатирамера ацетататом необходимо использовать надежные методы контрацепции. Неизвестно, выделяется ли глатирамера ацетат с грудным молоком, поэтому при необходимости применения в период лактации следует оцепить ожидаемую пользу терапии для матери и потенциальный риск для ребенка.
Побочные действия
Глатирамера ацетат безопасен и хорошо переносится пациентами. В отдельных случаях могут наблюдаться нижеперечисленные побочные реакции.
Со стороны крови и лимфатической системы: лимфаденопатия, лейкоцитоз, лейкопения, спленомегалия, тромбоцитопения. изменение структуры лимфоцитов.
Со стороны иммунной системы: реакция гиперчувствительности, анафилактоидная реакция, ангионевротический отек.
Со стороны эндокринной системы: гипертиреоз.
Со стороны обмена веществ: анорексия, повышение массы тела, непереносимость алкоголя, подагра, гиперлипидемия, гипернатриемия, снижение концентрации ферритина в сыворотке крови.
Со стороны нервной системы: головная боль, тревога, депрессия, эйфория, нервозность, патологические сновидения, психоз, галлюцинации, враждебность, мания, расстройство личности, суицидальное поведение, извращение вкуса, мигрень, обморок, туннельный синдром, когнитивные расстройства, тремор, судороги, дисграфия, дислексия, нарушение моторных функций, миоклонус, неврит, нейромышечная блокада, паралич, в том числе малоберцового нерва, ступор.
Со стороны органа зрения: диплопия, дефект полей зрения, нарушение движения глаз, катаракта, поражение роговицы, сухость склеры и роговицы, субконъюнктивальное кровоизлияние, птоз века, мидриаз, нистагм, атрофия зрительного нерва, нарушение зрения.
Со стороны органа слуха и равновесия: головная боль, нарушение слуха.
Со стороны сердечно-сосудистой системы: ощущение сердцебиения, тахикардия, экстрасистолия, синусовая брадикардия, пароксизмальная тахикардия, повышение артериального давления, варикозное расширение вен.
Со стороны дыхательной системы: кашель, одышка, сезонный ринит, апноэ, гипервентиляция легких, ларингоспазм.
Со стороны пищеварительной системы: тошнота, рвота, отек языка, запор, кариес, одонтогенный периостит, увеличение слюнных желез, диспепсия, дисфагия, отрыжка, язва пищевода, колит, энтероколит, полипоз толстой кишки, аноректальные нарушения, ректальное кровотечение.
Со стороны печени и желчевыводящих путей: желчнокаменная болезнь, гепатомегалия.
Со стороны кожи и подкожных тканей: экхимоз, гипергидроз, кожная сыпь, зуд, крапивница, контактный дерматит, узловатая эритема, кожные узелки.
Со стороны опорно-двигательного аппарата и соединительной ткани: артралгия, боль в шейном отделе позвоночника, боль в спине, артрит, бурсит, боль в боку, мышечная атрофия, остеоартрит.
Со стороны мочевыделительной системы: императивный позыв к мочеиспусканию, поллакиурия, задержка мочи, гематурия, нефролитиаз.
Со стороны половых органов и молочных желез: аменорея, увеличение молочных желез, эректильная дисфункция, пролапс тазовых органов, отклонение лабораторных показателей в мазках из канала шейки матки, нарушение менструального цикла, вульвовагинальные нарушения.
Инфекции: отит, бронхит, гастроэнтерит, обострение заболеваний, вызываемых Н. simplex, ринит, вагинальный кандидоз, воспаление подкожно-жировой клетчатки, фурункулез, пиелонефрит, опоясывающий герпес.
Прочие: реакции непосредственно после инъекции*, астения, усталость, озноб, повышение температуры тела, носовое кровотечение, периферические отеки, состояние похмелья.
* Реакции непосредственно после инъекции
Местные реакции: боль, покраснение, отек, абсцесс, гематома, липоатрофия, некроз кожи. Системные реакции: «приливы» крови, боль в груди, ощущение сердцебиения, состояние тревоги, одышка, затрудненное глотание, крапивница Указанные симптомы носят временный и ограниченный характер и не требуют специального вмешательства; они могут также начинаться спустя несколько месяцев после начала терапии, пациент может испытывать тот или иной симптом эпизодически.
Взаимодействие с лекарственными средствами
Взаимодействие между глатирамера ацетатом и другими лекарственными средствами изучено недостаточно. Не выявлено какого-либо лекарственного взаимодействия, включая одновременное применение глатирамера ацетата с препаратами, которые используются для терапии рассеянного склероза, в том числе с кортикостероидами (при комбинированном применении в течение до 28 дней). Крайне редко частота местных реакций может увеличиться.
Способ применения и дозы
В виде подкожных инъекций по 20 мг препарата глатирамера ацетата (один заполненный раствором препарата шприц для инъекций) один раз в сутки ежедневно предпочтительно в одно и то же время дня. Лечение длительное. Решение о прекращении терапии должен принимать лечащий врач.
Каждый шприц с препаратом глатирамера ацетата предназначен только для однократного применения.
Коррекция режима дозирования
Коррекция режима дозирования не предусмотрена. Препарат вводится в дозе 20 мг подкожно каждый день.
Передозировка
Данных о передозировке глатирамера ацетата нет. В случае передозировки показано тщательное наблюдение и симптоматическое лечение.
Меры предосторожности и особые указания
В начале лечения препаратом Тимексон® необходим контроль невролога и врача, имеющего опыт лечения рассеянного склероза.
Пациенты должны быть проинформированы о возможности появления побочных реакций, в том числе возникающих непосредственно после инъекции препарата Тимексон®.
Большинство этих симптомов непродолжительны, спонтанно разрешаются без последствий. При развитии серьезных побочных реакций следует немедленно прекратить терапию и обратиться к лечащему врачу или вызвать скорую медицинскую помощь. Решение о применении симптоматической терапии принимает врач.
Боль в груди, возникающая непосредственно после инъекций (см. раздел «Побочное действие»), как правило, носит преходящий характер, продолжается несколько минут, не имеет связи с другими симптомами, проходит самостоятельно без каких-либо клинических последствий. Механизм развития этого симптома неясен. При длительном применении (в течение нескольких месяцев) препарата Тимексон® в местах инъекций может развиться липоатрофия и в единичных случаях — некроз кожи. Для того чтобы предупредить развитие этих местных реакции, необходимо рекомендовать пациенту строго соблюдать последовательность мест для инъекций по схеме, в которой должно быть предусмотрено обязательное ежедневное изменение места для инъекции. Пациенты с нарушением функции почек или сердечно-сосудистыми заболеваниями должны находиться под контролем врача. В связи с тем, что препарат Тимексон® является иммуномодулирующим лекарственным средством и используется при лечении аутоиммунного заболевания — рассеянного склероза, его применение может сопровождаться изменениями функций иммунной системы, в связи с чем следует периодически контролировать состояние иммунной системы пациента. Шприцы следует хранить в холодильнике при температуре 2-8 °С.
Пациент должен быть проинформирован о возможных побочных реакциях, связанных с применением препарата.
Влияние на способность к вождению автотранспорта и управлению механизмами
На основании имеющихся данных нет необходимости в специальных мерах предосторожности для лиц, управляющих автомобилем или сложной техникой.
Условия хранения
В холодильнике при температуре +2 +8 градус
Условия отпуска из аптек
По рецепту
Тимексон
МНН: Глатирамера ацетат
Производитель: Биокад ЗАО
Анатомо-терапевтическо-химическая классификация: Glatiramer acetate
Номер регистрации в РК:
№ РК-ЛС-5№025526
Информация о регистрации в РК:
29.12.2021 — 29.12.2026
Номер регистрации в РБ:
11132/22
Информация о регистрации в РБ:
08.07.2022 — 08.07.2027
- русский
- қазақша
- Скачать инструкцию медикамента
Торговое наименование
Тимексон
Международное непатентованное название
Нет
Лекарственная
форма, дозировка
раствор
для подкожного введения, 20 мг/мл, 1 мл
Фармакотерапевтическая группа
Антинеопластические
и иммуномодулирующие препараты. Иммуностимуляторы. Иммуностимуляторы
другие. Глатирамера ацетат.
Код
АТХ L03AX13
Показания к применению
—
рассеянный склероз ремиттирующего течения (для уменьшения частоты
обострений, замедления развития инвалидизирующих осложнений).
Тимексон
не показан для терапии первично- или вторично-прогрессирующего
рассеянного склероза.
Перечень
сведений, необходимых до начала применения
Противопоказания
—
гиперчувствительность к глатирамера ацетату или маннитолу;
—
дети и подростковый возраст до 12 лет.
Необходимые
меры предосторожности при применении
—
пациенты должны быть проинструктированы по применению антисептических
методов при введении препарата, обучены методике самостоятельных
инъекций и проинформированы относительно процедуры безопасной
утилизации игл и шприцев. Полученные навыки должны периодически
контролироваться.
—
первую инъекцию необходимо проводить под наблюдением
квалифицированного специалиста
—
нельзя вводить препарат Тимексон внутривенно или внутримышечно —
препарат вводится только подкожно
—
не следует смешивать раствор, содержащийся в шприце, или вводить его
параллельно с каким-либо другим препаратом
—
при наличии нерастворенных частиц приготовленный раствор препарата
использованию не подлежит.
—
не замораживать содержимое шприца.
—
каждый шприц с препаратом предназначен только для однократного
применения
—
можно избавляться от использованных игл и шприцев только после того,
как они были предварительно помещены в твердую упаковку.
—
не прекращать применение препарата Тимексон без консультации с
врачом.
Взаимодействие
с другими лекарственными препаратами
Взаимодействие
между препаратом Тимексон и другими лекарственными средствами изучено
недостаточно. Нет данных о взаимодействии с интерфероном бета. При
одновременном применении препарата Тимексон с препаратами,
применяющимися для лечения рассеянного склероза, включая применение
глюкокортикостероидов до 28 дней, клинически значимых взаимодействий
не наблюдалось.
Глатирамера
ацетат связывается с белками плазмы крови, но он не замещается и не
замещает фенитоин или карбамазепин. Однако поскольку теоретически
препарат может влиять на распределение белоксвязывающих субстанций,
необходимо тщательно наблюдать за сопутствующим применением таких
лекарственных препаратов.
Специальные
предупреждения
В
начале лечения препаратом Тимексон необходим контроль врача-невролога
или врача, имеющего опыт лечения рассеянного склероза. Лечащий врач
должен предупредить пациента о возможности появления побочных
реакций, которые ассоциируются хотя бы с одним из следующих
симптомов: вазодилатация (прилив крови), гиперемия, боль в груди,
диспноэ (одышка), тахикардия, в течение нескольких минут после
инъекции препарата Тимексон.
Большинство
этих симптомов непродолжительны и проходят без осложнений. В случае
появления серьезной побочной реакции на препарат необходимо
немедленно прекратить прием препарата и сообщить об этом врачу или
вызвать скорую медицинскую помощь. В случае необходимости может быть
назначено симптоматическое лечение.
Нет
никаких доказательств повышенного риска возникновения побочных
реакций для любой группы пациентов. Несмотря на это, необходимо с
осторожностью применять Тимексон пациентам с нарушениями со стороны
сердца. Таких пациентов необходимо регулярно наблюдать во время
лечения.
Судороги
и/или анафилактоидные или аллергические реакции наблюдались редко.
Иногда могут развиваться серьезные реакции гиперчувствительности
(например, бронхоспазм, анафилаксия или крапивница). Если эти реакции
тяжелые, необходимо немедленно начать соответствующее лечение и
прекратить применение препарата.
Пациентам
с нарушением функции почек необходимо регулярно проводить контроль
лабораторных показателей. Хотя нет никаких свидетельств
гломерулярного депонирования иммунных комплексов у пациентов, но
такую возможность нельзя исключать. У пациентов, находящихся на
лечении препаратом Тимексон, были обнаружены антитела к глатирамера
ацетату в сыворотке крови. Максимальные уровни были достигнуты после
средней продолжительности лечения в 3-4 месяца и, после чего они
снижались и стабилизировались на уровне немного выше начального. Нет
доказательств тому, что образующиеся антитела обладают нейтрализующим
действием, снижающим клинический эффект препарата.
При
постмаркетинговом опыте применения препарата Тимексон сообщалось о
редких случаях выраженных нарушений функции печени (включая
проявления печеночной недостаточности и гепатита с желтухой). В
большинстве случаев выраженные нарушения функции печени проходили
после прекращения лечения. Проявления нарушений функции печени
происходили как в первые дни, так и через несколько лет от начала
лечения препаратом Тимексон.
Причиной
возникновения таких реакций чаще всего являлись: чрезмерное
употребление алкоголя, уже имеющееся в анамнезе повреждение печени,
использование других потенциально гепатотоксичных препаратов.
Пациентов
следует регулярно контролировать на предмет признаков повреждения
печени и инструктировать о необходимости немедленной медицинской
помощи при появлении симптомов поражения печени. В случае клинически
значимого повреждения печени, следует рассмотреть возможность
прекращения приема препарата Тимексон.
Существуют
ограниченные данные, указывающие, что профиль безопасности препарата
у подростков в возрасте от 12 до 18 лет, которые получали Тимексон
подкожно, подобен профилю у взрослых пациентов. Безопасность и
эффективность применения препарата Тимексон у детей в возрасте до 12
лет не изучена. Поэтому Тимексон не следует применять в этой
возрастной группе.
Влияние
на пожилых пациентов препарата Тимексон не изучено.
Применение
препарата Тимексон у пациентов с почечной недостаточностью специально
не изучалось.
Беременность
и период лактации
Беременность
Опыт применения препарата у беременных женщин
свидетельствует об отсутствии мальформативной или неонатальной
токсичности (фетотоксичности). Эпидемиологические данные отсутствуют.
Предпочтительно избегать использование препарата
Тимексон
во время беременности, если только польза для матери не перевешивает
риск для плода.
Лактация
Физико-химические
свойства и низкая абсорбция при пероральном приеме позволяют
предположить, что воздействие глатирамера ацетата на
новорожденных/младенцев через грудное молоко человека незначительно.
Результаты неинтервенционного ретроспективного исследования с
участием 60 детей не продемонстрировали отрицательного влияния
глатирамера ацетата во время грудного вскармливания на
новорожденных/младенцев матерей, получавших глатирамера ацетат, по
сравнению с находящихся на грудном вскармливании
новорожденных/младенцев матерей, не получавших какой-либо
болезнь-модифицирующей терапии. Оцениваемые результаты включали
параметры роста, частоту проявления задержки развития, частоту
госпитализации, а также терапию антибиотиками. Ограниченные данные из
опыта пострегистрационного применения препарата у людей также не
демонстрируют негативного воздействия глатирамера ацетата на
новорожденных/младенцев, находящихся на грудном вскармливании.
Препарат
Тимексон можно применять во время грудного вскармливания.
Перед планируемой беременностью, во время беременности и
в период лактации необходимо проконсультироваться с лечащим врачом.
Особенности
влияния лекарственного средства на способность управлять транспортным
средством или потенциально опасными механизмами
Исследования
по влиянию препарата Тимексон на способность управлять
автотранспортом и потенциально опасными механизмами не проводились.
Рекомендации
по применению
Режим дозирования
Рекомендуемая
доза составляет 20 мг глатимера ацетата (1 предварительно заполненный
шприц), которая вводится в виде подкожной инъекции один раз в сутки
ежедневно предпочтительно в одно и то же время дня, минимальный
интервал между инъекциями – 24 часа.
На
сегодня нет данных о продолжительности применения препарата.
Решение
о длительности лечения принимает врач конкретно по каждому случаю
Метод
и путь введения
Тимексон
вводится только подкожно. Каждый шприц с препаратом предназначен
только для однократного применения. Для
снижения риска появления раздражения или боли в области инъекции
каждый раз необходимо менять место для введения инъекции.
Рекомендации
для пациентов по применению препарата Тимексон в шприце:
Убедитесь
в том, что у Вас есть все необходимое для инъекции: одноразовый
шприц, заполненный раствором препарата, контейнер для использованных
шприцев, ватный тампон, смоченный спиртом.
Перед
инъекцией удалите этикетку с контурной ячейковой упаковки и
извлеките одноразовый шприц.
Выдержите
шприц с раствором при комнатной температуре не менее 20 минут.
Перед
введением препарата тщательно вымойте руки водой с мылом.
Внимательно
осмотрите раствор в шприце. При наличии взвешенных частиц или
изменений цвета раствора его не следует применять.
Выберите
место для инъекции. Возможные зоны для инъекций обозначены на рис.1
и 2: руки, бедра, ягодицы, живот (следует избегать зоны примерно 5
см вокруг пупка). Не следует проводить инъекцию в болезненные места,
обесцвеченные, покрасневшие участки кожи или области с уплотнениями
и узелками. Выбирая новое место, Вы сможете уменьшить неприятные
ощущения и боль во время инъекции. Внутри каждой инъекционной зоны
достаточно места для нескольких инъекций. Рекомендуется составить
схему мест инъекций и иметь ее при себе. Для инъекций на ягодицах и
руках Вам потребуется помощь другого человека.
Рис.1
Схема расположения Рис.2 Схема расположения мест
мест
инъекций. инъекций в ягодичную область.
Снимите
защитный колпачок с иглы.
Предварительно
обработав место инъекции ватным тампоном, смоченным спиртовым
раствором, слегка соберите кожу в складку большим и указательным
пальцами (рис.3).
Располагая
иглу шприца перпендикулярно месту инъекции (рис. 4), проколите кожу
и, равномерно надавливая на поршень шприца, введите его содержимое в
место инъекции.
Рис. 3
Рис. 4
Удалите
иглу движением шприца перпендикулярно месту инъекции.
Поместите
шприц в контейнер для использованных шприцов.
Частота
применения с указанием времени приема
Содержимое одного предварительно
заполненного препаратом шприца вводится в виде подкожной инъекции
один раз в сутки ежедневно предпочтительно в одно и то же время дня,
минимальный интервал между инъекциями – 24 часа.
Длительность
лечения
Решение о продолжительности
лечения принимается врачом индивидуально для каждого случая. Нельзя
прекращать применение препарата Тимексон без консультации с врачом.
Меры,
которые необходимо принять в случае передозировки
Были получены сообщения о нескольких случаях
передозировки препаратом Тимексон (до 300 мг глатирамера ацетата).
Эти случаи вызывали усиление побочных эффектов.
В
случае передозировки пациент должен находиться под наблюдением врача,
и пройти соответствующее симптоматическое лечение.
Меры,
необходимые при пропуске одной или нескольких доз лекарственного
препарата
При пропуске одной дозы, сделайте
инъекцию немедленно, как только вспомнили об этом. Не допускается
вводить двойную дозу препарата. Используйте следующий готовый шприц
только через 24 часа.
Указание
на наличие риска симптомов отмены
Обратитесь
к врачу или фармацевту за советом прежде, чем принимать лекарственный
препарат.
Описание
нежелательных реакций, которые
проявляются при стандартном применении ЛП и меры, которые следует
принять в этом случае
Очень
часто
—
грипп, инфекционные заболевания
—
тревожность, депрессия
—
головная боль
—
расширение кровеносных сосудов
—
одышка
—
тошнота
—
сыпь
—
артралгия, боль в спине
—
астения, боль в груди, реакции в месте
введения, боль
Часто
—
бронхит, гастроэнтерит, простой герпес, отит среднего уха, ринит,
абсцесс зуба, вагинальный кандидоз
—
доброкачественные новообразования кожи, другие
новообразования
—
увеличение лимфатических узлов
—
повышенная чувствительность
—
анорексия, увеличение массы тела
—
нервозность
—
дисгевзия, гипертония, мигрень, расстройства
речи, обморок, тремор
—
диплопия, нарушение зрения
—
нарушение слуха
—
учащенное сердцебиение, тахикардия
—
кашель, сезонный ринит
—
поражение аноректальной области, запор, зубной кариес, диспепсия,
дисфагия, недержание кала, рвота
—
отклонение от нормы функциональных проб печени
—
экхимоз, гипергидроз, зуд, воспаление кожи, крапивница
—
боль в области шеи
—
недержание мочи, поллакиурия, задержка мочи
—
озноб, отек лица, притупление
чувствительности в области инъекции, местные реакции, периферический
отек, отек, лихорадка
Нечасто
—
абсцесс, флегмона, фурункулез, герпес,
пиелонефрит
—
рак кожи
—
лейкоцитоз, лейкопения, спленомегалии,
тромбоцитопения, аномальная морфология лимфоцитов
—
зоб, гипертиреоз
—
непереносимость алкоголя, подагра, гиперлипидемия, повышения натрия в
крови, снижение ферритина сыворотки
—
необычные сновидения, спутанность сознания,
эйфория, галлюцинации, враждебность, помешательство, расстройство
личности, попытка самоубийства
—
туннельный синдром запястья, когнитивное расстройство, конвульсии,
дизгевзия, дислексия, дистония, нарушение координации движений,
миоклонические судороги, неврит, нервно-мышечные нарушения, нистагм,
паралич, паралич перонеального нерва, ступор, выпадение поля зрения
—
катаракта, поражение роговицы глаз, сухость в глазах, глазное
кровоизлияние, птоз век, мидриаз, атрофия зрительного нерва
— экстрасистолия, синусовая брадикардия, пароксизмальная
тахикардия
—
варикоз вен
—
апноэ, носовое кровотечение, гипервентиляция, спазм голосовой щели,
нарушение работы легких, ощущение удушья
—
колит, полип толстой кишки, энтероколит, отрыжка, язва пищевода,
периодонтит, кровотечение из прямой кишки, увеличение слюнной железы
—
холелитиаз, гепатомегалия
—
отек Квинке, контактный дерматит, нодозная эритема, узловатая эритема
—
артрит, бурсит, боль в боку, мышечная атрофия, остеоартрит
—
гематурия, нефролитиаз, заболевания мочевых путей, отклонение
показателей анализа мочи
— нагрубание молочных желёз, эректильная дисфункция,
опущение тазовых органов, приапизм, нарушение функции предстательной
железы, аномальные результаты мазка шейки матки, поражение яичек,
вагинальное кровотечение, вульвовагинальные нарушения
— киста, гипотермия, немедленная постинъекционная
реакция, воспаление, некроз в месте инъекции, воспаление слизистых
оболочек
—
пост-прививочный синдром
Редко
—
токсический гепатит, повреждение печени
Неизвестная
частота
—
проблемы с печенью или ухудшение состояния печени, включая печеночную
недостаточность (сообщалось о нескольких случаях трансплантации
печени), головокружение.
При
возникновении нежелательных лекарственных реакций обращаться к
медицинскому работнику, фармацевтическому работнику или напрямую в
информационную базу данных по нежелательным реакциям (действиям) на
лекарственные препараты, включая сообщения о неэффективности
лекарственных препаратов
РГП
на ПХВ «Национальный Центр экспертизы лекарственных средств и
медицинских изделий» Комитета медицинского и фармацевтического
контроля Министерства здравоохранения Республики Казахстан
http://www.ndda.kz
Дополнительные
сведения
Состав лекарственного препарата
Один
миллилитр препарата содержит
активное
вещество: глатирамера ацетат – 20,0 мг;
вспомогательные
вещества: маннитол – 40,0 мг, вода для
инъекций – до 1 мл.
Описание
внешнего вида, запаха, вкуса
От
бесцветного до светло-желтого цвета слегка опалесцирующий раствор.
Форма выпуска и упаковка
Раствор
для подкожного введения, 20 мг/мл.
По
1 мл препарата в трехкомпонентные стерильные шприцы из бесцветного
нейтрального стекла I гидролитического класса. Шприц, с одной
стороны, имеет впаянную иглу для инъекций из нержавеющей стали,
которая защищена пластмассовым колпачком с бутил каучуковым
уплотнителем. Шприц укупорен эластичным уплотнителем на поршень и
поршнем. На каждый шприц наклеивают этикетку самоклеящуюся.
По 1 шприцу в контурную ячейковую упаковку из пленки
ПВХ. По 28 контурных ячейковых упаковок вместе с инструкцией по
медицинскому применению на казахском и русском языках и картонными
вкладышами помещают в пачку из картона.
Допускается
комплектация пачки салфетками спиртовыми по 28 шт.
Срок
годности
2
года.
Не
применять по истечении срока годности!
Условия хранения
При
температуре от 2 до 8 °С.
Не
замораживать!
Хранить
в недоступном для детей месте!
Условия отпуска из аптек
По
рецепту.
Сведения
о производителе
АО
«БИОКАД», Россия, 198515, г. Санкт-Петербург, вн.тер.г.
поселок Стрельна, п. Стрельна, ул. Связи, д. 38, стр. 1.
Телефон:
+7(812) 380-49-33
факс:
+7(812) 380-49-34
e-mail:
biocad@biocad.ru
Держатель
регистрационного удостоверения
АО «БИОКАД», Россия, 198515, г.
Санкт-Петербург, вн.тер.г. поселок Стрельна, п. Стрельна, ул. Связи,
д. 38, стр. 1, помещ. 89.
Телефон:
+7(812) 380-49-33
факс:
+7(812) 380-49-34
e-mail:
biocad@biocad.ru.
Информацию
о развитии нежелательных реакций направлять по адресу:
safety@biocad.ru
Наименование,
адрес и контактные данные (телефон, факс, электронная почта)
организации на территории
Республики Казахстан, принимающей претензии (предложения) по качеству
лекарственных средств от потребителей и
ответственная за
пострегистрационное
наблюдение
за
безопасностью
лекарственного
средства
ТОО
«Карагандинский фармацевтический комплекс», Республика
Казахстан, 100009, г. Караганда, ул. Газалиева, строение 16.
Телефон:
(7212) 90-80-51, (7212) 90-80-43, факс: (7212) 90-65-49
E-mail:
kphk@kphk.kz, medinfo@kphk.kz
Сайт:
www.kphk.kz.
| 11132_22_p.pdf | 3.54 кб |
| 11132_22_s.pdf | 4.91 кб |
| Проект_ЛВ_PIL.063_.1_.KZ_.02_.03_.docx | 0.13 кб |
| 1.3_.3_Проект_ЛВ_Тимексон_Каз_clean_.docx | 0.12 кб |
Отправить прикрепленные файлы на почту
«Центр экспертиз и испытаний в здравоохранении» МЗ РБ Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники